
- DAZ.online
- News
- Pharmazie
- FDA-Warnung für ...
EMA-BEWERTUNG STEHT NOCH AUs
FDA-Warnung für Hepatitis C-Mittel Viekirax und Exviera
Stuttgart - 06.11.2015, 11:28 Uhr

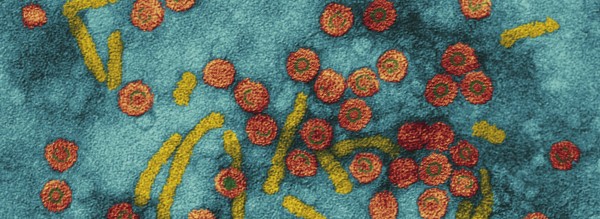
Hepatitis C: Die durch das Hep C-Virus ausgelöste Infektionskrankheit zeichnet sich durch eine hohe Rate der Chronifizierung aus. (Bild: fotoliaxrender / Fotolia)
Nicht nur bei schwerer, sondern auch bei mittelschwerer Leberfunktionseinschränkung gelten in den USA die Kombinationen Viekirax und Exviera in der Therapie einer chronischen Hepatitis C als kontraindiziert. Die FDA reagiert damit auf Schadensmeldungen. Derzeit noch offen ist, wie die EMA die Daten bewertet.
Die amerikanische Arzneimittelbehörde FDA hat Ende Oktober eine Warnung vor schweren Leberschäden ausgesprochen, die in der Therapie einer chronischen Hepatitis –C Erkrankung entstehen können. Diese sind in der Behandlung mittels einer antiviralen Kombination aus Viekirax (Ombitasvir, Paritaprevir und Ritonavir) und möglichweise zusätzlich Exviera (Dasabuvir) aufgetreten. Der FDA wurden seit Markteinführung der beiden Kombinationsmittel des Herstellers AbbVie 26 derartige Fälle gemeldet, die möglicherweise oder wahrscheinlich auf diese Arzneimittel zurückzuführen sind.
Der europäischen Prüfbehörde (EMA) wurden bereits die Beschreibungen der nach der Zulassung aufgetretenen Fälle von Dekompensation und Leberversagen vorgelegt, erklärt ein Sprecher des Herstellers AbbVie DAZ.online. Derzeit laufe die Bewertung der eingereichten Unterlagen. Ob und welche Schlussfolgerungen die EMA aus den eingereichten Unterlagen zieht, ist Gegenstand der laufenden Prüfung. Ein Analogschluss könne von der FDA-Entscheidung auf die EMA-Entscheidung nicht erfolgen, da es zwei um zwei unabhängige Prüfverfahren selbständiger regulatorischer Behörden handelt, erklärt der Firmensprecher.
Von Beginn an: Schwerkranke Patienten
Die Schadensereignisse, die der FDA gemeldet wurden, traten überwiegend in den ersten vier Wochen der Therapie auf und war durch einen akuten Anstieg des direkten Serumbilirubins und klinischen Zeichen einer hepatischen Dekompensation gekennzeichnet, schreibt das arznei-telegramm. Die meisten Patienten litten vor Beginn der Therapie an einer Leberzirrhose. Zehn Patienten entwickelten ein Leberversagen. Bei einigen Patienten verbesserte sich der Gesundheitszustand, nachdem die Arzneimittel abgesetzt wurden.
In der Fachinformation in den USA wurde bereits ein entsprechender Warnhinweis aufgenommen. Die Kombination Viekirax und Exviera ist nun nicht nur bei schwerer, sondern auch bei mittelschwerer dekompensierter Zirrhose (Child-Pugh B und C) kontraindiziert. Eine routinemäßige Überwachung wird bereits für die ersten vier Wochen empfohlen.
Die dekompensierten Zirrhosen sei eine schwierig zu behandelnde Patientengruppe, bei der es wenige Alternativen gibt. Die Betroffenen sind sowieso sehr krank, berichtet Michael Manns, Direktor der Klinik für Gastroenterologie, Hepatologie und Endokrinologie Medizinische Hochschule Hannover. „Wissenschaftlich ist es noch nicht definiert, bis wann sich im fortgeschrittenen Stadium eine anti HCV Therapie und somit eine Viruselimination noch lohnt“, erklärt der Professor.

























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.