Zu Arzneimitteln mit dem Wirkstoff „Loperamid“ und der
Wirkstoffkombination „Loperamid/Simeticon“ ist ein europäisches, die
periodischen Sicherheitsberichte bewertendes Verfahren durchgeführt worden. Der
Pharmakovigilanzausschuss PRAC der EMA (European Medicines Agency) ist dabei
auf Grundlage einer Überprüfung der Literatur und spontaner Meldungen zu dem
Schluss gelangt, dass ein Kausalzusammenhang zwischen der Verlängerung des
QRS-Komplexes und Loperamid nicht ausgeschlossen werden kann. Diese Erkenntnis
soll nun in die Abschnitte 4.4 und 4.9 der Fachinformationen aufgenommen
werden. Die Koordinierungsgruppe der Behörden der Mitgliedstaaten (CMDh, Coordination group for Mutual recognition and Decentralised procedures – human) hat
den wissenschaftlichen Schlussfolgerungen des PRAC zugestimmt,
sodass das Bundesinstitut für
Arzneimittel und Medizinprodukte (BfArM) mit Bescheid vom 2. April 2019 den einstimmigen Beschluss der
Koordinierungsgruppe umsetzt. Wird die „Verlängerung des QRS-Komplexes“ nun wie folgt in die
Produktinformationen eingefügt, gilt das Nutzen-Risiko-Verhältnis der
Loperamid-Präparate als unverändert:
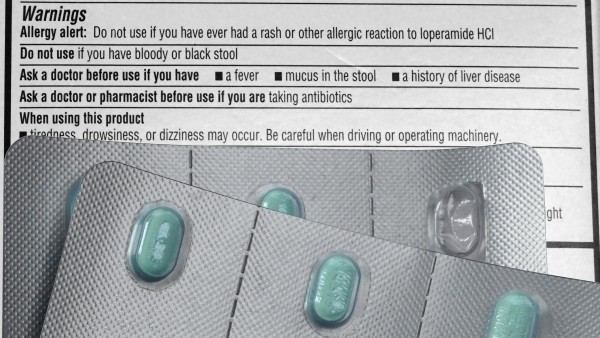
- „In Verbindung mit Überdosierung wurde über
kardiale Ereignisse, einschließlich QT-Verlängerung und Verlängerung des QRS-Komplexes und Torsade de pointes, berichtet.
Einige Fälle verliefen tödlich (siehe Abschnitt 4.9). Patienten dürfen die empfohlene
Dosis und/oder die empfohlene Behandlungsdauer nicht überschreiten.“
- „Bei Personen mit Überdosierungen von Loperamid
wurden kardiale Ereignisse, wie QT-Intervallverlängerung
und Verlängerung des QRS-Komplexes,
Torsades de pointes, sonstige schwere
ventrikuläre Arrhythmien, Herzstillstand und Synkopen, beobachtet (siehe
Abschnitt 4.4). Auch über Todesfälle wurde berichtet.“





























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.