
- DAZ.online
- DAZ / AZ
- DAZ 42/2016
- Molekulare Ketten, Räder...
Prisma
Molekulare Ketten, Räder und Maschinen
Chemie-Nobelpreis 2016 für Nano-Basteleien
Was man in der organischen Chemie gemeinhin „Kette“ (meistens: Seitenkette) nennt, ist mit einer Fahrradkette vergleichbar, denn die Kettenglieder sind quasi durch Gelenke miteinander verbunden; bei einer Fahrradkette sind zwar die Winkel zwischen zwei Gliedern veränderlich, aber sie bleibt immer gleich lang. Kohlenstoffketten sind etwas variabler, weil sie quasi Kugelgelenke besitzen. Ganz anders sind jedoch die klassischen Ketten konstruiert, wie sie schon unsere Vorfahren in der Bronzezeit schmieden konnten: Sie bestehen aus Gliedern, die ineinandergefügt und ansonsten völlig lose sind. Solche Ketten aus molekularen Ringen zu „schmieden“, ist Chemikern bereits in den 1960er-Jahren gelungen, indem sie Cyclodextrine und ihre Derivate ineinander fügten. Da die Ringe dieser Catenane (lat. catena = Kette) nicht durch kovalente Bindungen, sondern rein mechanisch aneinander gebunden waren, bedeuteten sie den ersten Schritt zur Konstruktion molekularer Maschinen.
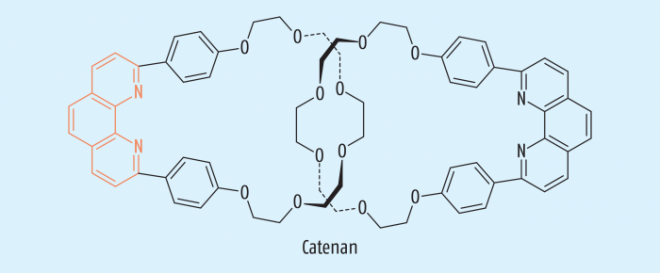
Der 1944 in Paris geborene Jean-Pierre Sauvage schaffte es 1983, die Ringbildung enorm zu beschleunigen. Er ging von einem mit zwei Phenylgruppen substituierten Phenanthrolin aus, das er an beiden Enden mit einem Polyethylenglykol (PEG) verband, um einen Makrozyklus zu erhalten (Abb. 1). Um in diesen Makrozyklus einen neuen Ring einzufügen, platzierte er in seine Mitte ein einwertiges Kupfer-Ion, das durch nicht-kovalente Wechselwirkungen den Makrozyklus und die beiden halbmondförmigen Bauelemente an die „richtigen“ Stellen positioniert (man spricht deshalb auch von „topologischer Chemie“). Nun brauchte Sauvage nur noch das Kupfer-Ion mithilfe von Kaliumcyanid zu entfernen, damit sich die Bauteile zu einem neuen Makrozyklus verbinden, der dank der Topologie das zweite Glied einer Kette bildet. Nach diesem Schema lässt sich die Kette beliebig verlängern. Diese „Template-Synthese“ ist heute so perfektioniert, dass die Ausbeute bei idealem Hochdruck etwa 90 Prozent beträgt.
Der 1942 in Edinburgh geborene, heute in den USA lebende Fraser Stoddart spezialisierte sich auf mechanische Verbindungen von zyklischen und linearen Polymeren, wobei die linearen Bauteile voluminöse Endgruppen besitzen. Da der nicht kovalent gebundene Makrozyklus zwischen den beiden Enden frei um die Achse rotieren kann, wurden diese Verbindungen Rotaxane genannt. Sie waren ebenfalls seit den 1960er-Jahren bekannt, doch Stoddart gab ihnen eine andere Qualität, als er Moleküle mit elektronischen Teilladungen verwendete. 1991 schuf er ein Rotaxan mit einem Ring aus elektrophilen Bipyridinen und einer PEG-Achse, in die zwei nukleophile Hydrochinon-Gruppen eingebaut waren. Wie ein Shuttle bewegte sich der Makrozyklus nun zwischen beiden Hydrochinon-Gruppen hin und her. Stoddart experimentierte darauf mit asymmetrischen Achsen und präsentierte drei Jahre später eine PEG-Achse, in der ein Diaminobenzol das eine Hydrochinon ersetzte. Durch wechselweise elektrochemische Oxidation und Reduktion mithilfe zugeführter Energie ließ sich nun der Positionswechsel des Makrozyklus zwischen den beiden „Stationen“ auf der Achse steuern. Damit war eine weitere Stufe auf dem Weg zur Konstruktion von molekularen Maschinen erklommen.
Etwa zur selben Zeit wie Stoddart experimentierte auch Sauvage mit asymmetrischen Ringen, die unterschiedliche elektronische Teilladungen aufwiesen. So ersetzte er bei dem einen Ring des oben beschriebenen Catenans (Abb. 1) die Phenanthrolin-Gruppe durch drei Pyridine. In der Mitte des Catenans positionierte er ein Kupfer-Ion, das elektrochemisch oxidiert und reduziert wurde. Da Cu+ das Terpyridin abstößt, während Cu2+ dasselbe anzieht, rotierte der asymmetrische Ring um das Kupfer-Ion.
Vor und zurück
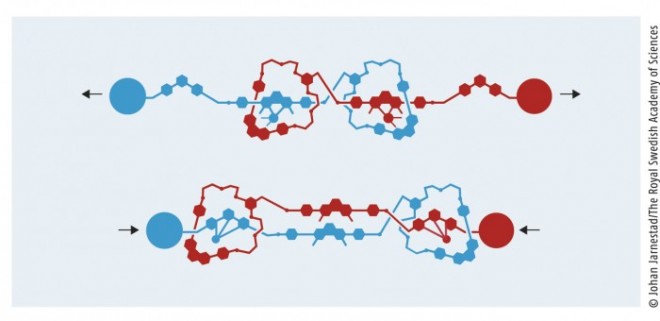
Die Arbeitsgruppen von Sauvage und Stoddart inspirierten sich gegenseitig und führten nun auch gemeinsame Projekte durch. Im Jahr 2000 schuf die Sauvage-Gruppe ein komplexes Rotaxan mit zwei identischen Bauteilen, die aus einer linearen Komponente mit nur einer voluminösen Endgruppe und einem Ring am anderen Ende bestanden; wie bei Rotaxanen üblich rotiert der Ring des einen Bauteils um die Achse des anderen Bauteils. Dabei können sich die Bauteile um die Distanz von 2 nm auseinanderziehen bzw. ineinanderschieben (s. Abb. 2).
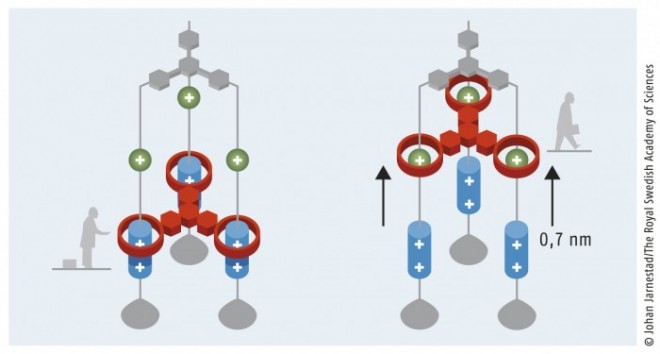
2004 antwortete die Stoddart-Gruppe mit einem „molekularen Fahrstuhl“, einem Drillings-Rotaxan, bei dem die axialen Komponenten jeweils zwei „Stationen“ aufweisen; die drei miteinander verbundenen Makrozyklen fahren aufgrund elektrischer Impulse zwischen diesen Stationen hin und her (Abb. 3).
Immer nur vorwärts
Das Bestreben der „mechanischen Chemiker“ ging dahin, die linearen Bewegungen durch kreisende Bewegungen zu ersetzen, doch Catenane und Rotaxane führten hier nicht weiter. Der 1951 geborene und in Groningen forschende Bernard Feringa experimentierte stattdessen mit chiralen helikalen Alkenen, die sich bei pulsierender UV-Licht-Bestrahlung aufgrund von cis-trans-Isomerisationen um die C=C-Doppelbindung drehen. 1999 konnte er einen molekularen Motor vorstellen, der die Drehbewegung immer in dieselbe Richtung ausführt: Nach jeder UV-Licht-induzierten 180°-Drehung führt ein Wärmestrahl zur drehsymmetrischen Umkehr der Chiralität, sodass der folgende UV-Licht-Impuls das Molekül in derselben Richtung weiterdreht (und nicht zurückdreht). Inzwischen haben solche „Motoren“ eine Frequenz von 12 MHz. Werden mehrere Motoren koordiniert, sind sogar Nanofahrzeuge möglich (Abb. 4).
Die Medaillen des Nobelpreises werden am 10. Dezember, dem Todestag Alfred Nobels, vom schwedischen König persönlich überreicht. Das Preisgeld, das sich die drei Chemiker teilen, beträgt acht Millionen Schwedische Kronen (ca. 830.000 Euro). |





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.