
Biopharmazeutika-Folgepräparate
Biosimilars

NMG Pharma ruft weitere Biopharmazeutika zurück
Der in Bonn ansässige Händler NMG Pharma hat in dieser Woche erneut einen Arzneimittelrückruf gestartet. Betroffen sind, wie bereits im vergangenen Monat, hochpreisige Biopharmazeutika. Nach ... » Weiterlesen

Ist der Produktionsstandort Deutschland für die Biosimilars-Welle gerüstet?
Spätestens durch die Valsartan-Krise ist auch der breiten Öffentlichkeit bewusst geworden, dass Generika zu großen Anteilen außerhalb Europas produziert werden. Doch wie sieht es bei der ... » Weiterlesen

Zulassungsbehörde FDA legt Plan zur Förderung von Biosimilars vor
Die US-Administration macht Ernst mit ihrem Vorhaben, die Arzneimittelausgaben zu senken. Dabei sollen Biosimilars eine entscheidende Rolle spielen. So hat die Zulassungsbehörde FDA nun einen Elf-... » Weiterlesen
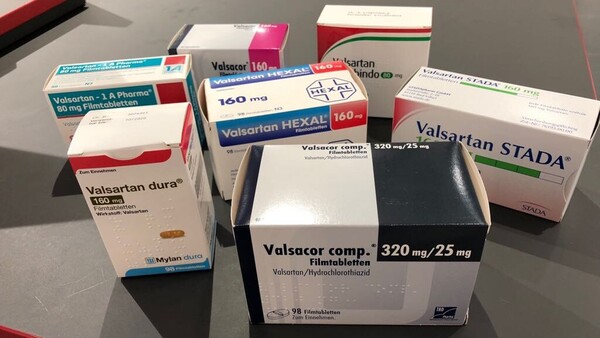
Welche Tragweite könnten die Valsartan-Rückrufe haben?
Das Bundesinstitut für Arzneimittel und Medizinprodukte hat europaweite Rückrufe für den Blutdrucksenker Valsartan angekündigt. Offenbar gibt es produktionsbedingte Verunreinigungen mit dem ... » Weiterlesen
Das Ende der Tablette
Seit mehreren Hundert Jahren stellen die Apotheken sicher, dass Arzneimittel logistisch und qualitativ einwandfrei vom Hersteller zum Patienten gelangen. Am häufigsten werden Arzneimittel oral ... » Weiterlesen

Generika für den Export
ks | Zukünftig sollen Unternehmen mit Sitz in der EU bereits dann Generika oder Biosimilars herstellen dürfen, wenn für das Original noch das ergänzende Schutzzertifikat gilt – allerdings nur f... » Weiterlesen
Generika und Biosimilars trotz Schutzzertifikat
Die EU-Kommission will die Vorschriften zum geistigen Eigentum im Pharmabereich nachbessern. Sie hat einen Vorschlag vorgelegt, der es Unternehmen mit Sitz in der EU erlauben soll, bereits dann ... » Weiterlesen

Pfizer arbeitet an neuen Biosimilars
Bereits drei Biosimilars hat Pfizer in der EU zugelassen: Infliximab, Filgrastim und Epoetin zeta. In den nächsten Jahren plant der US-Konzern sein Portfolio konsequent auszubauen. Neben Rituximab ... » Weiterlesen

Trastuzumab-Biosimilar auf dem Markt
Im Februar hatte die Europäische Kommission die Zulassung für Herzuma® erteilt, seit Mai ist der monoklonale Antikörper Trastuzumab nun als Biosimilar in Deutschland verfügbar. Eingesetzt wird ... » Weiterlesen

„Wir brauchen nicht jedes Jahr eine große Arzneimittel-Reform“
Generikahersteller fühlen sich unter Druck. Die Anforderungen an sie und ihre Produkte steigen, doch der Preis muss niedrig bleiben. Wie lässt sich unter diesem Druck Qualität und Lieferfähigkeit ... » Weiterlesen
Sind Biopharmazeutika Naturheilmittel?
Ein Großteil der Deutschen kann sich unter dem Begriff Biopharmazeutika nichts vorstellen, und von den wenigen, die sich eine Definition zutrauen, liegen die meisten falsch. Das ist das Ergebnis ... » Weiterlesen

Doppelt so viele Biosimilars
eda | Gut jeder vierte Euro bei den Arzneimittelgesamtausgaben entfällt mittlerweile auf Biologicals. Mit jährlichen Zuwächsen von rund zehn Prozent bewegt sich Deutschland damit im globalen ... » Weiterlesen
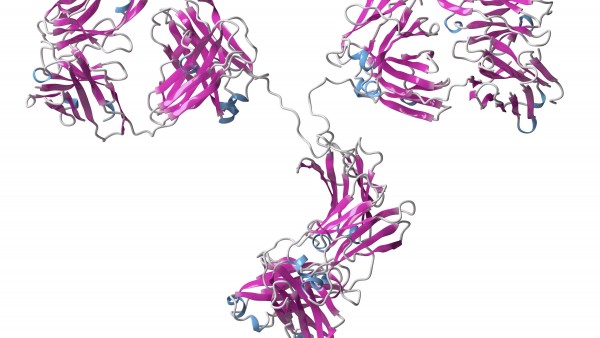
Trastuzumab-Biosimilar von Celltrion erhält EU-Zulassung
Roches Brustkrebsblockbuster Herceptin® bekommt weitere Konkurrenz in Europa. Die EU-Kommission hat nämlich nach Ontruzant® das zweite Trastuzumab-Biosimilar zugelassen – Herzuma® von Celltrion... » Weiterlesen

Abbvie trotzt Konkurrenz
eda/dpa | Auch der US-Pharmakonzern Abbvie zählt sich zu den Profiteuren der US-Steuerreform. Die Ergebnisprognose für 2018 konnte dank einer voraussichtlich niedrigeren effektiven Steuerrate erhö... » Weiterlesen

Weiteres Lantus-Biosimilar kurz vor der EU-Zulassung
Sanofis Basalinsulin Lantus® bekommt noch mehr Konkurrenz. Der Humanarzneimittelausschuss der EMA hat nämlich ein weiteres Biosimilar zur Zulassung empfohlen. Diesmal ist es die Firma Mylan, die ein... » Weiterlesen

AbbVie erfolgreich dank Humira
Der US-Pharmakonzern AbbVie blickt auf ein erfolgreiches Jahr 2017 zurück und will daher seine Prognosen für das laufende Jahr nach oben korriegieren. An der Umsatzsteigerung des letzten Jahres war ... » Weiterlesen

Ein weiteres Werkzeug zur Versorgungssteuerung?
Auf dem diesjährigen BMC-Kongress in Berlin wurde auch über das Arztinformationssystem (AIS) diskutiert. Themen waren unter anderem mögliche therapierelevante Fehlerquellen in dem System, mit dem ... » Weiterlesen

Welche Arzneimittel 2018 aus dem Patent laufen
In diesem Jahr laufen nach Information der Arbeitsgemeinschaft Pro Biosimilars mehrere Arzneimittel-Patente aus, hinter denen in Deutschland ein Umsatzpotenzial von insgesamt 1.324 Millionen Euro ... » Weiterlesen

Roche verklagt Sandoz in Japan
eda | Vor einem Gericht in Tokio will eine Roche-Tochter ein Verkaufsverbot für ein Biosimilar von Rituximab (MabThera®) erwirken. Sandoz und die lokale Vertreiberin Kyowa Hakko Kirin hätten drei ... » Weiterlesen
Cosentyx soll sich gegen Adalimumab bewähren
Wie schlägt sich das Psoriasis-Arzneimittel Cosentyx® im Vergleich zum TNFα-Antikörper Adalimumab? Das will Hersteller Novartis wissen und initiiert zwei Vergleichsstudien. Als Referenzen kommen ... » Weiterlesen

Fresenius beantragt erste Biosimilar-Zulassung
Abbvies Blockbuster Humira® muss sich auf weitere Nachahmer gefasst machen. Fresenius Kabi hat den Zulassungsantrag für sein Biosimilar bei der Europäischen Arzneimittelagentur eingereicht. Für ... » Weiterlesen

Über 27.000 Rabattverträge
hb | Generikaunternehmen haben im Jahr 2016 mit chemisch definierten Nachahmerprodukten bzw. Biosimilars 77,2 Prozent des Arzneimittelbedarfs der GKV (nach DDD) abgedeckt – das teilt der ... » Weiterlesen

Gute Zahlen, aber Biosimilar-Konkurrenz sitzt Roche im Nacken
Roche kann sich 2017 bislang über gute Zahlen freuen. In den ersten neun Monaten des Jahres wuchs der Umsatz dank guter Geschäfte mit Innovationen. Allerdings macht den Schweizern die Biosimilar-... » Weiterlesen























juustright / stock.adobe.com