
Thema
Committee for Medicinal Products for Human Use

Liraglutid bald für Kinder?
Der Humanarzneimittelausschuss CHMP empfiehlt, die Indikation von Liraglutid zur Behandlung von Diabetes mellitus Typ 2 zu erweitern, und zwar für Kinder ab zehn Jahren. Victoza soll als ... » Weiterlesen
Vorerst kein Romosozumab in der EU
Der Humanarzneimittelausschuss der EMA, CHMP, spricht sich gegen die EU-Zulassung von Romosozumab aus. Der Sclerostin-Antikörper zur Behandlung von Osteoporose senkte in den Studien FRAME und ARCH ... » Weiterlesen
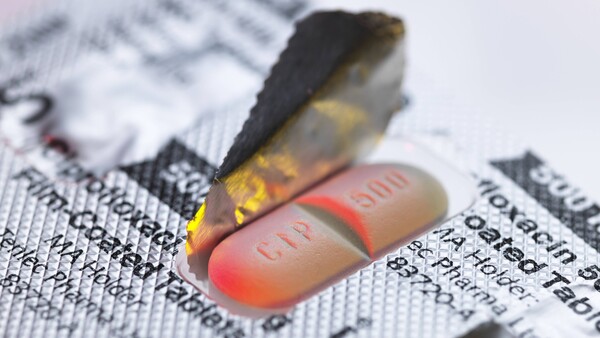
Ärzte verordnen zu viele Fluorchinolone
140 vermeidbare Todesfälle und 40.000 zusätzliche Nebenwirkungen gingen 2018 auf das Konto einer unkritischen ärztlichen Verordnung von Fluorchinolen. Das findet das Wissenschaftliche Institut der ... » Weiterlesen

Detaillierter Bericht der EMA zu Sartanen veröffentlicht
Im Sommer 2018 hatten weltweite Rückrufe des Blutdrucksenkers Valsartan aufgrund von Nitrosamin-Verunreinigungen für Aufsehen gesorgt. Am 1. Februar 2019 hatte die europäische Arzneimittelbehörde ... » Weiterlesen

Neue Sartan-Monographie kommt
dm/ral | Zum 1. Juli 2019 sollen in der Ausgabe 10.0 des Europäischen Arzneibuchs (Ph. Eur.) geänderte Sartan-Monographien veröffentlicht werden. Damit reagiert das Bundesinstituta für ... » Weiterlesen

Nach „Valsartan-Skandal“: neue Sartan-Monographie ab 1. Juli
Der Fall um die mit Nitrosaminen verunreinigten Blutdrucksenker der Wirkstoffklasse der Sartane ist noch immer nicht gänzlich abgeschlossen, auch wenn es seit dem 11. April 2019 die ersten rechtlich ... » Weiterlesen

Nicht nur Sartane: Antidiabetikum mit NDMA verunreinigt
„Update zu Nitrosamin-Verunreinigungen“: Die EMA arbeitet weiterhin daran, Verunreinigungen in Arzneimitteln vorzubeugen, heißt es in einer Pressemitteilung der EU-Arzneimittelbehörde vom ... » Weiterlesen
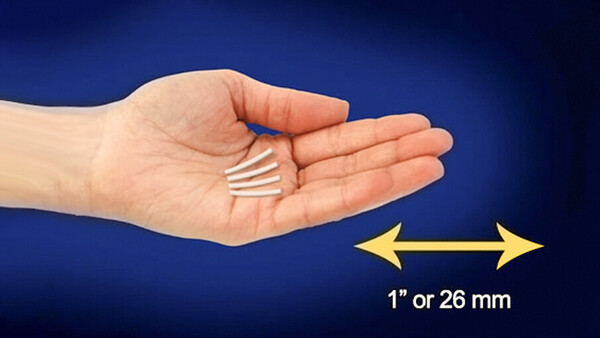
Opioid-Sucht: EU-Zulassungsempfehlung für Buprenorphin-Implantat
Für stabil eingestellte Opioidabhängige könnte sich die Substitutionsbehandlung demnächst vereinfachen: Der EMA-Ausschuss für Humanarzneimittel hat die Zulassung des Buprenorphin-Implantats Sixmo... » Weiterlesen

Anwendung in der Schwangerschaft: BfArM setzt Anpassungen bei Metamizol um
Im Dezember hatte der Humanarzneimittelausschuss CHMP die Ergebnisse eines Reviews zu novaminsulfonhaltigen Arzneimitteln veröffentlicht. Unter anderem sollen die Empfehlungen zur Anwendung in ... » Weiterlesen
Orales Add-on bei Typ-1-Diabetes: Überwiegt der Nutzen das Risiko?
Anfang März hat die europäische Arzneimittelbehörde EMA eine Zulassungsempfehlung für den SGLT-Inhibitor Sotagliflozin ausgesprochen. Unter dem Markennamen Zynquista® soll das Gliflozin als Ergä... » Weiterlesen

EMA erteilt Omega-3-Fettsäuren erneute Absage
Arzneimittel, die Omega-3-Fettsäuren enthalten, verhindern keine weiteren Herzerkrankungen nach einem Herzinfarkt. Betroffene Arzneimittel sollen nicht mehr in der Sekundärprävention eingesetzt ... » Weiterlesen

CGRP-Antikörper: Revolution bei Migräne?
Berechtigte Hoffnung oder ungerechtfertigter Hype: Welchen Nutzen bringen die innovativen CGRP-Antikörper Galcanezumab, Fremanezumab und der CGRP-Rezeptor-Antikörper Erenumab für Migränepatienten... » Weiterlesen
Roches Rituximab erhält EU-Zulassung bei Pemphigus Vulgaris
Die Europäische Kommission hat Mabthera® bei Pemphigus Vulgaris zugelassen. Roches Biologikum Rituximab erhält damit auch in der EU eine Zulassungserweiterung für die seltene, blasenbildende und ... » Weiterlesen

Risankizumab bei Plaque-Psoriasis
Für mittelschwere bis schwere Plaque-Psoriasis könnte bald ein neues Arzneimittel die Therapie erwachsener Schuppenflechtepatienten erweitern. Der CHMP, der Humanarzneimittelausschus der EMA, hat im... » Weiterlesen

Grünes Licht für Andexanet alfa
cst | Die Therapie mit Faktor-Xa-Inhibitoren könnte bald sicherer werden: Das Antidot Andexanet alfa wurde vom Ausschuss für Humanarzneimittel (CHMP) der europäischen Arzneimittelagentur (EMA) ... » Weiterlesen

Neurodermitis-Antikörper: Bald auch bei schwerem Asthma?
2017 wurde das erste zielgerichtete Biologikum gegen Neurodermitis zugelassen: Dupilumab. Nun hat der Humanarzneimittelausschuss der EMA für den vollhumanen Antikörper eine Indikationserweiterung ... » Weiterlesen
Zanamivir demnächst auch intravenös gegen Grippe
Der Humanarzneimittelausschuss der EMA, der CHMP, hat ein neues Arzneimittel gegen Grippe zur Zulassung empfohlen – Dectova®. Es wird als Infusion verabreicht und enthält mit dem Neuramidase-... » Weiterlesen

Das erste Antidot für Apixaban und Rivaroxaban kommt nach Europa
Orale Antikoagulanzien werden immer beliebter, ihre möglichst sichere Anwendung wird damit nicht weniger wichtig: Wenn auch nicht der einzige Aspekt, der im Mittelpunkt der fachlichen ... » Weiterlesen

Galcanezumab kommt auf den Markt
Zugelassen ist Galcanezumab in der EU bereits seit November 2018, nun bringt Lilly Emgality® zum 1. April 2019 auf den Markt. Nach Erenumab (Aimovig®) ist Galcanezumab der zweite Antikörper zur ... » Weiterlesen

Licht und Schatten von Dapagliflozin
Mit Dapagliflozin könnte das erste orale Antidiabetikum zur Add-on-Therapie bei Diabetes mellitus Typ 1 zugelassen werden. Die entsprechende Empfehlung des Ausschusses für Humanarzneimittel (CHMP) ... » Weiterlesen

Nitrosamin-Entstehung ausschließen!
du | Folgt die EU-Kommission den Empfehlungen des Ausschusses für Humanarzneimittel (CHMP) der EMA, müssen Hersteller von Tetrazolring-haltigen Sartanen ihre Herstellungsprozesse in Zukunft so ... » Weiterlesen

Dapagliflozin für Typ-1-Diabetiker
jb | Der Humanarzneimittelausschuss der EMA (CHMP) hat empfohlen, die Zulassung des SGLT-2-Hemmers Dapagliflozin zu erweitern. Er soll künftig auch bei bestimmten Patienten mit Typ-1-Diabetes zusä... » Weiterlesen




















Foto: dpa