
Thema
Committee for Medicinal Products for Human Use
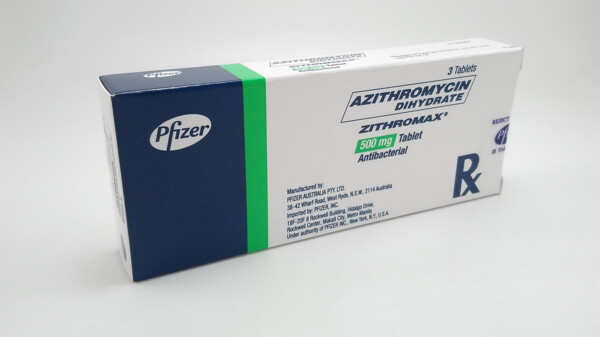
Azithromycin – überwiegt der Nutzen noch die Risiken?
Azithromycin wird häufig bei Infektionen der oberen Atemwege verordnet und stellt in vielen Fällen eine therapeutische Alternative zu Penicillinen dar. Aufgrund zunehmender Antibiotika-Resistenzen ... » Weiterlesen
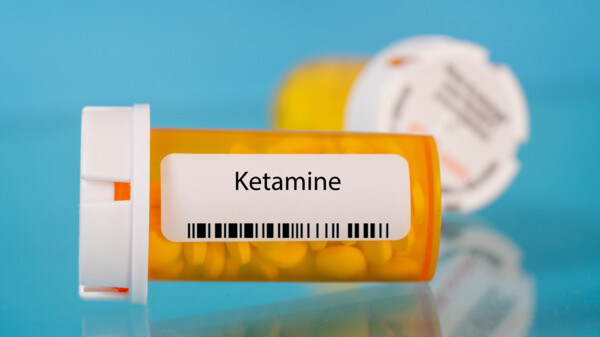
FDA: Keine Ketamin-Nasensprays für die häusliche Anwendung herstellen!
„Wundermittel Ketamin?“ – solche Schlagzeilen waren nicht nur in der DAZ in den vergangenen Jahren immer wieder zu lesen. Kein Wunder also, dass auch potenzielle Patient:innen mit Depressionen ... » Weiterlesen

Comirnaty Omicron XBB.1.5 – wann kommen die Kinderimpfstoffe?
Ab kommendem Montag, den 18. September, wird die erste Teilmenge des an die aktuell kursierenden Omikron-Subvarianten angepassten COVID-19-Impfstoffes von Biontech/Pfizer ausgeliefert. Dies gilt ... » Weiterlesen
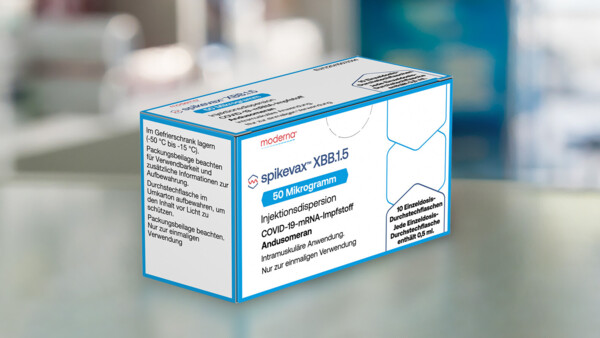
An XBB.1.5 angepasste COVID-19-Vakzine von Moderna in der EU zugelassen
Nachdem der an die SARS-CoV-2-Subvariante XBB.1.5 angepasste Impfstoff von Biontech/Pfizer bereits vor zwei Wochen die europäische Zulassung erhalten hatte, zieht Moderna nach. Auch Spikevax XBB.1.5 ... » Weiterlesen
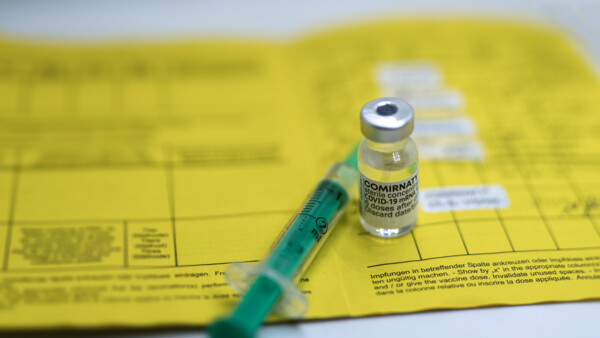
Comirnaty Omikron XBB.1.5 erhält europäische Zulassung
Der an aktuell kursierende Varianten von SARS-CoV-2 angepasste Impfstoff aus dem Hause Biontech und Pfizer wurde am 1. September 2023 in Europa zugelassen. Apotheken sollen den Impfstoff bis zum 12. ... » Weiterlesen
CHMP empfiehlt Zulassung eines an XBB.1.5 angepassten COVID-19-Impfstoffs
Nach Comirnaty, Comirnaty Original/Omicron BA.1 und Comirnaty Original/Omicron BA.4-5 haben Biontech und Pfizer nochmal nachgelegt. Ihrem neuen, an derzeit kursierende ... » Weiterlesen

Zulassungsempfehlung für neue Langzeit-PrEP
Mit sechs Injektionen pro Jahr könnte bald eine neue HIV-Präexpositionsprophylaxe (PrEP) die bisherige (orale) PrEP vereinfachen. Denn für den HIV-Integrase-Inhibitor Cabotegravir in einer ... » Weiterlesen

EMA empfiehlt neue Behandlungsoption beim kreisrunden Haarausfall zur Zulassung
Ganze 14 Arzneimittel hat der Ausschuss für Humanarzneimittel der Europäischen Arzneimittelagentur im Juli zur Zulassung empfohlen. Darunter ist auch ein Inhibitor der Januskinase 3 zur Behandlung ... » Weiterlesen

Tysabri bekommt Konkurrenz
jb/dpa-AFX | Der Ausschuss für Humanarzneimittel der Europäischen Arzneimittel-Agentur hat den Zulassungsantrag für ein Natalizumab-Biosimilar positiv bewertet » Weiterlesen

Wirkstoff Gefapixant gegen chronischen Husten zur Zulassung empfohlen
Im Juli empfahl der Ausschuss für Humanarzneimittel der EMA gleich 14 neue Arzneimittel zur Zulassung – darunter auch den Wirkstoff Gefapixant (Lyfnua) in der Indikation refraktärer oder ... » Weiterlesen

Natalizumab-Biosimilar zur Zulassung empfohlen
Das MS-Arzneimittel Tysabri (Natalizumab) bekommt wohl demnächst Biosimilar-Konkurrenz. Der Ausschuss für Humanarzneimittel (CHMP) der Europäischen Arzneimittel-Agentur (EMA) hat ein entsprechendes... » Weiterlesen

Wenn endogene Antikörper die Biologika-Therapie stören
Mittlerweile sind in Deutschland laut Verband der forschenden Industrie-Unternehmen vfa (Stand: April 2023) 323 gentechnisch hergestellte Wirkstoffe in 364 Biopharmazeutika zugelassen. Diese ... » Weiterlesen
Zulassungsempfehlung für Ublituximab bei Multipler Sklerose
Der Ausschuss für Humanarzneimittel der Europäischen Arzneimittelbehörde EMA empfiehlt die Zulassung von Briumvi (Wirkstoff Ublituximab) für die Therapie der schubförmigen Multiplen Sklerose. Die... » Weiterlesen

Neuer Antikörper bei Colitis ulcerosa kurz vor Zulassung
Mit Mirikizumab hat das CHMP erstmals die Zulassung eines ausschließlichen Interleukin (IL)-23-Inhibitors für die Therapie der chronisch-entzündlichen Darmerkrankung Colitis ulcerosa auf ... » Weiterlesen
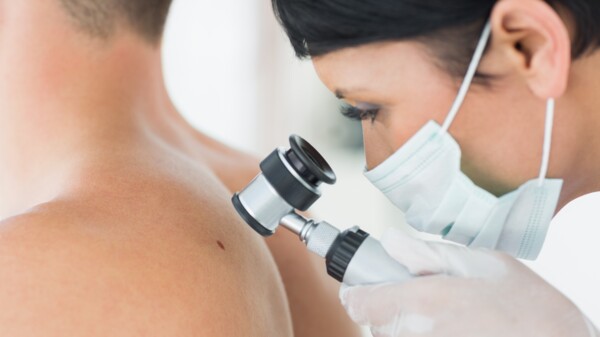
Wenn es JAK-Inhibitoren sein müssen, Haut regelmäßig kontrollieren!
Im Februar 2022 hatte die Europäische Arzneimittel-Agentur EMA mit der Sicherheitsüberprüfung von Januskinase-Inhibitoren zur Behandlung von Entzündungskrankheiten begonnen. Bereits Ende 2022 war ... » Weiterlesen

Schattendasein der SARS-CoV-2-Antikörper
Es hätte eine Erfolgsstory werden können: Der Einsatz neutralisierender monoklonaler Antikörper zur Prophylaxe und Therapie von COVID-19. Auch wenn Infektionskrankheiten nicht gerade zu den ... » Weiterlesen






















Foto: dpa