
Thema
Committee for Medicinal Products for Human Use
Anakinra nun auch bei COVID-19
Anakinra kennen Apotheker aus der Behandlung der rheumatoiden Arthritis, nun darf es auch bei Corona angewendet werden. Wie hilft der Interleukin-1-Rezeptorblocker bei COVID-19 » Weiterlesen

Drittes Corona-Antikörperpräparat für die EU
Sotrovimab ist zugelassen. Der SARS-CoV-2-Antikörper darf zur Behandlung von COVID-19 eingesetzt werden. Wirkt er auch gegen Omikron » Weiterlesen
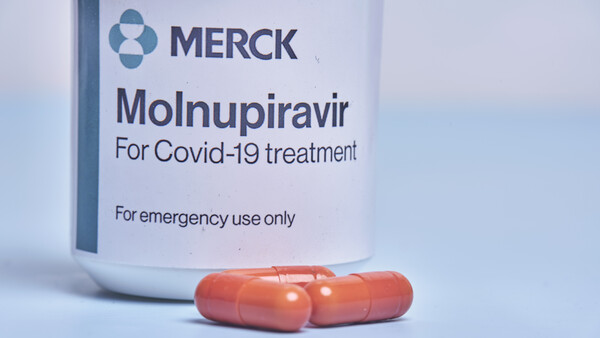
EMA prüft neue Daten zu Molnupiravir
Molnupiravir wirkt schlechter als gedacht, das COVID-19-Arzneimittel verringert Krankenhauseinweisung und Tod statt zu 50 Prozent nur zu 30 Prozent. Grund genug, dass sich auch die EMA vor Zulassung ... » Weiterlesen

Corona-Ticker
mab/cel | Nach und nach drängen neue Therapieoptionen und Impfstoffkandidaten auf den europäischen Markt. Einige wie der Totimpfstoff von Valneva befinden sich noch in einem beschleunigten ... » Weiterlesen
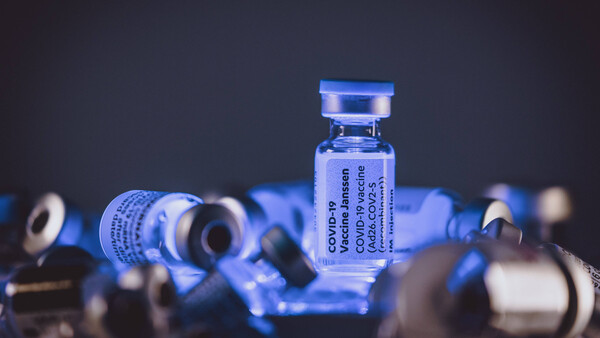
EMA: Zweite Dosis mit COVID-19-Impfstoff Janssen möglich
Wer einmal mit dem COVID-19-Imfpstoff Janssen geimpft ist, sollte sich mindestens zwei Monate danach mit einer zweiten Impfdosis des Vektorimpfstoffs impfen lassen. Das rät die EMA. Doch auch andere ... » Weiterlesen

Tocilizumab ist nun auch in der EU gegen COVID-19 zugelassen
Am Ende ging es jetzt doch schnell: Gestern erst empfahl der Ausschuss für Humanarzneimittel CHMP der europäischen Arzneimittelbehörde EMA, den Interleukin-6-Antagonisten Tocilizumab in Roactemra ... » Weiterlesen

Wirksam ja – aber sicher?
Die Europäische Arzneimittel-Agentur hat die Zulassung des COVID-19-Impfstoffs von Biontech/Pfizer für Fünf- bis Elfjährige empfohlen. Studiendaten zeigen eine vergleichbare Immunogenität wie ... » Weiterlesen

Kinder warten auf Impfung
cha | Angesichts der hohen Inzidenzen auch bei Kindern wird die COVID-19-Impfung für ihre Sprösslinge von zahlreichen Eltern herbeigesehnt. Ein erster Schritt ist die am vergangenen Donnerstag ... » Weiterlesen
EMA empfiehlt COVID-19-Impfung mit Comirnaty ab 5 Jahren
Wie angekündigt, hat sich heute der Humanarzneimittelausschuss CHMP der EMA für die Erweiterung der Zulassung des COVID-19-Impfstoffs von Biontech/Pfizer ausgesprochen. Damit empfiehlt die EMA, auch... » Weiterlesen
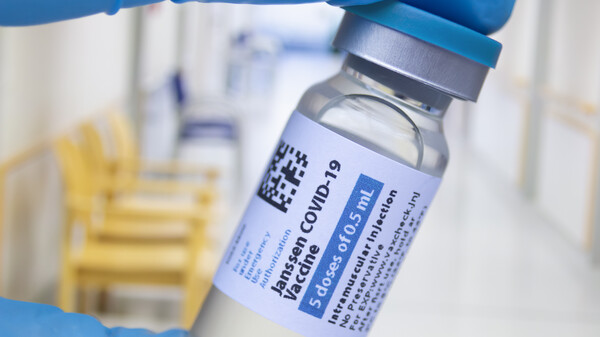
EMA prüft Daten zur Auffrischungsdosis mit COVID-19-Impfstoff Janssen
Die Zulassung der „COVID-19 Vaccine Janssen“ erlaubt derzeit für die Grundimmunisierung eine einmalige Impfstoffdosis. Allerdings empfiehlt die STIKO mittlerweile eine Optimierung des ... » Weiterlesen
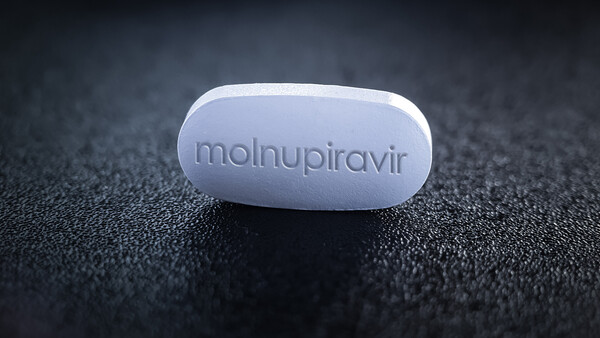
Wie kann Molnupiravir bei COVID-19 angewendet werden?
Noch während des laufenden Rolling-Review-Verfahrens zu Molnupiravir in Lagevrio hat sich die EMA zur Anwendung des oralen COVID-19-Arzneimittels vor Zulassung in der EU geäußert. Welche COVID-19-... » Weiterlesen

Grünes Licht für zwei Antikörperpräparate
cel | Am 11. November 2021 hatte der Ausschuss für Humanarzneimittel der EMA, das CHMP, gleich zwei SARS-CoV-2-Antikörperpräparate zur Zulassung empfohlen: Casirivimab / Imdevimab in Ronapreve ... » Weiterlesen
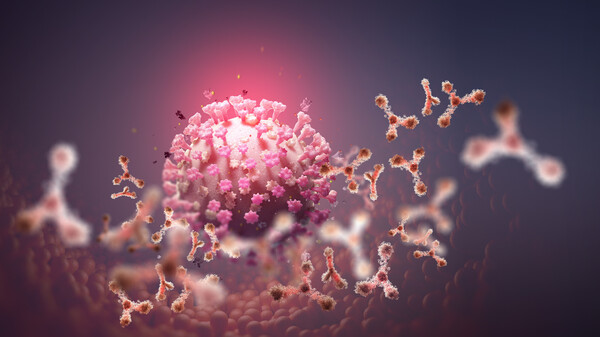
Corona-Antikörper – wo stehen wir?
Die Namen muten durchaus kompliziert an. Unübersichtlich wird es auch schnell, welcher der SARS-CoV-2-Antikörper in welchem Stadium des EMA-Zulassungsprozesses ist und welcher zur Behandlung von ... » Weiterlesen
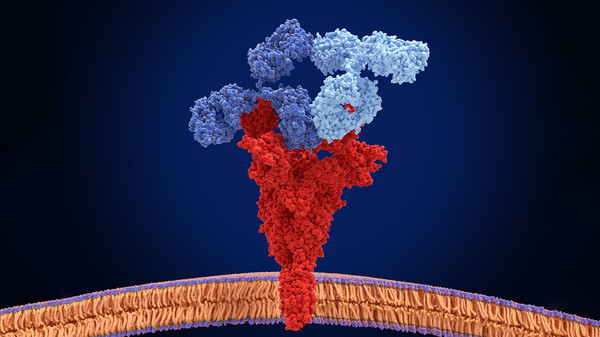
EMA-Zulassungsempfehlung für Casirivimab/Imdevimab und Regdanvimab
Gleich zwei SARS-CoV-2-Antikörperpräparate hat das CHMP der EMA zur Zulassung empfohlen – es geht um Casirivimab/Imdevimab in Ronapreve von Roche und Regdanvimab in Regkirona von Celltrion. ... » Weiterlesen

Corona-Antikörper – wo stehen wir?
cel | Sowohl im Rolling-Review- als auch im normalen Zulassungsverfahren befinden sich Antikörper, die zur Prophylaxe und/oder Therapie von COVID-19 entwickelt wurden. Der Antrag für Bamlanivimab ... » Weiterlesen

Sildenafil bald auch in Deutschland ohne Rezept?
In manchen Ländern gibt es Sildenafil bereits ohne Rezept. Nun steht „Sildenafil 50mg“ auf der Tagesordnung des Sachverständigen-Ausschusses für Verschreibungspflicht in Deutschland – am 25. ... » Weiterlesen
EMA beendet Rolling-Review für Bamlanivimab und Etesevimab
In absehbarer Zeit wird Eli Lilly die EU-Zulassung für seine SARS-CoV-2-Antikörper Bamlanivimab und Etesevimab nicht erhalten. Die EMA hat das Rolling-Review-Verfahren zu Bamlanivimab und Etesevimab... » Weiterlesen
EMA rät zum Moderna-Booster
Nachdem das CHMP der EMA bereits Booster-Dosen mit Comirnaty empfohlen hat, spricht der Ausschuss nun auch eine Zulassungsempfehlung für Auffrischimpfungen mit Spikevax von Moderna aus. Beide mRNA-... » Weiterlesen

Corona-Ticker
ck/du | Biontech treibt die Forschung rund um seinen Impfstoff Comirnaty® weiter voran, ein Antrag auf Zulassung für Kinder wurde eingereicht, eine vom CHMP positiv bewertete neue Formulierung ... » Weiterlesen
Comirnaty wird einfacher in der Handhabung
Mit dem neuen Jahr 2022 kommt eine neue Formulierung des Pfizer/Biontech-Impfstoffes – Comirnaty muss sodann vor Verabreichung nicht mehr verdünnt werden und ist länger im Kühlschrank lagerfähig... » Weiterlesen

EMA empfiehlt Dritt- und Booster-Impfungen
Immungeschwächte sollten als Grundimmunisierung gegen COVID-19 drei Impfdosen einer mRNA-Vakzine erhalten. Dabei wird die dritte Dosis 28 Tage nach der zweiten verabreicht. Allgemeine ... » Weiterlesen
EMA prüft Moderna-Auffrischimpfung
Moderna will, dass Spikevax auch für eine Auffrischimpfung explizit zugelassen wird – nun hat die EMA mit der Prüfung des Zulassungsantrags für den Booster begonnen » Weiterlesen






















Foto: dpa