
Thema
Zulassungsbehörde

Locabiosol ab 28. Mai nicht mehr verkehrsfähig
Das Bundesinstitut für Arzneimittel und Medizinprodukte beabsichtigt, die Zulassung für Locabiosol (Fusafungin) zum 28. Mai 2016 zu widerrufen. Fusafungin-haltigen Präparaten war ein negatives ... » Weiterlesen

Ein Antidiabetikum zum Abnehmen
Seit Anfang April steht mit Saxenda® in Deutschland ein zusätzliches Arzneimittel zur Behandlung der Adipositas zur Verfügung. Die Indikationserweiterung des ursprünglich als Antidiabetikum ... » Weiterlesen

Elektrische Wechselfelder gegen Krebs
Eine Erhaltungstherapie mit dem Zytostatikum Temozolomid begleitet von der kontinuierlichen Applikation elektrischer Wechselfelder kann die Lebenserwartung von Glioblastom-Patienten erhöhen – ein... » Weiterlesen

Jenseits der Zulassung
Patienten mit lebensbedrohlichen Erkrankungen klammern sich an jeden Strohhalm. Bei Internet-Recherchen stoßen sie oft auf Wirkstoffe, die sich noch in der klinischen Erprobung befinden. Je nach ... » Weiterlesen

Nichts gewonnen
Unregelmäßige Regelblutungen, Hitzewallungen – angesichts dieser Symptome stellen sich Frauen ab Mitte 40 oft die Frage, ob sie vielleicht schon in den Wechseljahren sind. Selbsttests, die in ... » Weiterlesen
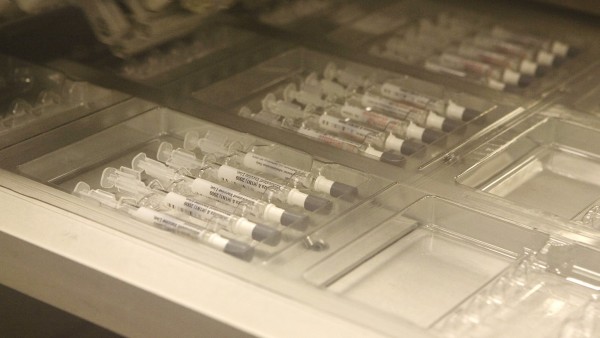
Zulassung für nasalen Vogelgrippe-Pandemie-Impfstoff empfohlen
Der Humanarzneimittelausschuss der EMA (CHMP) hat sich dafür ausgesprochen, einen nasalen Pandemieimpfstoff gegen H5N1-verursachte Influenza zuzulassen. Dieser soll im Pandemiefall bei Kindern und ... » Weiterlesen

Positives Votum für Gentherapie gegen seltenen Immundefekt
Mit der Zulassungs-Empfehlung für Strimvelis hat sich der Humanarzneimittelausschuss der EMA (CHMP) für einen gentherapeutischen Ansatz ausgesprochen. Er soll Kindern mit dem angeborenen seltenen ... » Weiterlesen

Beschleunigte Zulassungen müssen Ausnahmen bleiben
Um Risiken für Patienten zu begrenzen, fordert GKV-Vize Johann-Magnus von Stackelberg verschärfte Standards für schnelle Zulassungen – und erinnert an den Contergan-Skandal. Da die Industrie kaum... » Weiterlesen

Symbioflor 2 auf dem Prüfstand
Die Wirksamkeit des Escherichia-coli-Präparats Symbioflor 2 bei Reizdarm ist möglicherweise nicht ausreichend belegt. Die europäische Aufsichtsbehörde EMA hat daher auf Initiative des ... » Weiterlesen

Forscher entwickeln Pharmafabrik in Schrankgröße
Das Gerät hat die Größe eines Kühlschranks und produziert verschiedene Arzneimittel – wesentlich schneller als herkömmliche Verfahren. Der Apparat könne bei Epidemien oder nach Katastrophen ... » Weiterlesen
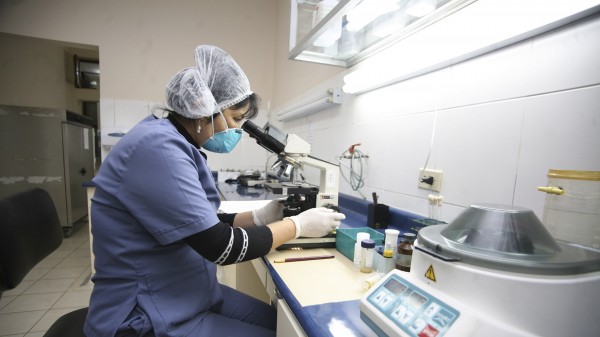
FDA erlaubt Einsatz eines Roche-Tests zur Prüfung von Blutspenden
Um Blutspenden auf das möglicherweise darin enthaltene Zika-Virus zu untersuchen, rät die US-Gesundheitsbehörde FDA jetzt zum Einsatz eines Tests des Unternehmens Molecular Systems. Der Test soll ... » Weiterlesen

So wird die Pharmakotherapie ein Kinderspiel
rr | Auf dem Pädiatrie-Symposium des consilium Offizin, einem Service der Pädia GmbH, ging es am Samstagvormittag um die orale Antibiotika-Gabe bei Kindern und um Besonderheiten bei pädiatrischen ... » Weiterlesen

Große Studien-Beratungsfirmen schließen sich zusammen
Die amerikanische PharmApprove berät Pharmahersteller bei FDA-Anträgen, die schwedische NDA Group insbesondere bei europäischen Zulassungen. Durch ihren Zusammenschluss wollen sie zur weltweit fü... » Weiterlesen

Bereits Kurzzeitanwendung erhöht Risiko für Eierstockkrebs
Bislang ging man davon aus, dass durch eine Hormonersatztherapie das Risiko für ein Ovarialkarzinom erst bei Langzeitanwendung geringfügig steigt. Neuen Daten zufolge ist das aber schon in den ... » Weiterlesen

Erhöhen Neuroleptika bei Parkinson die Mortalität?
Neuroleptika scheinen bei Demenzpatienten die Mortalität zu erhöhen. Ob das bei Parkinsonpatienten, die oft mit Antipsychotika behandelt werden, auch der Fall ist, wollten Forscher in einer große ... » Weiterlesen
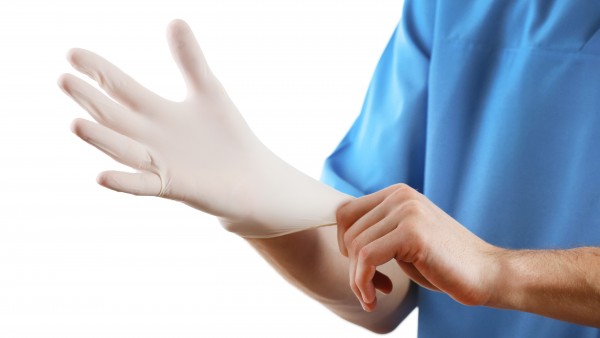
FDA will gepuderte Handschuhe verbieten
Die amerikanische Zulassungsbehörde FDA möchte gepuderte Untersuchungs- und OP-Handschuhe verbieten. Die Handschuhe, die vereinzelt auch in Apotheken genutzt werden, stellten ein erhebliches und ... » Weiterlesen
Experten fordern Konsequenzen aus tödlichem Zwischenfall in Rennes
Die teils tödlichen Nebenwirkungen bei der Phase-1-Studie in Rennes zeigen die Grenzen in Genehmigungsverfahren klinischer Studien auf, schreiben Pharmakologen aus Großbritannien und den ... » Weiterlesen
Schulungsmaterialien zu kombinierten oralen Kontrazeptiva
Das BfArM stellt auf seiner Homepage ergänzende Unterlagen zur sicheren Arzneimittelanwendung für Ärzte und Patienten bereit. Seit kurzem sind auch harmonisierte, Wirkstoff-bezogene ... » Weiterlesen
Mit Arzneimitteln zum Wunschgewicht?
Von André Said | „Appetitzügler“, „Fettblocker“ oder „Schlankheitspillen“ – Die Auswahl an vermeintlichen Mitteln zur Gewichtsreduktion ist breit und unübersichtlich. Proklamiert ... » Weiterlesen


















Foto: Imago