
- DAZ.online
- DAZ / AZ
- DAZ 40/2008
- Rückruf aller Chargen ...
DAZ aktuell
Rückruf aller Chargen von Ionsys®
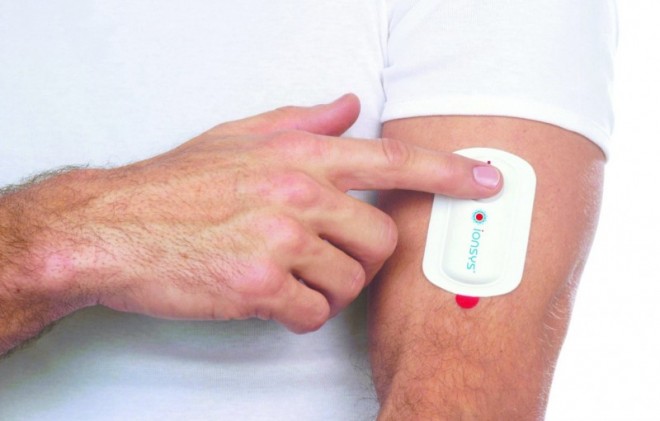
Diese Maßnahme erfolgt in enger Abstimmung mit den europäischen Arzneimittelbehörden einschließlich des Bundesinstituts für Arzneimittel und Medizinprodukte in den folgenden Ländern: Österreich, Belgien, Finnland, Frankreich, Deutschland, Luxemburg, Niederlande, Slowenien, Schweden, Großbritannien, Irland, Singapur, Dänemark, Norwegen. Adressat dieses Schreibens sind alle Kliniken und krankenhausversorgenden Apotheken, die Ionsys® erhalten haben. Das vom Patienten selbst zu aktivierende Applikationssystem, bei dem die Freisetzung von Fentanyl aus dem transdermalen System auf dem Prinzip der Iontophorese beruht, ist zugelassen für die Behandlung von erwachsenen Patienten mit akuten mäßigen bis starken postoperativen Schmerzen ausschließlich in einem Krankenhaus. Es wird seit dem 15. Januar 2008 auf dem Markt angeboten.
Selbstaktivierung nicht ausgeschlossen
Bei einigen Systemen einer einzelnen Charge sind Defekte entdeckt worden, so dass nicht ausgeschlossen werden kann, dass sich das System selbst aktivieren könnte. Derzeit liegen Janssen-Cilag keine Hinweise vor, dass Patienten wegen dieses Defekts zu Schaden gekommen sind. Eine Untersuchung zur Feststellung der Ursache dauert derzeit an. Alle Krankenhäuser, in denen Ionsys® angewendet wird, wurden aufgefordert, ihre Bestände zu prüfen und gegebenenfalls zurückzusenden. Das Applikationssystem sollte bei allen Patienten, die zur Zeit Ionsys® benutzen, umgehend entfernt werden und diese Patienten müssen mit einer angemessenen alternativen Schmerzmedikation zur Behandlung ihrer akuten mäßigen bis schweren post-operativen Schmerzen versorgt und entsprechend überwacht werden.
QuelleRote-Hand-Brief der Janssen-Cilag GmbH vom 28. September 2008.
ck





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.