
- DAZ.online
- DAZ / AZ
- DAZ 29/2009
- Neues humanes GLP-1-...
Arzneimittel und Therapie
Neues humanes GLP-1-Analogon Liraglutid
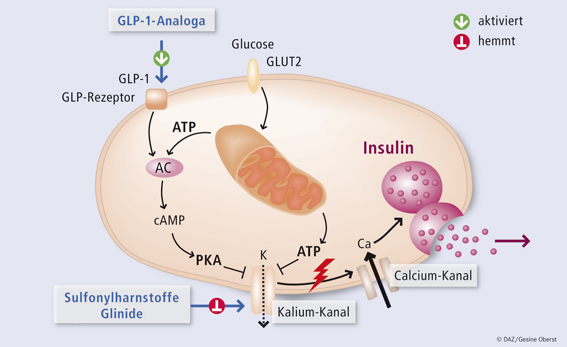
Bei Liraglutid handelt es sich um das erste, einmal täglich anzuwendende humane Glucagon-like-Peptid(GLP-1)-Analogon. Der Wirkstoff, der unter dem Markennamen Victoza® in den Handel kommt, weist eine 97%ige Homologie zum natürlichen GLP-1 auf, welches auf einen Nahrungsreiz hin im Gastrointestinaltrakt gebildet wird und glucoseabhängig die Insulinbildung und Insulinfreisetzung stimuliert (Abb.). Gleichzeitig bewirkt das GLP-1 Analogon eine Hemmung der Glucagonfreisetzung. Allerdings beeinträchtigt Liraglutid nicht die Gegenregulation bei einer Hypoglykämie, bei niedrigen Blutglucosespiegeln wird die Unterdrückung der Glucagonsekretion aufgehoben und die Insulinsekretion somit nicht vermehrt. Damit ist das Hypoglykämierisiko unter der Therapie sehr viel geringer als beispielsweise unter Insulin oder anderen, die Insulinsekretion stimulierenden oralen Antidiabetika.
Das belegen die klinischen Studien, die dem GLP-1-Analogon zudem eine gute klinische Wirksamkeit bescheinigen. Die neue Substanz wurde in sechs Einzelstudien, den so genannten LEAD-Studien (Liraglutid Effect and Action in Diabetes), bei insgesamt mehr als 4200 Patienten in unterschiedlichen Therapieregimen getestet. Der Wirkstoff führte dabei zu einer signifikanten Reduktion des HbA1c -Wertes in der Mono- wie auch der Kombinationstherapie. Es resultierte gleichzeitig eine Reduktion der Nüchternblutzuckerwerte wie auch der postprandialen Hyperglykämie.
Parallel dazu wurde in den Studien eine dosisabhängige Reduktion des Körpergewichtes der Patienten registriert und ein signifikanter Rückgang des systolischen Blutdrucks um 4 bis 6 mmHg.
Die Verträglichkeit des neuen Wirkstoffs erwies sich als gut. Es können gastrointestinale Nebenwirkungen auftreten, die jedoch im Allgemeinen vorübergehender Natur sind und innerhalb von vier Wochen abklingen.
Günstiger Einfluss auf die Betazellen
Unter der Behandlung mit dem neuen Antidiabetikum ist neben der guten Blutzuckerkontrolle auch ein günstiger Einfluss auf die insulinproduzierenden Betazellen des Pankreas zu erwarten. Denn in tierexperimentellen Untersuchungen wurden eine Steigerung der Betazellproliferation und eine Zunahme der Betazellmasse gesehen. Vergleichbare Daten gibt es beim Menschen nicht, allerdings weisen Surrogatparameter auf eine Besserung der Betazellfunktion unter Liraglutid hin.
Dessen Halbwertszeit liegt nach subkutaner Injektion bei 11 bis 15 Stunden, wobei durch eine Stabilisierung des Moleküls über eine C16-Fettsäure eine zuverlässige 24-Stunden-Wirkung erzielt wird. Das ermöglicht die nur einmal tägliche Applikation und damit eine deutliche Vereinfachung des Therapieregimes, zumal Liraglutid in einer Standarddosierung verabreicht wird und aufwändige, die Patienten häufig belastende Blutzuckerkontrollen nicht erforderlich sind.
Zugelassen ist Liraglutid für die Kombinationstherapie mit Metformin oder einem Sulfonylharnstoff oder mit Metformin plus einem Sulfonylharnstoff oder Glitazon, wenn die bisherige Behandlung nicht zu einer ausreichenden Blutzuckerkontrolle geführt hat. <
Quelle
Prof. Dr. Michael Nauck, Bad Lauterberg; Prof. Dr. Baptist Gallwitz, Tübingen; Lotte Bjerre Knudsen, Kopenhagen; Prof. Dr. Mads Krogsgaard Thomsen, Kopenhagen: Einführungspressekonferenz "Humanes-GLP-1 Analogon Liraglutid – Diabetestherapie mit System", Frankfurt, 18. Juni 2009, veranstaltet von der Novo Nordisk Pharma GmbH, Mainz.
Christine Vetter, freie Medizinjournalistin
|
Steckbrief: Liraglutid
Handelsname:
Victoza
Hersteller:
Novo Nordisk
Einführungsdatum:
1. Juli 2009
Packungsgrößen, Preise und PZN:
2 Fertigpens: 124,66 Euro, PZN 3277630; 5 Fertigpens, 221,33 Euro, PZN 3277653.
Zusammensetzung:
1 ml Lösung enthält 6 mg Liraglutid. 1 Fertigpen enthält 18 mg Liraglutid in 3 ml. Sonstige Bestandteile: Natriummonohydrogenphosphat-Dihydrat, Propylenglycol, Phenol, Wasser für Injektionszwecke.
Stoffklasse:
Antidiabetika; Inkretinmimetikum. ATC-Code: A10BX07.
Indikation:
Zur Behandlung des Diabetes mellitus Typ 2 bei Erwachsenen, in Kombination mit Metformin oder einem Sulfonylharnstoff bei Patienten mit unzureichender Blutzuckerkontrolle trotz maximal verträglicher Dosis bei Monotherapie mit Metformin oder Sulfonylharnstoff und in Kombination mit Metformin und einem Sulfonylharnstoff oder Metformin und einem Thiazolidindion bei Patienten mit unzureichender Blutzuckerkontrolle trotz Therapie mit zwei oralen Antidiabetika
Dosierung:
Einmal täglich unabhängig von den Mahlzeiten als subkutane Injektion, tägliche Anfangsdosis 0,6 mg, ist nach mindestens einer Woche auf 1,2 mg zu erhöhen, kann nach mindestens einer weiteren Woche auf 1,8 mg erhöht werden. Liraglutid kann zusätzlich zu einer bestehenden Therapie mit Metformin, einem Sulfonylharnstoff oder einer Kombination aus Metformin und Thiazolidindion oder Sulfonylharnstoff gegeben werden.
Gegenanzeigen:
Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile.
Nebenwirkungen:
sehr häufig: Hypoglykämie; Kopfschmerzen; Übelkeit, Durchfall, Erbrechen. Häufig: Nasopharyngitis, Bronchitis; Anorexie, verminderter Appetit; Schwindel; Dyspepsie, Oberbauchschmerzen, Obstipation, Gastritis, Flatulenz, abdominelles Spannungsgefühl, gastroösophageale Refluxkrankheit, abdominale Beschwerden, Zahnschmerzen, virale Gastroenteritis; Erschöpfung, Fieber.
Wechselwirkungen:
Die durch Liraglutid leicht verzögerte Magenentleerung kann die Resorption gleichzeitig oral angewendeter Arzneimittel beeinflussen. Diarrhö, die als unerwünschte Wirkung auftreten kann, kann die Resorption von begleitend oral gegebenen Arzneimitteln beeinträchtigen. Bei Patienten, die mit Warfarin behandelt werden, wird zu Beginn der Liraglutid-Behandlung eine häufigere Überwachung des INR (International Normalized Ratio) empfohlen.
Warnhinweise und Vorsichtsmaßnahmen:
Bei Patienten mit entzündlichen Darmkrankheiten und diabetischer Gastroparese liegen nur begrenzte Erfahrungen vor; folglich wird Liraglutid bei diesen Patienten nicht empfohlen. Die Anwendung anderer GLP-1-Analoga ist mit einem Pankreatitis-Risiko assoziiert, wird eine Pankreatitis vermutet, sind Liraglutid und andere potenziell in Verdacht stehende Arzneimittel abzusetzen. Über unerwünschte Ereignisse in Zusammenhang mit der Schilddrüse wurde in klinischen Studien berichtet, insbesondere bei Patienten mit bestehender Schilddrüsenerkrankung. Patienten, die Liraglutid in Kombination mit einem Sulfonylharnstoff erhalten, können ein erhöhtes Risiko für eine Hypoglykämie haben, dieses Risiko kann durch Reduktion der Sulfonylharnstoff-Dosis gesenkt werden. Patienten sollten Maßnahmen zur Hypoglykämievermeidung bei der Teilnahme am Straßenverkehr oder während des Bedienens von Maschinen ergreifen, besonders bei Anwendung von Liraglutid in Kombination mit einem Sulfonylharnstoff.
|





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.