
- DAZ.online
- DAZ / AZ
- DAZ 18/2013
- BfArM schafft Transparenz
DAZ aktuell
BfArM schafft Transparenz
Die neue Recherchemöglichkeit soll bereits vorhandene behördliche Informationen über Arzneimittelrisiken allerdings nicht ersetzen, sondern flankieren: "Entscheidende Informationsquellen zu Anwendung und Risiken von Arzneimitteln bleiben weiterhin die Gebrauchsinformation (‚Packungsbeilage‘) für Patienten und die Fachinformation für Ärzte", so das BfArM. Denn im Gegensatz zu den jetzt zugänglichen Rohdaten der Verdachtsmeldungen stellten Fach- und Gebrauchsinformationen bereits das Ergebnis einer behördlichen Bewertung dar und böten Ärzten und Patienten konkret anwendbare Informationen und Empfehlungen.
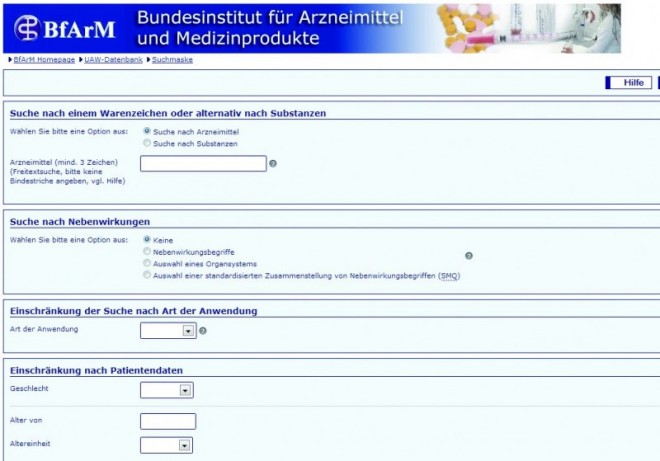
Was ist möglich?
Die UAW-Datenbank, die regelmäßig aktualisiert wird, umfasst alle der Behörde seit 1995 gemeldeten Verdachtsfälle unerwünschter Arzneimittelwirkungen (UAW) aus Deutschland – außer denen aus klinischen Prüfungen und solchen, die in der wissenschaftlichen Literatur publiziert worden sind. Verdachtsfälle sind dabei unerwünschte Ereignisse beim Patienten, die nach der Einnahme von Arzneimitteln eingetreten sind und möglicherweise im Zusammenhang mit dem Arzneimittel stehen. Das BfArM weist jedoch darauf hin, dass dies nicht automatisch bedeute, dass ein ursächlicher Zusammenhang mit dem Arzneimittel auch tatsächlich existiere.
Per Filter können Verdachtsfälle zu einzelnen Nebenwirkungsbegriffen, Wirkstoffen, Zeiträumen und Altersgruppen gesucht werden. Allerdings: "Die Rechercheergebnisse bedürfen einer medizinischen Interpretation und dürfen keinesfalls als Ersatz für eine ärztliche Aufklärung über mögliche Nebenwirkungen eines Arzneimittels betrachtet werden", betont das BfArM. Denn die individuelle Nutzen-Risiko-Bewertung eines Arzneimittels für einen Patienten könne nur im Gespräch mit dem behandelnden Arzt getroffen werden.


















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.