
- DAZ.online
- DAZ / AZ
- DAZ 1-2/2019
- Herz, Haut, Hypophyse
Arzneimittel und Therapie
Herz, Haut, Hypophyse …
Immunvermittelte Nebenwirkungen unter Checkpoint-Inhibitoren erkennen
Immuncheckpoint-Inhibitoren sind monoklonale Antikörper, die zu einer Aktivierung von T-Zellen führen und so eine gegen den Tumor gerichtete Immunantwort erzeugen. Dieses Prinzip hat sich in der Praxis bewährt, und Immunonkologika werden bei zahlreichen Tumorentitäten eingesetzt (s. Tabelle). Sie blockieren CTLA-4 (Cytotoxic T-Lymphocyte-associated antigen-4; Wirkstoff Ipilimumab) sowie die Rezeptoren von PD-1 (Programmed Cell Death-1; Wirkstoffe Nivolumab und Pembrolizumab) oder deren Liganden PD-L1 (Programmed Cell Death Ligand-1; Wirkstoffe Atezolizumab, Avelumab, Durvalumab). Teilweise ist ihre Wirksamkeit lang anhaltend, was sich besonders eindrücklich in den Fünf-Jahres-Überlebensraten beim fortgeschrittenen Melanom zeigt. Dem Nutzen der Immunonkologika stehen aber auch immunvermittelte unerwünschte Wirkungen gegenüber, die sich gegen die Haut, den Gastrointestinaltrakt, Leber, Drüsen und Nerven richten. Die immunvermittelten Nebenwirkungen sind nicht substanzspezifisch und treten mehr oder weniger unter allen Immunonkologika auf. Unter einer Blockade von CTLA-4 zeigen sich immunvermittelte Nebenwirkungen früher und häufiger als unter der Blockade von PD-1/PD-L1 und sind zudem stärker ausgeprägt. Sie sind unter der Therapie mit CTLA‑4-Inhibitoren dosisabhängig, unter der Gabe von PD‑1/PD-L1-Blockern nicht. Immunvermittelte Nebenwirkungen treten am häufigsten innerhalb der ersten zwölf Wochen nach Therapiebeginn auf, können sich aber auch bis zu sechs Monate nach Therapieende manifestieren. Die meisten immunvermittelten Nebenwirkungen treten akut auf und klingen unter einer Therapie mit Steroiden innerhalb von einem bis sieben Tagen ab. Bei geringer Ausprägung wird ein niedrig dosiertes Corticosteroid (Prednison 0,5 mg/kg Körpergewicht/Tag) gegeben, bei schweren Nebenwirkungen sind hoch dosierte Corticosteroide (1 bis 2 mg/kg Körpergewicht/Tag) erforderlich. Je nach Ausprägung der Nebenwirkungen wird die immunonkologische Therapie aus- oder abgesetzt. Infusionsbedingte Nebenwirkungen sind selten.
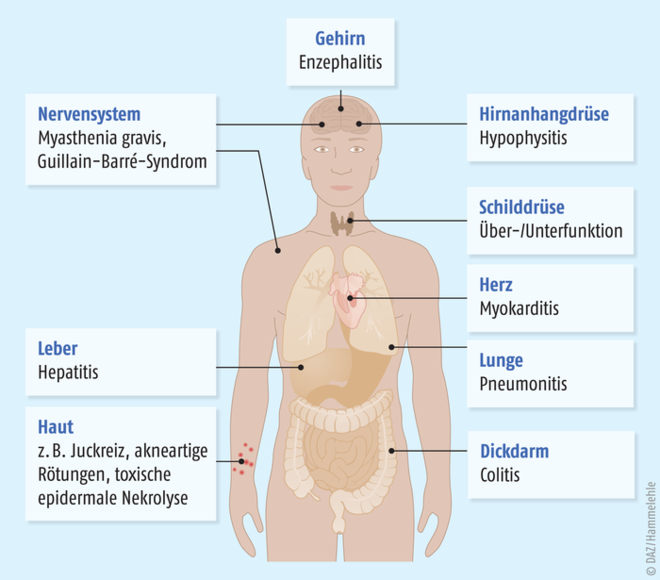
Organspezifische, immun-vermittelte Nebenwirkungen
Colitis: Rund 25% der mit Ipilimumab und weniger als 5% der mit PD-1/PD-L1-Inhibitoren behandelten Patienten erleiden eine Entzündung des Dickdarms, die lebensbedrohlich sein kann. Typische Symptome sind wässrige Durchfälle, abdominelle Beschwerden und gastrointestinale Blutungen. Eine verzögerte Behandlung kann eine schwere Dehydratation oder intestinale Perforation nach sich ziehen. Leicht bis moderat ausgeprägte Formen der Colitis werden mit Loperamid und Flüssigkeitszufuhr therapiert, schwere Formen mit hohen Steroiddosen, bei ungenügendem Therapieansprechen gegebenenfalls mit Infliximab oder Vedolizumab.
Pneumonitis: Die Inzidenz entzündlicher Veränderungen der Lunge liegt im niedrigen einstelligen Bereich, sollte aber als potenziell letale Nebenwirkung bei pulmonalen Symptomen wie trockenem Husten, Hypoxie oder Atemnot frühzeitig abgeklärt und behandelt werden (Gabe hoch dosierter Corticosteroide).
Wirkstoff (Handelsname) |
Indikation |
|---|---|
Atezolizumab (Tecentriq®)
|
Urothelkarzinom, NSCLC |
Avelumab (Bavencio®)
|
Merkelzellkarzinom |
Durvalumab (Imfinzi®)
|
NSCLC |
Ipilimumab (Yervoy®)
|
Melanom |
Nivolumab (Opdivo®)
|
Melanom, NSCLC, Nierenzellkarzinom, klassisches Hodgkin-Lymphom, HNSCC, Urothelkarzinom |
Pembrolizumab (Keytruda®)
|
Melanom, NSCLC, klassisches Hodgkin-Lymphom, HNSCC, Urothelkarzinom |
HNSCC: Plattenepithelkarzinom des Kopf-Hals-Bereichs; NSCLC: nicht-kleinzelliges Lungenkarzinom. | |
Dermatologische Nebenwirkungen: Etwa 30% der mit einem Checkpoint-Inhibitor behandelten Patienten erleiden Hautveränderungen wie Juckreiz, akneartige Rötungen oder eine toxische epidermale Nekrolyse; in einzelnen Fällen wurde ein Stevens-Johnson-Syndrom beschrieben. Zur Therapie werden topische Steroide und Antihistaminika eingesetzt, in schweren Fällen hoch dosierte systemische Corticosteroide.
Endokrine Dysfunktionen: Eine Entzündung der Hirnanhangdrüse (Hypophysitis) tritt bei rund 10% der mit Ipilimumab behandelten Patienten auf, unter anderen Checkpoint-Inhibitoren weitaus seltener. Sie kann sich in Hypotonie, Fatigue und Kopfschmerzen äußern. Zur Linderung werden Hydrocortison oder hoch dosiertes Prednison eingesetzt. Des Weiteren können Schilddrüsenüber- oder -unterfunktionen auftreten.
Hepatitis: Die Inzidenz einer Hepatitis liegt bei 1% der mit PD-1/PD-L1-Inhibitoren und bei 10% der mit Ipilimumab behandelten Patienten. Sie äußert sich in ansteigenden Transaminasen, Gelbsucht, Fatigue, Ödemen und Übelkeit. Sie wird mit hoch dosierten Steroiden behandelt, in refraktären Fällen mit Mycophenolat-mofetil.
Welcher Checkpoint-Inhibitor ist am besten verträglich?
In einer auf 36 direkten Vergleichsstudien mit insgesamt 15.370 Patienten basierenden Netzwerk-Metaanalyse wurde das Sicherheitsprofil einiger Checkpoint-Inhibitoren ermittelt. Im Hinblick auf die allgemeine Sicherheit konnte unter Berücksichtigung aller Nebenwirkungen folgende Rangfolge aufgestellt werden: Am sichersten war Atezolizumab, gefolgt von Nivolumab, Pembrolizumab und Ipilimumab. Schlusslicht war Tremelimumab (monoklonaler Antikörper gegen CTLA-4; wird in Studien untersucht). Ein Vergleich mit konventionellen Chemotherapeutika zeigte unter Checkpoint-Inhibitoren ein vermehrtes Auftreten von Nebenwirkungen an Haut, endokrinem System, Leber und Lunge. Betrachtet man die substanzspezifischen Nebenwirkungen, so traten unter Atezolizumab am häufigsten Hypothyreose, Übelkeit und Erbrechen auf. Unter Pembrolizumab waren es Arthralgien, Pneumonitis und Lebertoxizität, unter Ipilimumab gastrointestinale, renale und Hauttoxizitäten. Die meist nur wenig ausgeprägten Nebenwirkungen unter Nivolumab betrafen vor allem das endokrine System. Bei Patienten mit einem Lungenkarzinom erscheint Nivolumab unter Toxizitätsaspekten als die beste Option.
[Quelle: Xu C et al. Comparative safety of immune checkpoint inhibitors in cancer: systematic review and network meta-analysis. BMJ 2018;363:k4226]
Neurotoxizitäten: Seltene, aber schwerwiegende Neurotoxizitäten wie Myasthenia gravis, Enzephalitis oder ein Guillain-Barré-Syndrom treten bei weniger als 1% der Patienten auf. Myasthenia gravis und das Guillain-Barré-Syndrom müssen rasch therapiert werden (Immunglobuline, hoch dosierte Steroide, intensive Supportivmaßnahmen); eine Enzephalitis erfordert die Gabe hoch dosierter Steroide und bei bakterieller Genese eine antibiotische Therapie.
Myokarditis: Eine Herzmuskelentzündung, die oftmals von entzündlichen Erkrankungen der Skelettmuskulatur begleitet ist, tritt bei weniger als 1% der mit Checkpoint-Inhibitoren therapierten Patienten auf. Mögliche Symptome sind Fatigue, Kurzatmigkeit, Brustschmerzen und erhöhte Troponin-Spiegel. Fulminante Verläufe ereignen sich vor allem im ersten Therapiemonat. Bei Auftreten entsprechender Symptome erfolgen ein kardiales Monitoring und die schnelle Gabe von Steroiden. |
Quelle
Johnson D et al. Immune Checkpoint Inhibitor Toxicity in 2018. JAMA 2018;320(16):1702-1703




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.