
- DAZ.online
- News
- Spektrum
- Was aus den chinesischen ...
Strengere Gesetze?
Was aus den chinesischen Pharmaskandalen des Sommers wurde
Stuttgart - 26.10.2018, 15:15 Uhr
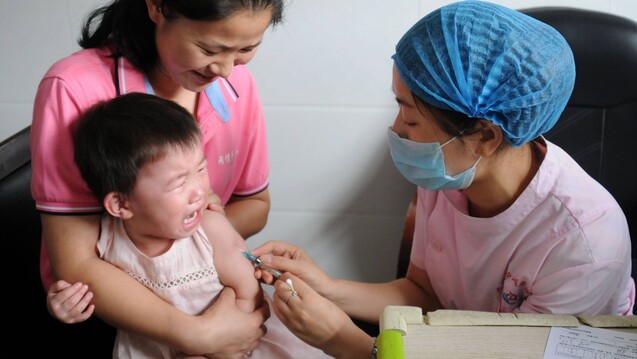
Wirkungslose Tollwutimpfstoffe waren im Sommer 2018 nicht der einzige Pharmaskandal in China. Welche Konsequenzen folgten? (Foto: imago)
Im Schatten des Skandals um die mit Nitrosaminen verunreinigten Sartane konnte man den Eindruck gewinnen, einen Sommer der chinesischen Pharmaskandale erlebt zu haben. Neben direkten Konsequenzen aus den einzelnen Fällen, könnte in China nun ein strengeres Gesetz gegen Arzneimittelfälschungen folgen.
Der letzte Impfstoff-Skandal aus China erfuhr viel mediale Aufmerksamkeit. Der öffentliche Druck für eine schnelle Aufklärung war dementsprechend groß. Die Vorgänge sollen laut der chinesischen Nachrichtenagentur Xinhua am 5. Juli 2018 durch einen nicht näher beschriebenen Hinweis über Manipulationen ans Licht gekommen sein. Der chinesische Impfstoff-Hersteller Changchun Changsheng Life Sciences Limited war daraufhin am 6. und 8. Juli 2018 unangekündigt inspiziert worden. Am 15. Juli gaben die Behörden dann bekannt, dass Changchun Changsheng Life Sciences Tollwut-Impfstoffe auf illegale Weise produziert habe. Nicht nur Unterlagen über Herstellungs- und Inspektionsprozesse seien gefälscht, sondern auch Einstellungen für die Produktion und Ausrüstung willkürlich verändert worden. Noch im Juli sprach die Polizei 18 Haftbefehle aus.
Geldstrafe von 9,1 Milliarden Chinesischen Yuan
Gegen Changchun Changsheng Life Sciences wurde nun eine Geldstrafe von 9,1 Milliarden Chinesischen Yuan (1,15 Milliarden Euro) verhängt. Das meldete die Nachrichtenagentur Xinhua am 16. Oktober. Außerdem seien sowohl die Zulassung für den Tollwutimpfstoff als auch die Zulassungen für verwandte Produkte des Unternehmens aufgehoben worden. Medienberichten zufolge hat Chansheng seinen Aktionären mitgeteilt, dass das Unternehmen dafür angeklagt wurde, 748 Chargen des Tollwutimpfstoffes ab Januar 2014 auf illegale Weise produziert zu haben.
Für Deutschland hatte das Paul-Ehrlich-Institut schon im August Entwarnung gegeben: Das chinesische Unternehmen Changchun Changsheng habe weder eine nationale noch eine EU-weite Zulassung für Impfstoffe. Außerdem habe keiner der Zulassungsinhaber, die Impfstoffe in Deutschland auf den Markt bringen, eine Herstellungsstätte in China. Auch Antigenkomponenten für die in Deutschland und der EU zugelassenen Impfstoffe beziehe keiner von dort.
China auf dem globalen Impfstoff-Markt
2014 hatte die Weltgesundheitsorganisation (WHO) noch optimistisch gemeldet, dass China in den globalen Impfstoff-Markt eintritt: „Die WHO ist überzeugt von der Qualität, Sicherheit und Wirksamkeit von Impfstoffen, die in China hergestellt werden”, sagte damals Dr. Margaret Chan, die damalige WHO-Generaldirektorin. Mittlerweile gibt es mehrere chinesische Impfstoffe, die von der WHO vorqualifiziert wurden, und somit für den globalen Markt geeignet sein sollen. Die entsprechende Liste lässt sich im Internet einsehen; der aktuell betroffene Impfstoff-Hersteller findet sich dort nicht. In der damaligen Mitteilung der WHO ist auch zu lesen, dass China seit Jahrzehnten Impfstoffe im Rahmen von Hilfsprogrammen in ärmere Länder exportiere (darunter auch solche gegen Diphtherie, Pertussis und Tetanus).
Mehr zum Thema

Zweifelhafte Tollwut-Imfpstoffe
Chinesischer Imfpstoffskandal: PEI gibt Entwarnung für Deutschland
Impfstoff-Skandal in China
Chinesische Pharma-Managerin festgenommen
Im Mittelpunkt standen im Sommer zunächst Impfstoffe gegen Tollwut, jedoch sollen Changsheng und andere Firmen auch minderwertige Kombi-Impfstoffe gegen Diphtherie, Tetanus und Keuchhusten in Umlauf gebracht haben. Dazu soll nun ebenfalls ein Ermittlungsverfahren eingeleitet worden sein. Im Oktober 2017 war eine fehlerhafte Charge von DPT-Impfstoffen des Herstellers aufgefallen und die Produktion gestoppt worden. Und auch 2016 hatte es in China einen Impf-Skandal gegeben: Damals waren Impfstoffe verkauft worden, deren Haltbarkeit abgelaufen war oder die unangemessen gelagert worden waren. Mehr als 350 Funktionäre wurden damals bestraft.
China prüft strengere Gesetze gegen Arzneimittelfälschungen
Am 22. Oktober vermeldete Xinhua nun, dass China derzeit an strengeren Gesetzen gegen Arzneimittelfälschungen arbeite. Demnach hat China am vergangenen Montag damit begonnen, einen Entwurf zur Änderung des Arzneimittelgesetzes zu prüfen. Die Änderungen sollen härtere Strafen vorsehen: Wer ohne Erlaubnis Arzneimittel herstellt, soll dem Entwurf zufolge in Zukunft mit Geldstrafen belegt werden können, die das Fünf- bis 30-fache des Verdienstes betragen – aktuell sollen sich Geldstrafen nur auf das Zwei- bis Fünffache belaufen.
Mehr zum Thema

Verunreinigungen in Valsartan
Kompromisslos der Qualität verpflichtet – unabhängig vom Produktionsstandort?
Der Gesetzentwurf folgt mit einer Woche Abstand auf die Geldstrafe, die gegen den Impfstoffhersteller Changchun Changsheng verhängt wurde. Dementsprechend werden laut Xinhua auch die Verwaltung und Überwachung von Impfstoffen im Entwurf besonders hervorgehoben: Impfstoffe, Blutprodukte und Anästhetika würden als Spezialarzneimittel definiert, die nicht für die Lohnfertigung zugelassen sind. Zudem werde von den Zulassungsinhabern der Impfstoffe verlangt, dass sie ihre Produkte pflichtversichern.
Arzneimittelüberwachung soll erweitert werden
Die Arzneimittelüberwachung insgesamt soll nicht nur verschärft, sondern auch erweitert werden – auf die Rohstoffversorgung, Herstellung und Vorverkaufsprüfung. Der Entwurf führt dem Bericht zufolge einen Mechanismus zur vollständigen Rückverfolgbarkeit und ein Rückrufsystem ein. Hersteller, die Arzneimittelsicherheitsrisiken nicht erkennen oder beseitigen, sollen von der Produktion und dem Verkauf ausgeschlossen werden. Außerdem wird ein Arzneimittelsicherheitssystem vorgeschlagen, mit dem entsprechende Informationen rechtzeitig aktualisiert und veröffentlich werden sollen – beispielsweise Herstellungserlaubnisse, Ergebnisse täglicher Inspektionen und Verstöße.
Forschungseinrichtungen als Zulassungsinhaber
Neben dem Sicherheitsaspekt wolle der Entwurf auch Innovationen fördern, so Xinhua. Und zwar mithilfe eines „Marktzulassungsinhaber-Systems“ (MAH). Das MAH-System werde seit 2015 in einem dreijährigen Pilotprojekt getestet: Darin dürfen nicht nur Pharmaunternehmen Marktzulassungen erwerben, sondern auch Forscher und Institutionen. Der Entwurf will das MAH-System aber strenger regeln – beispielsweise dadurch, dass Zulassungsinhaber verpflichtet sind, die Sicherheit und Wirksamkeit von Arzneimitteln auch nach dem Markteintritt weiter zu bewerten.
Außerdem ist eine Änderung des generellen Strafprozessrechts vorgesehen, auch das geht aus einer Meldung von Xinhua hervor. Ein Entwurf sehe vor, ein Strafverfahren auch dann fortsetzen zu können, wenn der Angeklagte aus China geflohen ist – etwa bei korruptionsbezogenen Kriminalfällen oder schweren Fällen, die die Staatssicherheit gefährden.





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.