
- DAZ.online
- News
- Apotheke
- Seit wann werden ...
Kommentar
Seit wann werden Tabletten gelüftet?
Stuttgart - 07.09.2021, 07:00 Uhr

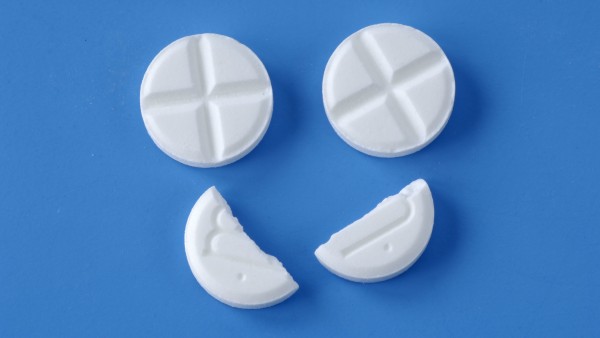
Einmal an die frische Luft: Wenn Metoprololsuccinat AL 95 mg stinken, rät die AMK, die Tabletten auszulüften. (s / Foto: Sergey / AdobeStock)
Wenn Metoprololsuccinat AL 95 mg stinken, rät die AMK, die Tabletten auszulüften. Sie fürchtet um die Einnahmetreue der Patienten. Doch fördert dann tatsächlich Lüften das Zutrauen der Patienten in die einwandfreie Qualität ihres Arzneimittels? DAZ-Redakteurin und Apothekerin Celine Müller zweifelt, ob bei „chemisch, ranzig, cannabis- oder knoblauchartig“ sowie unspezifisch „unangenehm“ riechendem Metoprolol Auslüften wirklich die optimale Adhärenz-fördernde Maßnahme ist.
Metoprololsuccinat Al 95 mg Retardtabletten stinken. Das berichten nicht nur Apotheken der Arzneimittelkommission der Deutschen Apotheker (AMK), auch das ZL bestätigt nach „Geruchsprüfung nach Ph. Eur. 2.3.4 (…) in allen Fällen auch nach 15 Minuten einen deutlich wahrnehmbaren Geruch der Retardtabletten im Vergleich zum entleerten Aluminium/Aluminium-Blister“, schreibt die AMK. Das Problem ist wohl neu, denn zwischen 2013 und 2020 erreichte die AMK gerade einmal eine einzige Meldung zu unangenehm riechendem Metoprolol, seit Mai dieses Jahres sind mittlerweile schon 54 Meldungen bei der AMK eingetrudelt. Stets sei der Geruch direkt nach Ausblistern der Tablette aufgetreten – als „chemisch, ranzig, cannabis- oder knoblauchartig“ sowie unspezifisch „unangenehm“ wird er beschrieben. Wie auch immer: Kein Duft, den man mit seinem Arzneimittel schlucken möchte – solange es sich nicht um Sativex oder Knoblauchpillen handelt.
Mehr zum Thema
Doch woran liegt`s? An Erklärungen mangelt es nicht. Da die Bulkware beim Hersteller nicht müffelt, könnte es folglich an der Verpackung liegen – und in der Tat: „Als mögliche Ursache wird die Kunststoff-Aluminium-Formfolie für die Verblisterung genannt, da diese bei allen betroffenen Chargen des Fertigarzneimittels identisch ist“. Ein sensorischer Test des Folienherstellers habe ergeben, dass der Geruch vom Kunststoffanteil der Folie ausgeht. Und weiter: „Es wird vermutet, dass die aus der Folie freigesetzten Geruchsmoleküle von der mikrokristallinen Cellulose, einem Hauptbestandteil der Retardtabletten, angenommen wird“, erklärt die AMK. Das würde auch erklären, warum der penetrante Geruch selbst nach der Entnahme weiterhin von den Tabletten ausgehe.
Nun ist Geruchsempfinden eine stark individuelle Sache – wie sonst ließe sich erklären, dass Alba-Trüffel bei manchen wahre Gaumenverzückungen auslösen und andere, angewidert von dem moschusartigen Geruch, auffällig die Nase rümpfen. Das räumt auch die AMK ein – relativiert jedoch auch sofort, dass der Geruch ja im Vergleich zu vormals eingenommenen Chargen aufgefallen sei, das heißt: Zuvor war der unangenehme Geruch offenbar nicht da.
Gefahr erkannt, Gefahr gebannt?
Nun könnte man meinen: Gefahr erkannt, Gefahr gebannt – und die betroffenen Chargen des Arzneimittels werden zurückgerufen. Immerhin wurden im Zusammenhang mit den unangenehm riechenden Tabletten bereits Nebenwirkungen wie erhöhter Blutdruck – nach Absetzen – berichtet. Und in der Tat fürchtet die AMK, dass Patienten wenig Vertrauen in ihre müffelnden Betablocker von AL haben – Überraschung – und diesen eigenmächtig absetzen. Rückruf? Pustekuchen. Den gibt es nicht. Stattdessen hat die AMK eine andere Idee: auslüften. Wenn das nichts hilft, bleibe der Austausch des Herstellers als Ultima ratio mit pharmazeutischen Bedenken.
Mag man an dieser Stelle des AMK-Schriebs zunächst verifizierend mit dem Blick, zurückschweifen, ob man sich nicht verlesen hat, bittet die AMK Apotheker:innen aber tatsächlich, Patienten, die einen unangenehmen Geruch bei Metoprololsuccinat 95 mg Retardtabletten der Firma AL beklagen, angemessen zu beraten und auf die Risiken, die von einem eigenmächtigen Absetzen ausgehen können, hinzuweisen. „Wenn ein ,Auslüften‘ der Tablette nach dem Ausblistern oder die Einnahme zum Essen nicht zur Besserung der Einnahmetreue beitragen, sollte eine engmaschige Blutduckkontrolle und ein Herstellerwechsel erwogen werden“.
Ist das klug?
Sorgt sich die AMK nicht, dass die Geruchsmoleküle vielleicht wenig gesundheitsförderlich sind oder gar Bindungen mit Stoffen in der Tablette eingehen? Die DAZ hat das interessiert und nachgefragt. Dort kann man zur Reaktivität der Tabletten jedoch nichts Genaueres sagen, da die Informationen vom Hersteller stammten. Zumindest sieht die AMK keine Gesundheitsgefahr, schließlich sei der Geruch von den Inhaltsstoffen der Folie bekannt, weswegen man die Tabletten auch nicht zurückgerufen habe. Die Standardempfehlung der AMK sei in diesen Fällen nun mal Lüften, bei Metoprolol sei das technologisch auch kein Problem, erklärt die AMK. Jedoch schließt die AMK auch einen Rote-Hand-Brief nicht aus, das erfolge sodann aber in Abstimmung mit der Behörde.
Auch wenn laut § 4 Arzneimittelgesetz die Qualität eines Arzneimittels, die nach Identität, Gehalt, Reinheit, sonstigen chemischen, physikalischen, biologischen Eigenschaften oder durch das Herstellungsverfahren bestimmt wird, vielleicht nicht beeinträchtigt ist, haftet der Lüftungs-Empfehlung der AMK doch eine abenteuerliche Konnotation an. Auch im Falle einer Nichtgesundheitsgefährdung muten „chemisch, ranzig, cannabis- oder knoblauchartig“ sowie unspezifisch „unangenehm“ wohl wenig vertrauenserweckend für den Konsumenten an – und Hand auf’s Herz: Wer würde denn die stinkenden Tabletten, in die Geruchsmoleküle der Blisterfolie diffundiert sind, selbst einnehmen wollen? Zumal Metoprololsucccinat nicht gerade ein Orphan Drug ist.
Wäre es im Sinne der Adhärenz folglich nicht klüger, die Tabletten aus dem Verkehr zu ziehen, statt den Apothekern zu empfehlen, sie sollten ihre Patienten beraten und dahingehend beruhigen – die Tabletten stinken zwar, das ist aber nicht schlimm?


























3 Kommentare
Leaching = Rückruf
von Indupharmie am 08.09.2021 um 10:12 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
mal richtig durchlüften
von J.M.L. am 07.09.2021 um 9:05 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Lüften von Tabletten
von Constanze Schäfer am 07.09.2021 um 8:11 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Das Kommentieren ist aktuell nicht möglich.