
Thema
Zulassung

Casgevy – EMA empfiehlt erstmals Zulassung einer Genscherentherapie
Die Europäische Arzneimittel-Agentur empfiehlt, das vor kurzem in Großbritannien und in den USA zugelassene Gentherapeutikum Casgevy auch in der EU „bedingt“ zuzulassen. Es soll bei den ... » Weiterlesen

GesundheitsID für Private
mik | Der Verband der Privaten Krankenversicherungen (PKV) hat am Freitag vergangener Woche mitgeteilt, dass die Gematik die erste Zulassung für eine digitale Identität für Privatversicherte ... » Weiterlesen

Fortschritt im Kampf gegen Malaria
gg | Seit den 1940er-Jahren beschäftigt die Suche nach einer Schutzimpfung gegen Malaria auslösende Plasmodien die Wissenschaft. 2023 erfüllte mit R21/Matrix-M erstmals ein Impfstoffkandidat die ... » Weiterlesen

GesundheitsID für Privatversicherte
Bereits im September gab es von der Gematik die erste Zulassung für eine digitale Identität bei einer Gesetzliche Krankenversicherung. Wie der PKV mitteilt, gibt es jetzt auch eine Zulassung der ... » Weiterlesen

Brustkrebs vorbeugen
Anfang November wurde in Großbritannien der Aromatase-Hemmer Anastrozol nun auch für die Prävention eines Mammakarzinoms zugelassen. Die Zulassungserweiterung betrifft Frauen nach der Menopause mit... » Weiterlesen

Mit JAK-3-Inhibitor Ritlecitinib gegen Alopecia areata
Seit November 2023 ist das peroral verfügbare Immunsuppressivum Ritlecitinib (Litfulo®) zur Behandlung von Patienten mit schwerer Alopecia areata auf dem deutschen Markt erhältlich. Die Wirkung ... » Weiterlesen
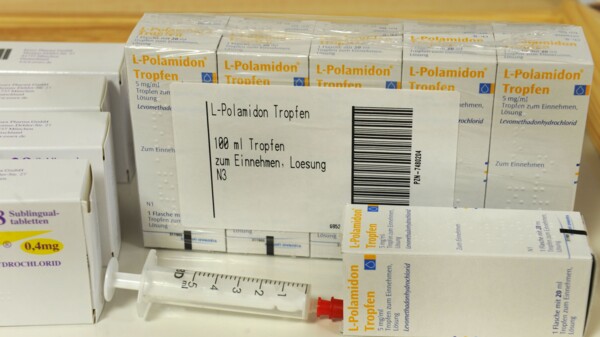
L-Polamidon künftig von Hexal
L-Polamidon® (Wirkstoff Levomethadon) wird künftig von Hexal vertrieben. Der Generikahersteller übernimmt den Vertrieb und die Zulassung für die Lösung zum Einnehmen und die Tabletten sowie für ... » Weiterlesen

Hitzewallungen – EMA empfiehlt Fezolinetant zur Zulassung
In der EU könnte für die Menopause und damit verbundene vasomotorische Symptome mit Fezolinetant bald ein neuer Wirkstoff zur Verfügung stehen – zumindest, wenn es nach dem ... » Weiterlesen
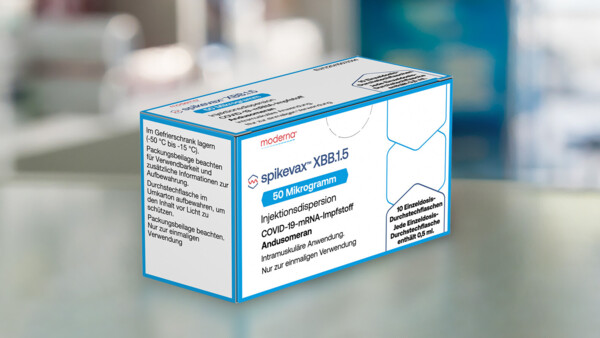
An XBB.1.5 angepasste COVID-19-Vakzine von Moderna in der EU zugelassen
Nachdem der an die SARS-CoV-2-Subvariante XBB.1.5 angepasste Impfstoff von Biontech/Pfizer bereits vor zwei Wochen die europäische Zulassung erhalten hatte, zieht Moderna nach. Auch Spikevax XBB.1.5 ... » Weiterlesen

Gematik erteilt Zulassung für erste GesundheitsID
Ab dem kommenden Jahr müssen die Krankenkassen ihren Versicherten eine digitale Identität anbieten, mit der ihre Versicherten beispielsweise das E-Rezept oder die elektronische Patientenakte nutzen ... » Weiterlesen

Wann sind Arzneimittel bioäquivalent?
Das Bioäquivalenz-Konzept dient als Grundlage in der Zulassung generischer Arzneimittel. Bisweilen wird es jedoch als „wenig geeignet“ oder sogar „gescheitert“ bezeichnet. Dieser Einschä... » Weiterlesen

Wann ist etwas bioäquivalent?
Anfang des Jahres wurden zwei Beiträge in der Deutschen Apotheker Zeitung veröffentlicht, in denen das Bioäquivalenz-Konzept als Grundlage für die Zulassung von generischen Arzneimitteln kritisch ... » Weiterlesen
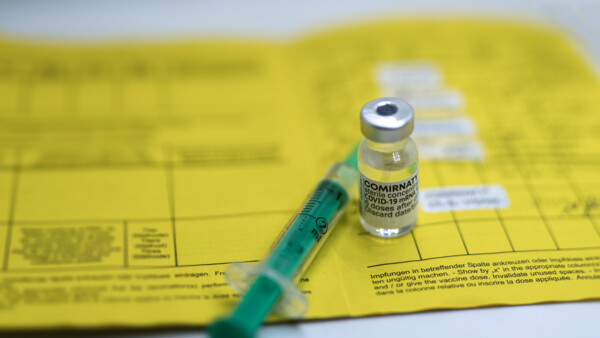
Comirnaty Omikron XBB.1.5 erhält europäische Zulassung
Der an aktuell kursierende Varianten von SARS-CoV-2 angepasste Impfstoff aus dem Hause Biontech und Pfizer wurde am 1. September 2023 in Europa zugelassen. Apotheken sollen den Impfstoff bis zum 12. ... » Weiterlesen
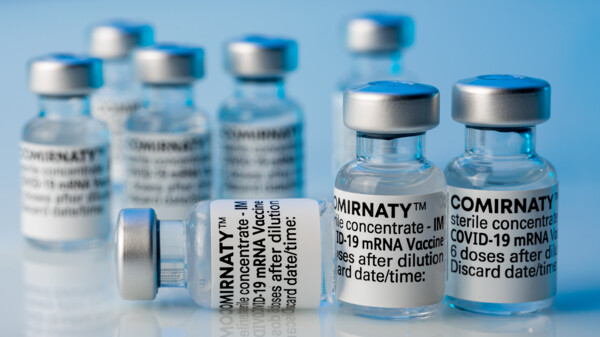
CHMP empfiehlt Zulassung eines an XBB.1.5 angepassten COVID-19-Impfstoffs
Nach Comirnaty, Comirnaty Original/Omicron BA.1 und Comirnaty Original/Omicron BA.4-5 haben Biontech und Pfizer nochmal nachgelegt. Ihrem neuen, an derzeit kursierende ... » Weiterlesen

Neue Option gegen epileptische Anfälle
js | Ende Juli 2023 erteilte die Europäische Kommission die Zulassung für Ganaxolon (Ztalmy®). Es ist für Kinder das erste Arzneimittel gegen epileptische Anfälle im Zusammenhang mit der CDKL5-... » Weiterlesen

EMA empfiehlt neue Behandlungsoption beim kreisrunden Haarausfall zur Zulassung
Ganze 14 Arzneimittel hat der Ausschuss für Humanarzneimittel der Europäischen Arzneimittelagentur im Juli zur Zulassung empfohlen. Darunter ist auch ein Inhibitor der Januskinase 3 zur Behandlung ... » Weiterlesen

Tysabri bekommt Konkurrenz
jb/dpa-AFX | Der Ausschuss für Humanarzneimittel der Europäischen Arzneimittel-Agentur hat den Zulassungsantrag für ein Natalizumab-Biosimilar positiv bewertet » Weiterlesen

Wirkstoff Gefapixant gegen chronischen Husten zur Zulassung empfohlen
Im Juli empfahl der Ausschuss für Humanarzneimittel der EMA gleich 14 neue Arzneimittel zur Zulassung – darunter auch den Wirkstoff Gefapixant (Lyfnua) in der Indikation refraktärer oder ... » Weiterlesen

RSV-Impfstoff für Schwangere zur Zulassung empfohlen
Mit Spannung wird ein Impfstoff gegen RSV (Respiratory Syncytial Virus) für den Schutz von Säuglingen erwartet. Eine Zulassungsempfehlung der EMA rückt diesen nun in greifbare Nähe: Geimpft werden... » Weiterlesen

Natalizumab-Biosimilar zur Zulassung empfohlen
Das MS-Arzneimittel Tysabri (Natalizumab) bekommt wohl demnächst Biosimilar-Konkurrenz. Der Ausschuss für Humanarzneimittel (CHMP) der Europäischen Arzneimittel-Agentur (EMA) hat ein entsprechendes... » Weiterlesen




















Foto: psdesign1 / Fotolia