
Thema
Zulassung

Diskussion der Bioäquivalenz-Leitlinie
Der International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use (ICH) hat den Entwurf für seine M13-Bioäquivalenz-Leitlinie zur Kommentierung durch die ... » Weiterlesen

Migräneprophylaxe – EMA empfiehlt Atogepant zur Zulassung
Mit Atogepant (Aquipta) soll nach Rimegepant (Vydura) das zweite „Gepant“ bei Migräne in der EU zugelassen werden. Für wen eignet sich Atogepant und wie unterscheiden sich die beiden neuartigen ... » Weiterlesen

Vom Wundermittel zum Ladenhüter (und zurück)
Groß waren die Erwartungen und Hoffnung an die Kombination aus Nirmatrelvir und Ritonavir (PaxlovidTM) zur COVID-19-Behandlung bei Erwachsenen, ca. eine Million Packungen hatte die Bundesregierung im... » Weiterlesen

Beschleunigte Stabilitätsuntersuchungen dank Mechanochemie
Stabilitätsdaten sind im Rahmen der Zulassung neuer Arzneimittel unerlässlich. Um sie zu generieren, bedarf es allerdings sehr viel Zeit. Daher haben Wissenschaftler ein neues mechanochemisches ... » Weiterlesen

Chikungunyafieber – Impfstoffentwicklung macht Fortschritte
Die von Mücken übertragene Viruserkrankung Chikungunyafieber gehört zu den Tropenkrankheiten, die bedingt durch die klimatischen Veränderungen mittlerweile auch in Europa auftreten. Für einen ... » Weiterlesen
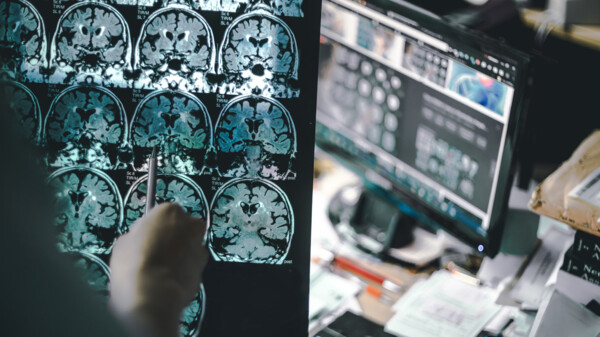
Donanemab – dritter Alzheimer-Antikörper in den Startlöchern?
Eli Lilly hat erste Ergebnisse der Phase-III-Studie TRAILBLAZER-ALZ 2 mit dem Anti-Amyloid-Antikörper Donanemab bekannt gegeben: Der Antikörper verlangsamte die klinische Verschlechterung von ... » Weiterlesen

Erster RSV-Impfstoff zur Zulassung empfohlen
Die Frage „wann kommt der erste RSV-Impfstoff“ ist in den letzten Monaten gehäuft gestellt worden – eine Antwort ist nun ein ganzes Stück näher gerückt: Die europäische Arzneimittelbehörde... » Weiterlesen

Streit um Mifepriston in den USA geht weiter
Kürzlich sollte im US-Bundesstaat Texas die Zulassung von Mifepriston ausgesetzt werden, das zum medikamentösen Schwangerschaftsabbruch eingesetzt wird. Bevor der Beschluss in Kraft treten konnte... » Weiterlesen

Ghana lässt Malaria-Impfstoff zu
In Ghana erhielt ein Malaria-Impfstoff erstmals eine nationale Zulassung: „R21/Matrix-M“ hat als erster Impfstoffkandidat das internationale Ziel einer 75-prozentigen Schutzwirkung geknackt. ... » Weiterlesen
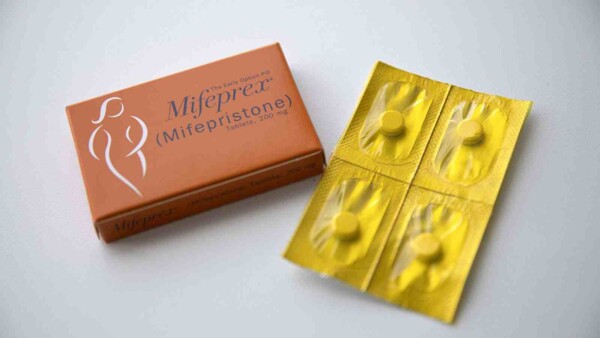
Mifepriston: US-Richter setzen Zulassung aus, Regierung interveniert
Im US-Bundesstaat Texas hat ein konservativer Richter die Zulassung von Mifepriston, das zum medikamentösen Schwangerschaftsabbruch angewendet wird, ausgesetzt. Der am vergangenen Freitag (Ortszeit) ... » Weiterlesen
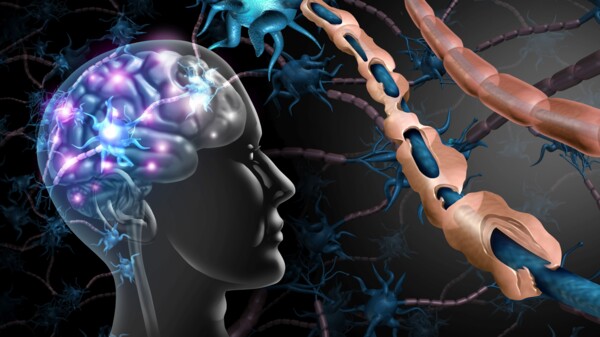
Zulassungsempfehlung für Ublituximab bei Multipler Sklerose
Der Ausschuss für Humanarzneimittel der Europäischen Arzneimittelbehörde EMA empfiehlt die Zulassung von Briumvi (Wirkstoff Ublituximab) für die Therapie der schubförmigen Multiplen Sklerose. Die... » Weiterlesen

Neuer Antikörper bei Colitis ulcerosa kurz vor Zulassung
Mit Mirikizumab hat das CHMP erstmals die Zulassung eines ausschließlichen Interleukin (IL)-23-Inhibitors für die Therapie der chronisch-entzündlichen Darmerkrankung Colitis ulcerosa auf ... » Weiterlesen

Adipositas-App Zanadio – jetzt auch für Männer verordnungsfähig
Die Zulassung der Adipositas-App Zanadio wurde erweitert, damit ist sie eine Regelleistung für alle Geschlechter. Für Frauen und nichtbinäre Personen ist Zanadio bereits seit Mitte 2022 dauerhaft ... » Weiterlesen

Hilfe bei Off-Label-Use
Den Einsatz von Fertigarzneimitteln außerhalb der zugelassenen Anwendung bezeichnet man als Off-Label-Use. Insbesondere in Fachgebieten wie der Palliativmedizin spielt er eine wichtige Rolle, da es ... » Weiterlesen

Haarwuchs mit Folgen
Nicht selten leuchten Sicherheitssignale neuer Wirkstoffe erst nach der Zulassung auf. So auch im Fall Finasterid: Vor über zehn Jahren gab es die ersten Fälle des Post-Finasterid-Syndroms. Junge M... » Weiterlesen

Apotheken dürfen Lagevrio nicht mehr abgeben
Der Humanarzneimittelausschuss der EMA empfiehlt das COVID-19-Medikament Lagevrio (Molnupiravir) nicht zur Zulassung. Das hat hierzulande unmittelbare Konsequenzen: Wie das BfArM informiert, darf das ... » Weiterlesen

Wo bleiben die Cannabis-Fertigarzneimittel?
mp | Die seit März 2017 mögliche Versorgung mit Medizinalcannabis findet fast ausschließlich abseits zugelassener Fertigarzneimittel statt. Dies zu ändern, hätte für Ärzte, Apotheken und ... » Weiterlesen

Diskussion um Atezolizumab bei Blasenkrebs
Der Checkpoint-Inhibitor Atezolizumab darf in den USA nicht mehr zur Behandlung von Urothelkarzinomen eingesetzt werden, da eine geforderte Postmarketing-Studie keinen Vorteil beim Gesamtüberleben ... » Weiterlesen

Der Wunsch nach Cannabis-Fertigarzneimitteln wird lauter
Die Patientenversorgung mit Medizinalcannabis beruht seit 2017 auf einer Übergangslösung: Denn die Therapie spielt sich fast ausschließlich außerhalb zugelassener Fertigarzneimittel ab. Die Lücke... » Weiterlesen




















Foto: psdesign1 / Fotolia