
- DAZ.online
- DAZ / AZ
- DAZ 6/2005
- Hätte die Marktrü...
Arzneimittel und Therapie
Hätte die Marktrücknahme früher erfolgen müssen?
Rofecoxib (Vioxx®) wurde am 30. September 2004 vom Markt genommen, als die Approve-Studie (Adenomatous polyp prevention on Vioxx) ein erhöhtes kardiovaskuläres Risiko bei mehr als 18-monatiger Einnahme gezeigt hatte. In dieser Studie nahmen Patienten, die an kolorektalen Adenomen gelitten hatten, den Cyclooxygenase-2-Hemmer zum Schutz vor erneuten kolorektalen Polypen ein.
VIGOR-Studie falsch gedeutet?
Rofecoxib war im Jahr 1999 als Antirheumatikum zugelassen worden. Seine Indikationsgebiete waren Arthrose und chronische Polyarthritis. Bald nahm es insbesondere in den USA eine marktbeherrschende Stellung unter den verordneten nicht-steroidalen Antirheumatika ein. Im Jahr 2000 ergab die VIGOR-Studie (Vioxx gastrointestinal outcomes research) für Patienten mit Rofecoxib im Vergleich zu Patienten mit Naproxen ein auf das Vierfache (laut FDA-Daten sogar Fünffache) erhöhtes Herzinfarktrisiko. Dieser Unterschied im kardiovaskulären Risiko wurde jedoch als kardioprotektive Wirkung von Naproxen und nicht als kardiotoxische Wirkung von Rofecoxib gewertet.
Kumulative Metaanalyse
In einer kumulativen Metaanalyse wurde kürzlich untersucht, ob schon vor September 2004 Beweise für die Nebenwirkungen von Rofecoxib vorlagen. Die Metaanalyse erfasste:
- alle randomisierten klinischen Studien, in denen Rofecoxib in einer Tagesdosis von 12,5 bis 50 mg an erwachsenen Patienten mit chronischen muskuloskelettalen Störungen mit anderen nicht-steroidalen Antirheumatika oder Plazebo verglichen wurde,
- Kohorten- und Fall-Kontroll-Studien, die den Zusammenhang zwischen Naproxen-Einnahme und kardiovaskulärem Risiko untersuchten. Randomisierte plazebokontrollierte Studien zur kardioprotektiven Wirksamkeit von Naproxen gibt es nicht.
Literaturdatenbanken und die Dateien der amerikanischen Gesundheitsbehörde FDA wurden nach entsprechenden Studien durchsucht. Als primärer Endpunkt wurde der Herzinfarkt festgelegt. 18 randomisierte, kontrollierte Studien mit 25.273 Patienten und elf Beobachtungsstudien – acht Fall-Kontroll-Studien und drei retrospektive Kohortenstudien – erfüllten die Einschlusskriterien.
Art und Qualität der Rofecoxib-Studien
Rofecoxib wurde in zwölf randomisierten Studien bei Arthrose geprüft, in fünf bei chronischer Polyarthritis und in einer bei unteren Rückenschmerzen. Die meisten Studien besaßen drei oder vier Behandlungsarme; meist wurden mehrere Rofecoxib-Dosierungen eingesetzt. 14 Studien enthielten einen Plazebo-Arm. Die Studien dauerten zwischen vier Wochen und über einem Jahr. Fünf Studien hatten eine Erweiterungsphase, in vier davon wurden Daten zur kardiovaskulären Sicherheit gesammelt. Vier Studien hatten eine ausreichende Verblindung. In acht Studien wurden kardiovaskuläre Ereignisse extern begutachtet.
Mehr Herzinfarkte in Rofecoxib- als in Kontroll-Armen
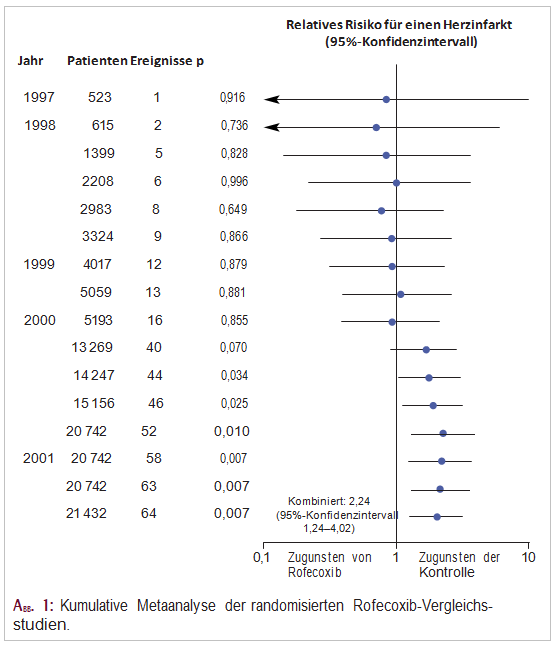
Bis im Jahr 2001 waren in 16 Rofecoxib-Studien mit 21.432 Patienten 64 Herzinfarkte aufgetreten, davon 52 in Rofecoxib- und 12 in Kontrollgruppen. Das relative Risiko für einen Herzinfarkt mit Rofecoxib betrug 2,24. Bereits am Ende des Jahres 2000 waren in einer Studienpopulation von insgesamt 20.742 Patienten 52 Herzinfarkte aufgetreten (Abb. 1), und das relative Risiko betrug 2,3.
Die jüngsten Daten zum Herzinfarktrisiko unter Rofecoxib stammen aus dem Oktober 2001. Spätere Studien berichteten nicht mehr über kardiovaskuläre Ereignisse. Das relative Risiko hing nicht wesentlich davon ab, ob im Kontrollarm Plazebo, Naproxen oder ein anderes nicht-steroidales Antirheumatikum verwendet wurde. Auch Dosis und Dauer der Rofecoxib-Behandlung schienen das relative Risiko für einen Herzinfarkt kaum zu beeinflussen. Dagegen war das relative Risiko für einen Herzinfarkt in solchen Studien größer, in denen ein externes Komitee die kardiovaskulären Ereignisse begutachtet hatte. Das relative Risiko für Schlaganfälle war mit 1,02 nicht erhöht: Von 44 Schlaganfällen in elf Vergleichsstudien waren 25 in Rofecoxib- und 19 in Kontrollgruppen aufgetreten.
Naproxen kaum kardioprotektiv
Die Naproxen-Beobachtungsstudien hatten unterschiedliche kardiovaskuläre Zielkriterien (z. B. Herzinfarkt, erster Herzinfarkt, Herzinfarkt/Koronartod, Herzinfarkt/plötzlicher Herztod). Alle bis auf eine Studie verwendeten Daten aus großen klinischen oder administrativen Datenbanken, vier davon Daten aus der UK General Practice Research Database. Sowohl im Vergleich zu Personen, die keine nicht-steroidalen Antirheumatika einnahmen, als auch im Vergleich zu Anwendern anderer nicht-steroidaler Antirheumatika hatten Naproxen-Anwender nur ein geringfügig reduziertes kardiovaskuläres Risiko (relatives Risiko 0,86). Die Beobachtungsstudien ergaben also, dass Naproxen wenn überhaupt nur eine geringe kardioprotektive Wirkung hat, die allein das bessere kardiovaskuläre Abschneiden in der VIGOR-Studie nicht erklären kann.
Marktrücknahme kommt vier Jahre zu spät
Dieser Metaanalyse zufolge lagen bereits im Jahr 2000 genug Daten vor, die ein erhöhtes Herzinfarktrisiko unter Rofecoxib belegten. Diese frühen Daten ergaben im Unterschied zur Approve-Studie keinen Hinweis auf eine Dosisabhängigkeit der Kardiotoxizität. Auch die Behauptung der Firma Merck, in den ersten 18 Behandlungsmonaten bestehe kein erhöhtes Herzinfarktrisiko, wird durch die Ergebnisse dieser Metaanalyse in Frage gestellt. Das Ausmaß des Schadens durch Rofecoxib dürfte weit größer sein, als die klinischen Studien es nahe legen, da in ihnen nur wenige Patienten mit kardiovaskulären Vorerkrankungen erfasst wurden.
Susanne Wasielewski, Münster
Quelle
Jüni, P., et al.: Risk of cardiovascular events and rofecoxib: cumulative meta- analysis. Lancet 364, 2021–2029 (2004).
Info
- Metaanalyse In einer Metaanalyse werden alle relevanten Originalarbeiten gesucht. Die Ergebnisse dieser Einzelstudien werden mit statistischen Methoden zusammengefasst.
- Kumulative Metaanalyse Kumulative Metaanalysen sind Metaanalysen, in denen die Studien chronologisch angeordnet sind und dabei für jede neu hinzugekommene Studie ein neues Metaanalysen-Ergebnis dargestellt wird (Abb. 1).





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.