
- DAZ.online
- DAZ / AZ
- DAZ 27/2007
- Platzverweis für HI-
AIDS
Platzverweis für HI-Virus
Hält man Ausschau nach Krank-heiten, die sich durch eine Inter-vention mit einem oder mehreren Vertretern unseres riesigen Arzneimittelschatzes heilen lassen, so fallen einem nur wenige Beispiele ein. Ganz oben auf der Liste stehen allerdings die Infektionskrankheiten, von denen sich viele durch den Einsatz von Antibiotika und Virustatika tatsächlich heilen lassen. Allerdings auf die Frage nach der Möglichkeit einer Heilung einer HIV-Infektion lautet die einfache und ernüchternde Antwort ganz klar: NEIN ... ... zumindest bis zum letzten Freitag des Monats Juni 2007, als morgens langsam durchsickerte, dass in der neuen Ausgabe des renommierten Wissenschaftsmagazins Science ein Artikel enthalten sei, der tatsächlich einen Ansatz zur endgültigen Heilung einer HIV-Infektion aufzeige [1]. Dies sei dadurch möglich, so die ersten Meldungen, dass es Wissenschaftlern aus Dresden und Hamburg gelungen sei, das virale Progenom des HI-Virus aus der Zelle zu entfernen. Denn in der Tat ist die Antwort auf die Frage nach der Heilbarkeit einer HIV-Infektion deshalb so apodiktisch negativ, weil sich die HI-Viren nach einer Infektion der Zelle in Form eines viralen DNA-Progenoms in die DNA der infizierten Zelle integrieren und so zu einem nicht mehr trennbaren Teil dieser DNA werden.
Eine Therapie einer HIV-Infektion bedeutet daher derzeit das "Ruhigstellen" dieses viralen Teilabschnitts der betroffenen Kern-DNA, was im Übrigen in den letzten Jahren immer besser gelingt, so dass sich die HIV-Infektion von einer tödlichen Krankheit zu einer chronischen Infektion gewandelt hat. An Heilung wäre nur zu denken, wenn alle infizierten Zellen ausgerottet würden. Oder?
Tatsächlich zeigt der Ansatz der beiden Gruppen um Joachim Hauber (Max-Planck-Institut für Molekulare Zellbiologie und Genetik, Dresden) und Frank Buchholz (Heinrich-Pette-Institut für experimentelle Virologie und Immunologie, Hamburg) einen alternativen Weg auf. Ihr Ansatz zielt darauf ab, das virale Progenom aus der DNA der infizierten Zelle auszuschneiden.
In der Natur stellt sich dieses Problem ganz konkret immer wieder bei Bakteriophagen und Hefen, die darauf angewiesen sind, bestimmte DNA-Bereiche zu modifizieren. Gelöst wurde das Problem durch die "Erfindung" von Rekombinasen, Enzyme, die an zwei ganz spezifische DNA-Bereiche binden und die zwischen den Bindungsstellen liegende DNA ausschneiden.
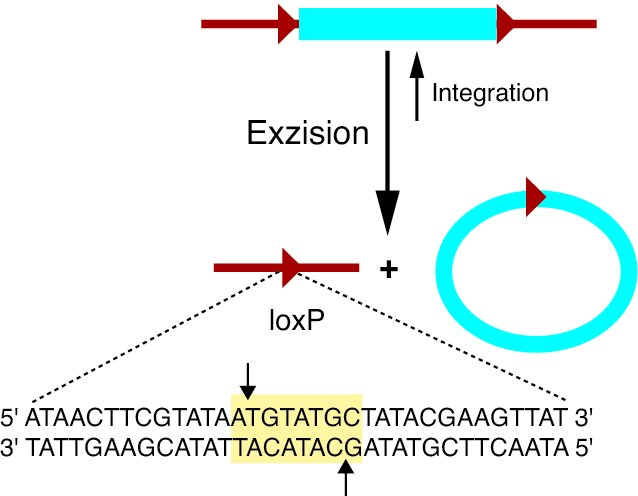
Cre/loxP-Rekombinase-System weist den Weg
Eines dieser Systeme, das heute in der experimentellen Genetik schon fast routinemäßig eingesetzt wird, ist das so genannte Cre/loxP-Rekombinase-System des Bakteriophagen P1 [2]. Dabei katalysiert die Rekombinase Cre (cyclization recombination) die Rekombination zwischen zwei loxP-Erkennungssequenzen (locus of X-over of P1) unabhängig von weiteren Cofaktoren. Die loxP-Sequenz besteht aus einem zentralen Element aus acht Basenpaaren einer bestimmten Orientierung, welches von zwei palindromischen Sequenzen mit 13 Basenpaaren Länge flankiert wird. Ein chromosomales DNA-Segment, das zwischen gleichgerichteten loxP-Sequenzen liegt (man spricht von einem "gefloxten" DNA-Segment), wird durch die Cre-Rekombinase in Form eines zirkulären Produktes aus dem Chromosom herausgeschnitten und in der Zelle abgebaut (Abb. 1). Auf dem Chromosom bleibt eine einzelne loxP-Sequenz zurück. Prinzipiell kann über die Rückreaktion auch fremde DNA ins Chromosom integriert werden. Diese Richtung der Reaktion ist allerdings sehr ineffektiv, da das Gleichgewicht ganz klar auf der Seite der Exzision liegt.
Kein einfaches Verfahren
Seit etwa zehn Jahren wendet man dieses System sehr erfolgreich auch in Säugerzellen an und erzeugt auf diese Weise beispielsweise so genannte gewebespezifische Knockout-Mäuse [3].
Obwohl dieses Verfahren sehr häufig angewendet wird, ist es alles andere als einfach. Man muss zunächst eine Maus "herstellen", in der durch homologe Rekombination das Zielgen oder ein chromosomaler Zielabschnitt durch ein "gefloxtes" Zielgen bzw. einen "gefloxten" Zielabschnitt ausgetauscht wird. Dann benötigt man eine zweite transgene Maus, die eine Cre-Rekombinase enthält, deren Expression von einem Promotor gesteuert wird, der nur in einem ganz bestimmten Zelltyp oder in einem bestimmten Gewebe aktiv ist ("gewebespezifische Cre-Maus"). Schließlich kreuzt man die beiden Tiere. Bei den Nachkommen werden nun die Genbereiche zwischen den loxP-Sequenzen in denjenigen Zellen herausgeschnitten, die die Cre-Rekombinase exprimieren (Abb. 2).
Cre-Rekombinase muss richtige Stelle erkennen
Was fasziniert an diesem Ansatz im Hinblick auf das HIV-Problem? Natürlich die Möglichkeit zur zielgenauen Entfernung des in das Wirtsgenom integrierten proviralen HIV-Genoms durch eine Cre-Rekombinase. Allerdings fehlen dieser Rekombinase in den infizierten Zellen die Erkennungssequenzen, und diese einzufügen – wie im Falle des geschilderten Mausexperimentes – scheidet hier natürlich aus.
Stattdessen haben die Forscher aus Dresden und Hamburg einen äußerst mutigen Alternativweg ausprobiert. Und sie waren erfolgreich!
Sie haben in einem evolutiven Ansatz die Cre-Rekombinase an Erkennungssequenzen "gewöhnt", die in den langen terminalen Wiederholungseinheiten des HIV-1-Genoms (HIV-1 LTRs) vorkommen.
Hierzu wurde zunächst in den LTRs nach Bereichen gesucht, die eine gewisse Sequenzhomologie mit den loxP-Sequenzen aufwiesen – und man hat solche gefunden. Dieser Bereich wurde dann isoliert und in einen so genannten "Evolutionsvektor" kloniert, mit dessen Hilfe in E. coli angezeigt werden kann, ob die Sequenz von einer Cre-Rekombinase erkannt und geschnitten wird [4]. In den E.-coli- Zellen wurden dann Cre-Mutantengene exprimiert, in der Hoffnung, dass sich unter den Mutanten auch solche befänden, die statt der loxP-Sequenz die HIV-1-LTR-Sequenz erkennen würden.
Mühsame Suche nach HIV-spezifischen Cre-Mutanten
Erste Versuche waren erfolglos, da sich offensichtlich die loxP-Sequenzen und die HIV-1-LTR-Sequenzen zu stark unterschieden. Aus diesem Grund wurden "Zwischensequenzen" als Zielsequenzen generiert, um die gewünschte Spezifikationsänderung der Cre-Rekombinase in kleinen Schritten zu vollziehen.
Tatsächlich gelang es, zunächst sehr geringe Rekombinationsaktivitäten in der Mutantenmischung nachzuweisen und immer stärker anzureichern. Nach 126 Evolutionszyklen hatte man das gesteckte Ziel erreicht und hatte Cre-Mutanten mit einer derart veränderten Struktur isoliert, dass sie nun HIV-1-Sequenzen erkannten und den von diesen Sequenzen flankierten DNA-Bereich aus dem Genom entfernten.
Der Sieger heißt Tre
Das beste Enzym nannten die Wissenschaftler Tre, und eine Detailanalyse ergab, dass sich Tre von Cre durch 19 Aminosäureaustausche unterschied.
Im nächsten Experiment wurde getestet, ob Tre auch in Säugerzellen aktiv und spezifisch war. Dieser Test wurde zunächst in HeLa-Zellen, also humanen Epithelzellen eines Zervixkarzinoms, durchgeführt, und zur großen Freude der Wissenschaftler waren die Versuche positiv.
Schließlich wurde die Tre-Rekombinase dahingehend getes-tet, ob sie tatsächlich ein ganzes HIV-Genom auszuschneiden vermochte. Und auch das gelang.
Ein Schritt in Richtung Heilung?
Eine faszinierende Story großer moderner Wissenschaft, die mit einer Publikation in Science be-lohnt wurde! Aber auch ein Ansatz in Richtung neuer Therapiestrategien bei HIV-Infektionen?
Die Autoren sehen das in der Tat so und bezeichnen ihre Arbeit als einen ersten "proof of principle" für einen kurativen Ansatz einer HIV-Therapie. In wie weit dies eine realistische Einschätzung ist, bleibt abzuwarten.
Welche Schwierigkeiten gilt es bei einem solchen Ansatz zu überwinden?
- Zunächst einmal müsste es gelingen, die Tre-Rekombinase effektiv in eine infizierte Zelle einzuschleusen. Dies ist nach heutiger Vorstellung nur durch einen gentherapeutischen Ansatz möglich.
- Die Tre-Rekombinase müsste über lange Zeit stabil exprimiert werden, denn die Autoren zeigten, dass es unter ihren optimalen Zellkulturbedingungen etwa drei Monate dauerte, bis alle HIV-Progenome entfernt waren.
- Die gentherapeutisch veränderten Zellen dürften in ihrer Funktion nicht von der Tre-Rekombinase beeinträchtigt werden, wie generell der Organismus eine gentherapeutische Intervention sicher tolerieren müsste. Hier denken die Wissenschaftler offensichtlich auch über einen extrakorporalen Behandlungsansatz nach, bei dem den Patienten zuvor entnommene und in vitro modifizierte Zellen reinfundiert werden.
- Problematisch dürfte auch das große Diversifizierungspotenzial sein, das gerade die HI-Viren auszeichnet. Sicherlich werden Varianten darunter sein, die von der Tre-Rekombinase nicht mehr erkannt werden.
- Das größte Problem dürfte darin bestehen, dass wirklich alle infizierten Zellen getroffen werden müssten, um nicht nur eine Heilung einzelner infizierter Zellen zu gewährleisten, sondern eine nachhaltige Heilung des Patienten zu erreichen.
Dies alles sind doch so große Hürden, dass eine baldige Option für einen kurativen Therapieansatz sehr unwahrscheinlich erscheint.
Doch schmälert dies in keinster Weise die wissenschaftliche Leistung der beiden Gruppen aus Dresden und Hamburg, die einen mutigen Weg gegangen sind und die Möglichkeiten einer molekularen Evolution am Beispiel eines wirklichen "medical needs" aufgezeigt haben.
Allerdings kann man in Frage stellen, ob diese wissenschaftliche Leistung mit einer Publikation in Science gewürdigt worden wäre, wenn die Machbarkeit der zielgerichteten Rekombination nicht gerade an HIV gezeigt worden wäre, zumal in der Science-Ausgabe auch ein sehr kritisches Editorial publiziert wurde. Mit Sicherheit hätte die Arbeit jedoch nicht diese Medienpräsenz erfahren.
Literatur[1] Sarkar I, Hauber I, Hauber J, Buchholz F: HIV-1 Proviral DNA Excision Using an Evolved Recombinase. Science 2007; 316: 1912–1915.
[2] Sauer B, Henderson N: Site specific DNA recombination in mammalian cells by the Cre recombinase of bacteriophage P1. Proc Natl Acad Sci U.S.A. 1988; 85: 5166–5170.
[3] Gu H, Marth JD, Orban PC, Mossmann H, Rajewsky K: Deletion of a DNA polymerase beta gene segment in T cells using cell type-specific gene targeting. Science 1994; 265: 103–106.
[4] Buchholz F, Stewart AF: Alteration of Cre recombinase site specificity by substrate-linked protein evolution. Nature Biotechnology 1991; 19: 1047–1052.
Prof. Dr. Theo Dingermann, Dr Ilse Zündorf, Institut für Pharmazeutische Biologie, BiozentrumMax-von-Laue-Straße 960438 Frankfurt



















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.