
- DAZ.online
- DAZ / AZ
- DAZ 29/2007
- Tumorerkrankungen
Arzneimittel und Therapie
Tumorerkrankungen
Cetuximab zweimal auf dem Weg in die First-line-Therapie
Als vor wenigen Jahren die neuen zielgerichteten Therapien auf den Markt kamen, bewiesen sie zunächst – besonders bei soliden Tumoren, bei denen sich hochwirksame Zytostatika als Standard etabliert hatten – ihren Stellenwert in den Zweit- oder Dritt-Linien-Therapien. Da hier die Wirksamkeiten sehr überzeugend waren, lag es nahe, diese Therapien auch in der First-line zu testen. Diesbezüglich machte Cetuximab (Erbitux®) gleich zweimal auf sich aufmerksam: bei metastasierten kolorektalen Karzinomen und bei fortgeschrittenen Kopf- und Halstumoren.
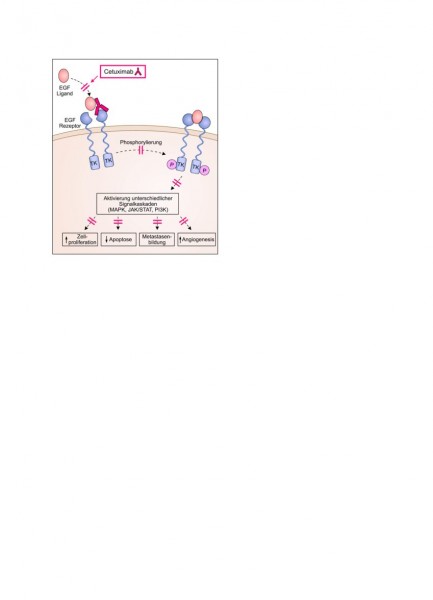
Cetuximab ist ein monoklonaler Antikörper, der den EGF-Rezeptor (Epidermal Growth Factor Receptor), der bei sehr vielen soliden Tumoren überexprimiert wird, blockiert. Bisher ist Cetuximab sowohl in den Vereinigten Staaten als auch in Europa bei einigen Entitäten für die Zweit-Linien-Therapie zugelassen, so z. B. nach Versagen anderer Chemotherapien bei kolorektalen Karzinomen und in Kombination mit Strahlentherapie bei Kopf- und Halstumoren.
Jetzt wurden auf dem amerikanischen Krebskongress ASCO (American Society of Clinical Oncology) in Chicago die Ergebnisse von zwei Studien mit Cetuximab in Kombinationstherapien vorgestellt. In der ersten Studie wurde bei Patienten mit EGF-R-positiven kolorektalen Karzinomen die Effektivität von Cetuximab in Kombination mit dem Standardregime FOLFIRI (5-Fluorouracil, Folinsäure und Irinotecan) verglichen mit FOLFIRI allein in der Erst-Linien-Therapie [1]. Zwischen August 2004 und Oktober 2005 wurden 1217 Patienten randomisiert und bekamen entweder Cetuximab (400 mg/m2 initial, dann 250 mg/m2 wöchentlich plus FOLFIRI zweiwöchentlich (Gruppe A) oder nur FOLFIRI (Irinotecan 180 mg/m2 , FA 400 mg/m2 , 5-FU bolus 400 mg/m2 , 5-FU Infusion 2400 mg/m2 über 46 Stunden) (Gruppe B). Primärer Studienendpunkt war progressionsfreies Überleben (PFS), sekundäre Endpunkte Gesamtüberleben, Ansprechrate und Sicherheit. In der Gruppe A wurde ein signifikant längeres medianes progressionsfreies Überleben (8,9 vs. 8 Monate, p = 0,036) und signifikant bessere Ansprechraten (46,9% vs. 38,7%), p = 0,005 erreicht. Die Therapie wurde im Allgemeinen gut vertragen. Die Nebenwirkungen waren wie erwartet moderate Diarrhö und Hautreaktionen. Letztere traten in der Kombinationsgruppe signifikant häufiger auf.
In der zweiten Studie führte die Kombination aus Cetuximab mit Cisplatin oder Carboplatin bei Patienten mit rezidivierenden und metastasierten Kopf-Hals-Tumoren in der First- line-Therapie sogar zu einer Verlängerung des Gesamtüberlebens [2]. 442 Patienten mit diesen Tumoren, die außerdem nicht resezierbar waren, wurden entweder in der Gruppe A mit Cetuximab (initial 400 mg/m2 , dann 250 mg/m2 wöchentlich) plus maximal sechs dreiwöchentliche Zyklen Cisplatin (100 mg/m2 am Tag 1) oder Carboplatin (AUC 5, Tag 1) und in jedem Zyklus vier Tage mit 5-FU (1000 mg/m2) behandelt. In der Gruppe B bekamen die Patienten nur Cisplatin bzw. Carboplatin und 5-FU wie oben beschrieben. Am häufigsten lag bei den Patienten eine Tumorerkrankung von Pharynx (47%) und Larynx (25%) vor. Nach 340 aufgetretenen Todesfällen zeigte sich, dass das mediane Überleben im Arm B nur 7,4 Monate, in dem Arm mit der Cetuximab-Kombination dagegen 10,1 Monate betrug (p = 0,036), eine Überlebenszeit, die bisher in keiner Phase-III-Studie bei diesem Patientenkollektiv jemals erreicht wurde.
Quelle[1] Randomized phase III study of irinotecan and 5-FU/FA with or without cetuximab in the first-line treatment of patients with metastatic colorectal cancer (CRC): the CRYSTAL trial. E. Van Cutsem, M. Nowacki, I. Lang et al. Proc. Am. Cli. Oncol. 25: 164s, abstr. 4000, 2007.
[2] Erbitux extends survival of patients with recurrent or metastatic SCCHN when added to first line platinum based therapy – Results of a randomized phase III (Extreme) study. Vermorken, Mesia, Vega et al. Oral Presentation ASCO 2007.
Apothekerin Dr. Annette Junker



















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.