
- DAZ.online
- DAZ / AZ
- DAZ 40/2016
- Cer-Katalysator zur ...
Prisma
Cer-Katalysator zur organischen Synthese
Potenzial für die Arzneistoffsynthese
Organische Chemiker um Jens Christoffers an der Universität Oldenburg erforschen das Potenzial von Cer-katalysierten Oxidationsverfahren zur Synthese von 1,4-Dicarbonylverbindungen, die der Produktionn verschiedener Heteroaromaten dienen, z. B. von Thiophen-, Pyrrol- und Furan-Derivaten. Der Katalysator besteht aus untoxischem Cer(III)-chlorid-Heptahydrat (CeCl3· 7 H2O), gelöst in Trifluorethanol; das Oxidationsmittel ist molekularer Sauerstoff. Dabei entsteht kein problematischer Abfall wie bei den etablierten Verfahren, jedoch ist die Ausbeute teilweise geringer.
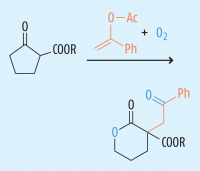
Als neueste Entdeckung stellten zwei Oldenburger Doktorandinnen nun einen einfachen Syntheseweg für bestimmte δ-Lactone vor. Die Reaktion beruht auf einer Baeyer-Villiger-Oxidation eines Ketons (hier: Cyclopentanon-2-carboxyl-Derivat) zu einem Ester (hier: δ-Lacton) mithilfe einer Percarbonsäure (hier: 1-Phenyl-vinylacetat). Die Reaktion läuft bei 30 °C ab und führt zu einem 1,4-Diketon mit einem quartären C-Atom und dem besagten Lactonring. Die Ausbeute bei den bisherigen Versuchen war mäßig bis gut (maximal 74%). Die Oldenburger Arbeitsgruppe will sie weiter optimieren, um das Verfahren für die Industrie interessant zu machen. |
Quelle
Geibel I, et al. Formation of δ-Lactones by Cerium-Catalyzed, Baeyer–Villiger-Type Coupling of β-Oxoesters, Enol Acetates, and Dioxygen. J Org Chem 2016;81(17):7790–7798






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.