
- DAZ.online
- DAZ / AZ
- DAZ 49/2017
- Zwei Seiten einer ...
Schwerpunkt Contergan
Zwei Seiten einer Medaille
Embryotoxizität und Anti-Tumorwirkung von Thalidomid
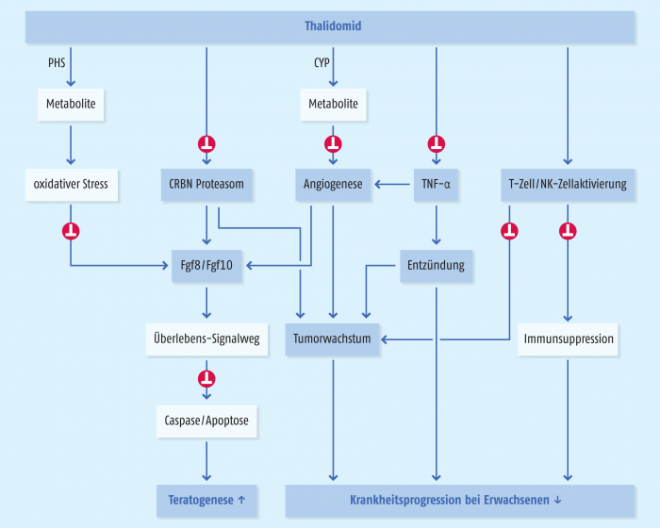
Der genaue Wirkmechanismus der durch Thalidomid hervorgerufenen Schäden ist im Detail nur für die Verkürzung der Gliedmaßen geklärt. Derzeit noch nicht sicher geklärt ist, ob Missbildungen an anderen Organen auf genau denselben Mechanismen beruhen. Ebenso sind die molekularen Vorgänge, die einer krebshemmenden Wirkung von Thalidomid zugrunde liegen, nur bruchstückweise bekannt. Experimentellen Daten zufolge besitzen Thalidomid und dessen Metaboliten das Potenzial, mit verschiedenen zellulären und molekularen Prozessen zu interagieren, die bei der Bildung der Gefäße und der Tumorprogression eine Rolle spielen. Aufgrund der derzeit vorliegenden Daten wurde ein Modell entwickelt, das die embryotoxischen und krebshemmenden Wirkungen sowie deren Überlappungen veranschaulicht.
Einsatz der Immunmodulatoren
EMA-Zulassung
- zur Therapie des multiplen Myeloms (Thalidomid, Lenalidomid, Pomalidomid)
- zur Therapie des Mantelzelllymphoms (Lenalidomid)
- zur Therapie des myelodysplastischen Syndroms (Lenalidomid)
FDA-Zulassung (für Thalidomid)
- zur Therapie des multiplen Myeloms und des ENL (Erythema Nodosum Leprosum, eine besonders schwere Verlaufsform der Lepra)
Off-label-use
- Einsatz bei einigen dermatologischen und malignen Erkrankungen; z. B. bei Lupus erythematosus, Prurigo nodularis, orogenitalen aphthösen Ulzerationen, beim Morbus Behçet (Kleingefäß-Vaskulitis unklarer Ätiologie) sowie beim Prostatakarzinom
Embryotoxische Wirkung
An der Wirkung von Thalidomid sind sowohl Thalidomid als auch seine Metaboliten beteiligt. Durch die Prostaglandin-H-Synthase und Cytochrom-P-450 werden Metaboliten gebildet, die die Bildung reaktiver Sauerstoffspezies induzieren und die Angiogenese hemmen. Thalidomid selbst bindet an Cereblon (CRBN). Cereblon ist Teil des E3-Ligase-Komplexes, der unter anderem für die Selektion von Proteinen und damit für die Aufrechterhaltung der Zellhomöostase verantwortlich ist. Durch die Blockade von Cereblon durch Thalidomid (Destabilisierung des Proteinkomplexes) kommt es zu einer pathogenen Anreicherung von Proteinen, die die Aktivität verschiedener Signalwege, einschließlich der Apoptose, beeinflussen. Oxidativer Stress, Angiogenesehemmung und Ausschalten der Proteasomaktivität durch die Bindung von Thalidomid an Cereblon führen zu einer Downregulation der Fibrinoblasten-Wachstumsfaktoren Fgf8/Fgf10 und davon abhängiger Signalwege (Überlebenssignalwege). Dies führt wiederum zu einer moderaten Apoptose in distalen mesenchymalen Zellen und Zellen der apikalen ektodermalen Randleiste der Extremitätenknospen. Die Folge ist eine Beeinträchtigung der embryonalen Entwicklung der Gliedmaßen (Abb. 1).
Anti-Tumor-Wirkung
Die teratogenen und therapeutischen Wirkungen von Thalidomid überlappen sich, und die Angiogenesehemmung und die Destabilisierung des Cereblon-Proteasoms spielen sowohl bei den unerwünschten, das heißt den embryotoxischen, wie auch bei den erwünschten, nämlich den krebshemmenden Effekten eine Rolle. Der Anti-Tumorwirkung liegen noch weitere Vorgänge zugrunde: Eine TNFα-Downregulation und eine T-Zellaktivierung verringern inflammatorische Prozesse und die Immunsuppression. Die Induktion der Tumorimmunität durch die T-Zell- und NK-Zell-Aktivierung trägt ebenfalls zur Unterdrückung des Tumorwachstums bei.
Krebshemmung ohne Embryotoxizität?
Immunmodulierende Substanzen wie Thalidomid und seine Nachfolger werden heute unter strengen Auflagen zur Therapie bösartiger Erkrankungen des blutbildenden Systems eingesetzt. Des Weiteren ist ein Off-label-use bei zahlreichen weiteren Erkrankungen bekannt (s. Kasten „Einsatz immunmodulierender Substanzen“). Das große Problem hierbei liegt in den embryotoxischen Eigenschaften von Thalidomid und seiner Derivate, was zu neuen Therapie- und Forschungsansätzen führte. Dies sind zum einen die Entwicklung neuer Thalidomid-Derivate ohne embryotoxische Eigenschaften und zum andern der gezielte Einsatz von Thalidomid und seiner Nachfolger. Ersteres scheint schwierig zu sein, da die krebshemmende Wirkung mit der Unterdrückung der Angiogenese einhergeht. Ob teratogene Effekte von anti-inflammatorischen und immunsuppressiven Wirkungen getrennt werden können, ist derzeit noch unklar. Der zweite Weg scheint eher gangbar zu sein: Vor der Gabe immunmodulierender Substanzen werden die Erfolgschancen einer Behandlung abgeschätzt. So haben Beobachtungen gezeigt, dass eine Therapie nur dann anschlug, wenn ein Verlust des Cereblon-Proteinkomplexes erfolgte. Das heißt, nur wenn der Proteinkomplex in vorab entnommenen Tumorzellen nach einer Behandlung mit immunmodulierenden Substanzen verschwindet, ist es sinnvoll, eine Therapie mit Thalidomid und einem seiner Nachfolger einzuleiten. Vielleicht findet dieses Ergebnis der Grundlagenforschung Einzug in den klinischen Alltag. |
Literatur
Knobloch J et al.: The molecular mechansim of thalidomide teratogenicity and implications for modern medicine. Current Molecular Medicine 2017;17:108-117.
Eichner R et al.: Immunomodulatory drugs disrupt the cereblon–CD147– MCT1 axis to exert antitumor activity and teratogenicity, Nat Med. 2016 Jul;22(7):735-43.
Pressemeldung der Technischen Universität München: Funktionsweise von Contergan aufgedeckt. 17. Juni 2016. https://www.mri.tum.de/pressemeldungen/funktionsweise-von-contergan-aufgedeckt.
Celgene Corporation: Proposed Changes To Approved Thalomid Package Insert. https://www.accessdata.fda.gov/drugsatfda_docs/label/2006/021430lbl.pdf.
Behördlich genehmigtes Schulungsmaterial
Seit dem 1. Dezember 2016 gibt es die „Blaue Hand“. Sie weist auf Schulungsmaterial hin, das über die Packungsbeilage und die Fachinformation hinausgehende Informationen bereithält. Ziel ist die Risikominimierung; teilweise dienen die Materialien auch dazu, Anwender in die Verlaufskontrolle ihrer Therapie einzubeziehen oder die Adhärenz zu stärken.
Für Thalidomid, Lenalidomid und Pomalidomid stellt das BfArM Broschüren für Ärzte und Patienten bereit sowie Therapiepässe. Sie gelangen zu den Unterlagen, wenn Sie bei DAZ.online den Webcode in das Suchfeld eingeben.





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.