
- DAZ.online
- DAZ / AZ
- DAZ 52/2018
- Neue Arzneimittel 2018
Neue Arzneimittel
Neue Arzneimittel 2018
Informationen zu neuen Wirkstoffen
In der monatlich erscheinenden Beilage „Neue Arzneimittel“ stellen wir Ihnen alle neuen Wirkstoffe ausführlich vor und ordnen sie in die bestehenden Therapieoptionen ein. Ein Archiv mit allen seit 2000 eingeführten Wirkstoffen finden Sie
auf DAZ.online unter www.deutsche-apotheker-zeitung.de im Bereich „Pharmazie“.
Oder Sie geben einfach in die Suchfunktion auf DAZ.online den Webcode P7YV8 ein und gelangen direkt zur Übersichtsseite der „Neuen Arzneimittel“. Dort können Sie als Abonnent nach Wirkstoffnamen, Handelsbezeichnung, Einführungsjahr oder ATC-Code suchen.
Antidiabetika
Ertugliflozin
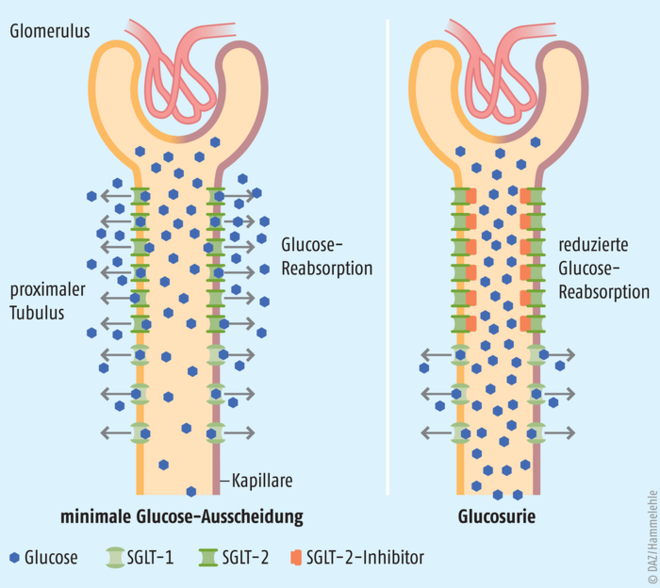
In der fixen Kombination mit dem Dipeptidylpeptidase-4(DPP4)-Inhibitor Sitagliptin wurde der neue Natrium-Glucose-Cotransporter-2(SGLT-2)-Inhibitor Ertugliflozin als Steglujan® eingeführt. Nach Dapagliflozin und Empagliflozin ist es der dritte auf dem deutschen Markt befindliche Vertreter dieser Stoffklasse. Der selektive kompetitive Inhibitor von SGLT-2 bewirkt über einen Insulin-unabhängigen Mechanismus eine Reduktion der Glucose-Rückresorption in den proximalen Nierentubuli. Es kommt zu einer verstärkten Glucose-Ausscheidung mit dem Urin sowie zu einer osmotischen Diurese. Sekundär wird der systolische Blutdruck gesenkt, bei längerer Anwendung kann auch das Körpergewicht reduziert werden. In Kombination mit einem weiteren antidiabetischen Wirkstoff, dem DPP4-Inhibitor Sitagliptin, mit komplementärem Wirkmechanismus wird bei Patienten mit Typ-2-Diabetes die Blutzuckerkontrolle verbessert. Ertugliflozin wird derzeit nur als Analogpräparat eingestuft, da keine Vorteile bezüglich Wirkungen und Nebenwirkungen gegenüber den bereits vorhandenen Substanzen erkennbar sind. Direkte vergleichende Studien liegen nicht vor.
Antidiarrhoika
Telotristatethyl
Das Karzinoid-Syndrom wird durch im Gastrointestinaltrakt lokalisierte neuroendokrine Tumoren ausgelöst, die verstärkt Neurotransmitter freisetzen. Insbesondere durch hohe Konzentrationen an Serotonin treten starke und schmerzhafte Durchfälle auf. Sowohl Telotristatethyl (Xermelo®) als auch sein aktiver Metabolit Telotristat inhibieren die für die Serotonin-Biosynthese erforderlichen L-Tryptophan-Hydroxylasen 1 und 2. Der neue Wirkstoff und sein Metabolit überwinden nicht die Blut-Hirn-Schranke, es werden ausschließlich peripher Enzyme gehemmt. Bei Karzinoid-Syndrom-Patienten kann die durchschnittliche Stuhlfrequenz von 6,1 auf 4,7 pro Tag gesenkt werden. Telotristatethyl gilt als ein gewisser therapeutischer Fortschritt, ob diese relativ geringe Reduktion therapeutisch relevant ist, sollte anhand des individuellen Ansprechens unter Berücksichtigung des persönlichen Leidensdrucks entschieden werden, für einige ist sicherlich eine adäquate Verbesserung der Lebensqualität erzielbar.
Antihämorrhagika
Emicizumab
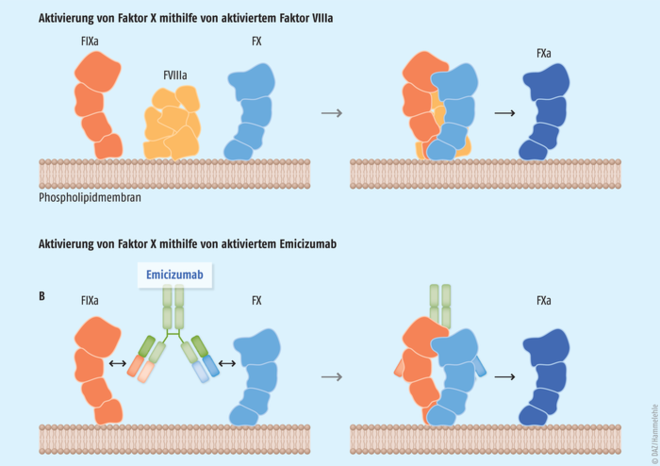
Das Immunglobulin Emicizumab (Hemlibra®) ist zur Langzeitprophylaxe von Blutungsereignissen bei Patienten mit Hämophilie A und Faktor-VIII-Hemmkörpern indiziert. Der bispezifische Antikörper verbindet die Gerinnungsfaktoren IXa und X und ahmt den aktivierten Gerinnungsfaktor VIII nach. Emicizumab gilt als erheblicher Fortschritt. In einer klinischen Studie hat sich Emicizumab gegenüber Placebo und bislang eingesetzten Bypassing-Präparaten mit rekombinantem Faktor VIIa oder aktiviertem Prothrombin-Komplex als signifikant besser wirksam erwiesen. Letztere haben eine geringe Halbwertszeit, sodass häufig Infusionen erforderlich sind. Das gut verträgliche Emicizumab muss nur einmal wöchentlich subkutan injiziert werden, was die Lebensqualität signifikant verbessert.
Rurioctocog alfa pegol
Rurioctocog alfa pegol (Adynovi®) wird bei angeborenem Faktor-VIII-Mangel (Hämophilie A) eingesetzt. Es ist zur Behandlung und Prophylaxe von Blutungen ab einem Alter von zwölf Jahren geeignet. Die Eliminationshalbwertszeit der rekombinant hergestellten pegylierten Substanz ist mit 15 Stunden gegenüber dem entsprechenden nicht pegylierten Faktor-VIII-Präparat Octocog alfa signifikant verlängert. Rurioctocog alfa pegol wird nach derzeitigem Kenntnisstand nicht als relevanter therapeutischer Fortschritt eingestuft. Zwar wird es mit gentechnischen Methoden hergestellt, sodass keine Gefahr der Übertragung von Infektionserkrankungen mehr besteht. Die Produktion mit Zelllinien des Chinesischen Hamsters ist aber mit verstärkten Überempfindlichkeitsreaktionen assoziiert.
Antiinfektiva zur systemischen Gabe, spezifische Immunglobuline
Bezlotoxumab
Zur Vorbeugung eines Rezidivs einer Clostridium-difficile-Infektion wurde der gegen das Clostridium-difficile-Toxin-B gerichtete Antikörper Bezlotoxumab (Zinplava®) eingeführt. Das Immunglobulin wird bei hohem Rekurrenzrisiko eingesetzt und begleitend zu einer Antibiotikatherapie einmalig intravenös appliziert. Der humane, monoklonale IgG1-Antikörper bindet spezifisch an das Zytotoxin B und hemmt somit dessen zerstörende Wirkung auf die Darmschleimhaut. So wird die Oberfläche des Darms bei der Erstinfektion weniger stark beschädigt, eine raschere Regeneration ist möglich. Bezlotoxumab gilt nicht als relevanter Behandlungsfortschritt. Zwar ist die Substanz das erste prophylaktisch einzusetzende Therapeutikum mit völlig neuem Wirkmechanismus. Ob der Behandlungserfolg an die Heilungsraten durch Stuhltransplantationen und Therapieoptionen wie Fidaxomicin heranreicht, bleibt fraglich, es fehlen direkte vergleichende klinische Studien. Ein Nachteil des neuen Antikörpers ist, dass etwa 75% der Patienten auch ohne dieses Prophylaktikum gar kein Clostridium-difficile-Rezidiv erleiden. Es wird also ein Großteil umsonst mit einer vergleichsweise teuren Zubereitung behandelt.
Antineoplastische Mittel
Atezolizumab
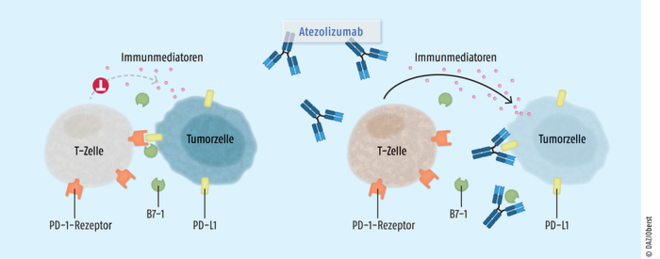
Das Immuntherapeutikum Atezolizumab (Tecentriq®) wird als Monotherapeutikum zur Behandlung von Erwachsenen mit lokal fortgeschrittenem oder metastasiertem Urothel- oder nicht-kleinzelligem Lungenkarzinom (NSCLC) eingesetzt.
Der monoklonale Antikörper richtet sich gegen den Liganden des Checkpoint-Rezeptor PD-1 (Programmed Death Ligand 1, PD-L1). Die Wirkung des im Fc-Teil modifizierten Immunoglobulin-G1(IgG1)-Antikörpers beruht auf einer hochselektiven Bindung an PD-L1 und den Kofaktor B7-1. Als Folge werden Interaktionen mit dem PD-1-Rezeptor unterbunden. Die zytotoxische Aktivität und Proliferation von T-Zellen sowie deren Zytokin-Produktion wird wiederhergestellt und die antitumorale Immunantwort reaktiviert. Der Checkpoint-Inhibitor Atezolizumab wurde fast zeitgleich mit dem weiteren PD-L1-Antikörper Avelumab eingeführt. Für die Behandlung des Urothelkarzinoms wird Atezolizumab nicht als therapeutischer Fortschritt eingestuft. Direkte vergleichende Untersuchungen mit den Checkpoint-Inhibitoren Nivolumab und Pembrolizumab, die nicht gegen PD-1-Liganden, sondern gegen den zugehörigen Rezeptor gerichtet sind, fehlen aber.
Avelumab
Auch der monoklonale Antikörper Avelumab (Bavencio®) richtet sich gegen den programmierten Zelltod-Liganden 1 (PD-L1) des entsprechenden Checkpoint-Rezeptors. Er wird zur Behandlung von Erwachsenen mit metastasiertem Merkelzell-Karzinom eingesetzt. Avelumab gilt als bedeutender therapeutischer Fortschritt bei diesem seltenen Hauttumor. In klinischen Studien bewirkte der Checkpoint-Inhibitor ein gutes Ansprechen, teilweise mit kompletten Remissionen, sowie eine deutliche Verlängerung des progressionsfreien und des Gesamtüberlebens.
Gemtuzumab
Gemtuzumab Ozogamicin (Mylotarg®) ist ein Immunkonjugat aus dem zytotoxischen Wirkstoff N-Acetyl-Gamma-Calicheamicin-Dimethylhydrazid und einem gegen das CD33-Antigen gerichteten monoklonalen Antikörper. Der Wirkstoff wird als Krebsimmuntherapie zur Behandlung einer CD33-positiven akuten myeloischen Leukämie (AML) eingesetzt. Sobald eine Bindung von Gemtuzumab Ozogamicin an CD33 stattfindet, kommt es zur Bildung eines Komplexes, der in die Zellen aufgenommen wird. Dort wird das hochtoxische Calicheamicin durch hydrolytische Spaltung freigesetzt und induziert DNA-Doppelstrangbrüche, die zum Zellzyklus-Arrest und so zum apoptotischen Zelltod der leukämischen Blasten führen. Da die Betroffenen mit einer akuten myeloischen Leukämie meist innerhalb weniger Wochen bis Monate an ihrer schnell voranschreitenden Erkrankung versterben, gilt Gemtuzumab Ozogamicin als ein relevanter therapeutischer Fortschritt: Die Patienten gewinnen etwa acht Monate an Lebenszeit.
Genetisch verändertes T-Zell-Präparat
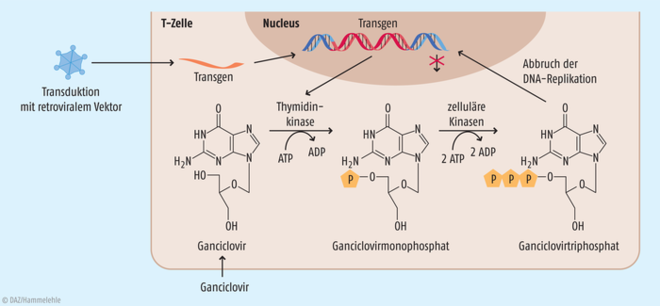
Für Patienten, die aufgrund hämatologischer Tumore eine haploidentische hämatopoetische Stammzelltransplantation erhalten, wurde das allogene T-Zell-Präparat (Zalmoxis®) eingeführt. Das patientenspezifisch hergestellte Gentherapeutikum unterstützt die Rekonstitution des Immunsystems und bedeutet für Patienten, bei denen nicht rechtzeitig ein passender Spender zur Verfügung steht, einen relevanten therapeutischen Fortschritt. Mit einer völlig neuartigen Methode werden die T-Zellen zunächst aus Spenderblut abgetrennt und anschließend mit einem genetischen Vektor so umprogrammiert, dass sich das Immunsystem des Patienten mithilfe der zusätzlichen T-Zellen rasch erholt (siehe Abb.). Eine zusätzliche Gabe von Immunsuppressiva ist nicht erforderlich und es können auch weniger gut geeignete Spender genommen werden. Der Therapieansatz ist absolut innovativ und für die Betroffenen häufig lebensrettend. Allerdings liegt der Preis von Zalmoxis® bei über 200.000 Euro.
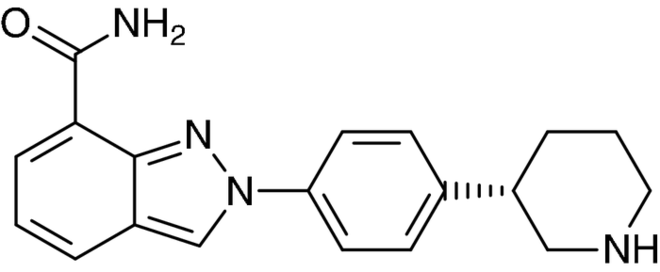
Niraparib
Für Patientinnen mit einem Rezidiv eines
Platin-sensiblen Karzinoms der Ovarien, der Tuben oder mit primärer
Peritonealkarzinose wurde der Inhibitor der humanen
Poly(ADP-Ribose)-Polymerase-Enzyme (PARP 1 und 2) Niraparib (Zejula®)
eingeführt. Das PARP-Enzym dient zur Reparatur von
DNA-Einzelstrangbrüchen. Niraparib bindet an das aktive Zentrum des
DNA-assoziierten PARP-Enzyms, es kommt zu DNA-Doppelstrangbrüchen, die
zu Apoptose und Zelltod führen. So wird verhindert, dass Tumorzellen
einen Zytostatika-induzierten DNA-Schaden reparieren. Niraparib gilt als
ein gewisser therapeutischer Fortschritt, es verlängert signifikant das
progressionsfreie Überleben. Nach Olaparib ist Niraparib der zweite
Vertreter seiner Wirkstoffklasse, muss aber nur einmal täglich
eingenommen werden.
Sonidegib
Für Erwachsene mit lokal fortgeschrittenem Basalzellkarzinom steht der Smoothened-Rezeptor-Antagonist Sonidegib (Odomzo®) zur Verfügung. Der oral applizierbare antitumorale Wirkstoff hemmt den Hedgehog-Signalweg und wird als Zweitlinien-Therapeutikum eingesetzt. Sonidegib bewirkt durch Bindung an G-Protein-gekoppelte, rezeptorartige Membranproteine eine Hemmung des Signalwegs, was wiederum zu einer verminderten Transkription von wachstumsfördernden Genen führt. Der neue Wirkstoff wirkt antitumoral und antiproliferativ und führt bei Patienten mit fortgeschrittenem Basalzellkarzinom zu einem deutlichen Rückgang der Tumoren. In dieser Indikation gilt bislang der 2013 zugelassene Inhibitor des Hedgehog-Signalwegs Vismodegib als Standardtherapeutikum, Sonidegib ist allenfalls als moderater therapeutischer Fortschritt anzusehen.
Tisagenlecleucel
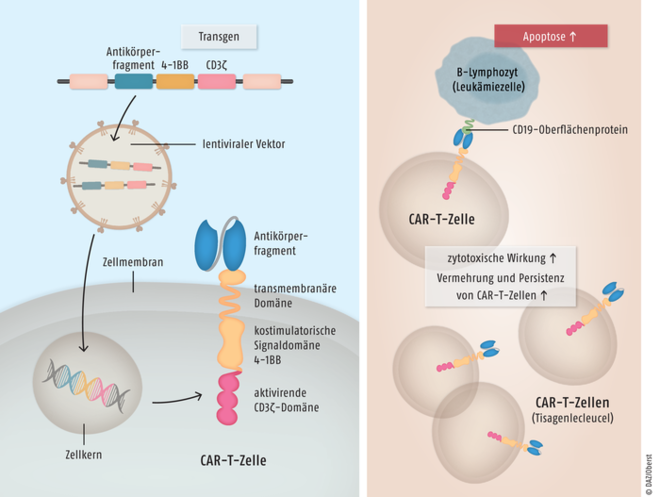
Für Patienten mit refraktärer oder rezidivierter akuter lymphatischer B-Zell-Leukämie (ALL) und mit rezidiviertem oder refraktärem diffus großzelligem B-Zell-Lymphom wurde Tisagenlecleucel (Kymriah®) eingeführt, eine für jeden Patienten individuell hergestellte „lebende“ Immunzell-Therapie auf Basis autologer T-Zellen. Die T-Zellen werden ex vivo mithilfe eines Vektors so umprogrammiert, dass sich ihre zytotoxische Aktivität auf B-Zellen mit dem spezifischen Oberflächenprotein CD19 richtet. Tisagenlecleucel gilt als effektive und innovative Behandlungsmethode und wird als außerordentlicher therapeutischer Fortschritt eingeschätzt. Die personalisierte Krebstherapie ist eine Kombination aus zytotoxischer Therapie und Gentherapie. Sie wird nur einmalig appliziert und verbleibt über längere Zeit im Organismus. In der zulassungsrelevanten klinischen Studie konnten sehr gute Erfolge erzielt werden. Bei mehr als 80% der Teilnehmer wurde durch das CAR-T-Zell-Präparat ein vollständiges Ansprechen erreicht. Dies übertrifft deutlich die bislang durch Standardmethoden erzielten Resultate. Wie lange eine Remission durch die umprogrammierten T-Zellen anhält, muss in längerfristigen Studien geklärt werden. Neben dem hohen Preis – in den USA kostet eine Therapie derzeit 475.000 US-Dollar – sind die mit Tisagenlecleucel assoziierten, teilweise lebensbedrohlichen Nebenwirkungen zu beachten.
Tivozanib
Tivozanib (Fotivda®) ist ein potenter und selektiver Inhibitor von drei vaskulären endothelialen Wachstumsfaktorrezeptoren (VEGFR). Die Substanz wird beim fortgeschrittenen Nierenzellkarzinom als Erst- und Zweitlinien-Therapeutikum eingesetzt. Es werden die durch verschiedene VEGF-Liganden induzierten biochemischen und biologischen Reaktionen gehemmt, einschließlich Rezeptor-Phosphorylierung sowie die Proliferation humaner Endothelzellen. In geringerem Ausmaß ist auch die ebenfalls Proliferations-fördernde Tyrosinkinase c-KIT von der Inhibition betroffen. Als Folge werden Wachstum und Metabolisierung von Tumoren reduziert. Tivozanib gilt allenfalls als moderater Fortschritt, denn mit Sunitinib und Pazopanib sind bereits VEGFR-Inhibitoren verfügbar.
Mittel für das alimentäre System und den Stoffwechsel
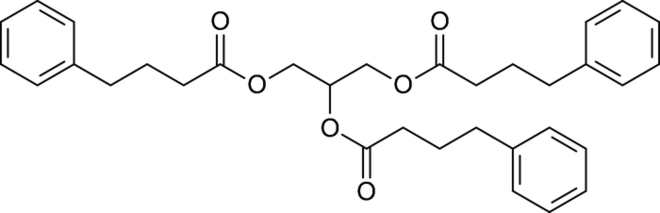
Glycerolphenylbutyrat
Verschiedene Harnstoffzyklusstörungen (urea cycle disorders, UCD), die nicht ausreichend auf eine diätetische Eiweißrestriktion und/oder Aminosäuresubstitution ansprechen, können nun mit Glycerolphenylbutyrat (Ravicti®) als Add-on-Therapeutikum behandelt werden. Die Stickstoff-bindende Substanz ist sowohl bei Erwachsenen als auch bei Kindern einsetzbar und verhindert das Auftreten von schädlichen Hyperammonämien. Patienten mit völlig fehlender Harnstoffsynthese-Kapazität erleiden meist bereits in den ersten Lebenstagen ein hyperammonämisches Koma, das trotz Behandlung mit einer 50%igen Mortalität assoziiert ist. Glycerolphenylbutyrat ist ein alternatives Vehikel für die Ausscheidung von Stickstoff wird als moderater therapeutischer Fortschritt eingeschätzt.
Mittel bei obstruktiven Atemwegserkrankungen
Benralizumab
Der gegen den Interleukin-5α-Rezeptor (IL-5Rα) gerichtete monoklonale Antikörper Benralizumab (Fasenra®) kann bei schwerem eosinophilem Asthma bronchiale als Add-on-Therapeutikum zu oralen und inhalativen Corticosteroiden sowie β2-Sympathomimetika eingesetzt werden. Benralizumab bindet als humanisierter, monoklonaler Immunglobulin-G1-kappa(IgG1κ)-Antikörper hochaffin an die α-Untereinheit des Interleukin-5-Rezeptors, der auf der Oberfläche von Eosinophilen und auch von Basophilen exprimiert wird. Aufgrund eines fehlenden Fucose-Moleküls im Fc-Bereich bindet er zudem mit hoher Affinität an FcγRIII-Rezeptoren auf natürlichen Killerzellen und löst die Apoptose von Eosinophilen und Basophilen aus. Es ist weltweit der erste monoklonale Antikörper, der über eine Bindung an die α-Untereinheit des IL-5-Rezeptors auf Eosinophilen die nachgeschaltete Signalkaskade inhibiert und gleichzeitig den Zelltod der an der Pathogenese von Asthma beteiligten eosinophilen Granulozyten auslöst. Der Antikörper muss nur alle acht Wochen subkutan appliziert werden. Benralizumab gilt als ein moderater Fortschritt bei der Add-on-Behandlung von eosinophilem Asthma bronchiale.
Metreleptin
Patienten mit generalisierter oder partieller Lipodystrophie und einer hiermit assoziierten Leptin-Defizienz können mit Metreleptin (Myalepta®) eine Substitutionstherapie erhalten. Durch das Derivat des körpereigenen Polypeptidhormons Leptin werden Glucose- und Fettstoffwechselstörungen reduziert und zudem das Hungergefühl gedämpft. Somit können bei den Betroffenen mitunter lebensbedrohliche Folgeerkrankungen von Leber, Nieren, Muskeln und Immunsystem zumindest gemildert werden. Das Leptin-Analogon Metreleptin hat einen innovativen Behandlungsansatz und gilt als erste kausale Therapieoption als ein bedeutender therapeutischer Fortschritt.
Velmanase alfa
Für Patienten mit leichter bis mittelschwerer Alpha-Mannosidose, einer genetisch bedingten lysosomalen Speicherkrankheit, steht mit Velmanase alfa (Lamzede®) eine Enzymersatztherapie zur Verfügung. Mithilfe dieser rekombinant hergestellten Form des humanen Enzyms Alpha-Mannosidase können nicht-neurologische Manifestationen der Erkrankung behandelt und deren Progression verlangsamt werden. Das Orphan Drug wird daher als therapeutischer Fortschritt angesehen. Allerdings ist es weder möglich, irreversible Schädigungen rückgängig zu machen noch neurologische Schäden oder intellektuelle Defizite zu verhindern, da Velmanase alfa nicht die Blut-Hirn-Schranke überwindet.
Immunsuppressiva
Guselkumab
Für Erwachsene mit mittelschwerer bis schwerer Plaque-Psoriasis steht mit dem Interleukin-23-Inhibitor Guselkumab (Tremfya®) ein neues Erstlinien-Therapeutikum zur Verfügung. Der subkutan applizierbare, humanisierte monoklonale IgG1λ-Antikörper wirkt über eine Inhibierung des IL-23-Zytokinwegs entzündungshemmend und immunsuppressiv. Bei Plaque-Psoriasis wird er als ein gewisser therapeutischer Fortschritt eingeschätzt. In klinischen Studien erwies sich die Substanz bei guter Verträglichkeit dem TNF-α-Blocker Adalimumab als überlegen. Zudem profitierte ein größerer Anteil an Patienten, die mit dem IL-12/23-Antikörper Ustekinumab nicht zufriedenstellend therapiert werden konnte.
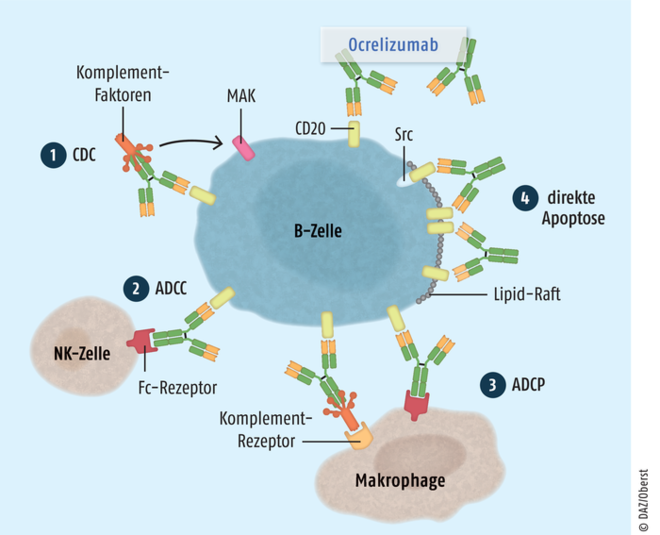
Ocrelizumab
Der monoklonale humanisierte CD20-Antikörper Ocrelizumab (Ocrevus®) ist zur Behandlung der aktiven schubförmigen sowie der frühen primär progredienten multiplen Sklerose indiziert. Über eine Bindung an die Oberfläche CD20-exprimierender B-Zellen führt Ocrelizumab mittels Antikörper-abhängiger zellulärer Phagozytose, Antikörper-abhängiger zellulärer Zytotoxizität, komplementabhängiger Zytotoxizität und Apoptose eine Depletion von B-Zellen herbei. Obwohl Ocrelizumab nur etwa halbjährlich appliziert wird, hält die B-Zell-Depletion im Verlauf des gesamten Intervalls an. Wichtige Funktionen des Immunsystems wie die Fähigkeit der B-Zellen-Rekonstitution und die bestehende humorale Immunität bleiben erhalten. Ocrelizumab ist der erste Wirkstoff, der für die frühe primär progrediente multiple Sklerose indiziert ist, und stellt einen erheblichen therapeutischen Fortschritt dar. Das Wirkprinzip ist allerdings nicht neu. Die CD20-Antikörper Rituximab und Obinutuzumab sind zwar derzeit nicht bei MS zugelassen, aber Rituximab wird z. B. bereits als Off-label-Therapeutikum bei schweren Erkrankungsformen eingesetzt.
Ophthalmika
Cenegermin
Für Erwachsene mit neurotropher Keratitis wurde zur topischen Therapie der rekombinante humane Nervenwachstumsfaktor Cenegermin (Oxervate®) eingeführt. Die seltene degenerative Hornhauterkrankung wird durch eine Beschädigung des Nervus trigeminus verursacht. Cenegermin führt nach achtwöchiger Therapie bei mehr als 70% der unter Sensibilitätsstörungen, epithelialen Defekten und Geschwüren der Hornhaut leidenden Patienten zu einer Heilung der Hornhautschäden. Cenegermin gilt als erheblicher therapeutischer Fortschritt, es ist die erste pharmakologische Behandlungsoption für diese Patienten. In klinischen Studien konnte bei 70 bis 75% der Erkrankten eine vollständige Heilung der Epithelschäden und Ulzera auf der Hornhaut erreicht werden.
Psycholeptika
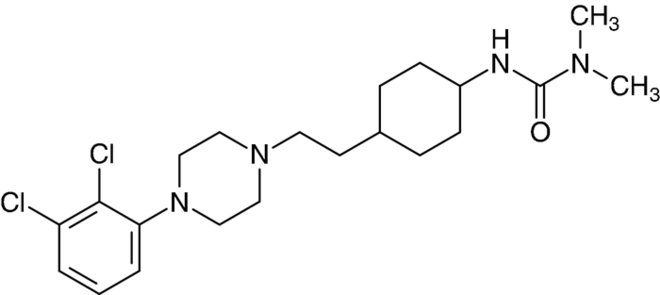
Cariprazin
Zur Therapie der Schizophrenie wurde das atypische Antipsychotikum Cariprazin (Reagila®) eingeführt. Die antipsychotische Wirkung von Cariprazin und seinen beiden pharmakodynamisch aktiven Hauptmetaboliten Desmethylcariprazin und Didesmethylcariprazin wird auf eine Kombination aus partialagonistischen Aktivitäten an dopaminergen D3- und D2-Rezeptoren sowie serotoninergen 5-HT1A-Rezeptoren zurückgeführt, ebenso auf einen Antagonismus an 5-HT2B-, 5-HT2A-Rezeptoren und histaminergen H1-Rezeptoren. Die Substanz mildert insbesondere auch NegativSymptome der Erkrankung (z. B. Gefühlsverflachung, Antriebslosigkeit, Sprachverarmung sowie Aufmerksamkeits- und Gedächtnisstörungen). Die Negativ-Symptome führen zu einem relevanten Verlust an Lebensqualität und bislang gibt es dagegen keine spezifischen Pharmaka. Daher gilt das neue atypische Antipsychotikum als ein gewisser therapeutischer Fortschritt.
Antivirale Mittel
Bictegravir
Der neue Integrase-Strangtransfer-Inhibitor Bictegravir kann zur Behandlung von Infektionen mit dem humanen Immundefizienz-Virus 1 (HIV-1) eingesetzt werden. Die Substanz ist im Präparat Biktarvy® in fixer Kombination mit Emtricitabin und Tenofoviralafenamid enthalten und wird als mäßiger therapeutischer Fortschritt eingeschätzt. Die Zubereitung muss nur einmal täglich appliziert werden, ein zusätzlicher Booster ist nicht erforderlich. Bictegravir bindet an das aktive Zentrum der HIV-1-Integrase und hemmt den Strangtransfer und den Einbau des retroviralen Erbguts in die DNA der Wirtszelle. Die kombiniert eingesetzten antiviralen Wirkstoffe Emtricitabin und Tenofoviralafenamid wirken synergistisch.
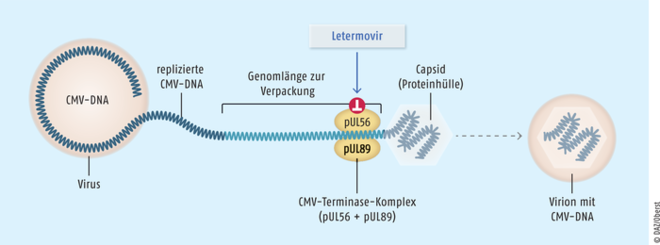
Letermovir
Mit dem Inhibitor des Cytomegalie-Virus(CMV)-DNA-Terminase-Komplexes Letermovir (Prevymis®) wurde ein bedeutender therapeutischer Fortschritt zur Prophylaxe einer CMVReaktivierung bzw. -Erkrankung eingeführt. Das nicht-nucleosidische Virustatikum wird bei CMV-seropositiven Patienten angewendet, die eine allogene hämatopoetische Stammzelltransplantation erhalten haben. Bei diesen Personen ist das Immunsystem geschwächt und es kommt häufig zu einer Reaktivierung einer vorangegangenen Primärinfektion mit dem Cytomegalie-Virus bis hin zu lebensbedrohlichen Infektionen. Das völlig neuartige Wirkprinzip ist die Hemmung des CMV-DNA-Terminase-Komplexes. Letermovir wird prophylaktisch eingesetzt und ist seit 15 Jahren das erste neue für diese Indikation zugelassene Medikament.
Voxilaprevir
Der NS3/4A-Serinprotease-Inhibitor Voxilaprevir wird im Präparat Vosevi®
in fixer Kombination mit den Hepatitis-C-Virus(HCV)-Therapeutika
Sofosbuvir und Velpatasvir zur Behandlung der chronischen Hepatitis C
eingesetzt. Das neue Präparat ist bei allen HCV-Genotypen wirksam. Eine
Kombination mit weiteren HCV-Therapeutika wie Ribavirin ist nicht
erforderlich. Voxilaprevir ist mittlerweile der siebte Inhibitor der
HCV-NS3/4A-Serinprotease. Die Substanz wird derzeit ausschließlich in
fixer Kombination mit dem RNA-Polymerase-NS5B-Inhibitor Sofosbuvir und
dem NS5A-Inhibitor Velpatasvir als pangenotypisches HCV-Therapeutikum
angewandt und kann durchaus als gewisse therapeutische Innovation
eingeordnet werden.
Dermatika
Dupilumab
Der IgG4-Antikörper Dupilumab (Dupixent®) ist zur Behandlung der mittelschweren bis schweren atopischen Dermatitis indiziert und wird in zweiwöchigen Abständen subkutan appliziert. Der Hemmstoff der Interleukin-4- und -13-Signalwege wirkt insgesamt entzündungshemmend und selektiv immunsuppressiv und gilt als ein relevanter Fortschritt. Der Antikörper ist der erste, speziell für die atopische Dermatitis zugelassene systemische Wirkstoff mit einem völlig neuen Wirkmechanismus. Über eine Hemmung der Interleukin-4- und Interleukin-13-Signalwege führt er zu einer für die Patienten bedeutenden signifikanten Verbesserung von Hautbild, Pruritus sowie der erkrankungsbedingten psychischen Störungen, die Lebens- und Schlafqualität konnte anhaltend verbessert werden. Es wäre wünschenswert, wenn die Substanz auch für die Behandlung von Kindern und Jugendlichen zugelassen würde, entsprechende Studien laufen bereits. Ebenso wird derzeit der Nutzen bei ebenfalls durch die Zytokine IL-4 und IL-13 begünstigten Erkrankungen (persistierendem, unkontrolliertem Asthma bronchiale, Nasenpolypen und eosinophiler Ösophagitis) geprüft.
Urologika
Desfesoterodin
Für Erwachsene mit erhöhter Harnfrequenz, imperativem Harndrang und/oder Dranginkontinenz, wie sie bei dem Syndrom der überaktiven Harnblase vorkommen, wurde ein neuer muscarinerger Antagonist eingeführt. Desfesoterodin (Tovedeso®) ist der aktive Metabolit der bereits seit Jahren für dieselbe Indikation eingesetzten Arzneistoffe Fesoterodin und Tolterodin. Der kompetitive, relativ selektive M3-Muscarinrezeptor-Antagonist wird nicht als therapeutischer Fortschritt eingeschätzt. Er bewirkt wie andere Antimuskarinika eine Reduktion der Inkontinenzereignisse und der Anzahl der Miktionen sowie einen Anstieg des Miktionsvolumens. Aufgrund der großen Übereinstimmungen mit dem seit zehn Jahren im Handel befindlichen zugehörigen Prodrugs Fesoterodin wurde vollständig auf die Durchführung von Zulassungsstudien verzichtet. Auch die Einnahmemodalitäten der beiden Präparate sind identisch.
Arzneimittel zur Behandlung von Knochenerkrankungen
Burosumab
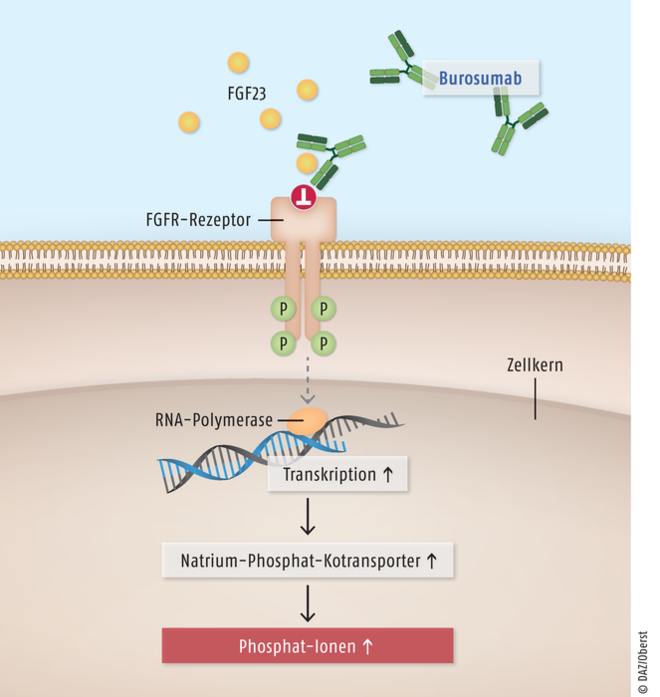
Burosumab (Crysvita®) ist ein gegen den Fibroblasten-Wachstumsfaktor 23 gerichteter monoklonaler Antikörper. Er ist für die Behandlung von Kindern ab einem Jahr und Jugendlichen in der Skelettwachstumsphase indiziert, die unter X-chromosomaler Hypophosphatämie (XLH) leiden.
Durch die Bindung an den Fibroblasten-Wachstumsfaktor 23 wird dessen Aktivität blockiert, sodass in den Nieren die Phosphat-Rückresorption gesteigert wird. So können bei Patienten mit X-chromosomaler Hypophosphatämie die Serumphosphat-Werte normalisiert und rachitische Schädigungen und Deformationen der Knochen und Zähne sowie Wachstumsprobleme reduziert werden. Burosumab wird als relevanter therapeutischer Fortschritt mit einem völlig neuen Wirkprinzip bei der X-chromosomal dominant vererbten Hypophosphatämie eingesetzt. Es besteht zum ersten Mal eine kausale Behandlungsmöglichkeit, da der im Übermaß biosynthetisierte FGF23 unmittelbar abgefangen wird, noch bevor es zu einer Veränderung des Phosphat-Transportsystems am proximalen Tubulus der Nieren kommt.
Arzneimittel zur Behandlung der Hyperkaliämie und Hyperphosphatämie
Patiromer
Das nicht aus dem Gastrointestinaltrakt resorbierbare Kationen-Austauschpolymer Patiromer (Veltassa®) ist für die orale Behandlung von Erwachsenen mit Hyperkaliämie vorgesehen. Es bindet Kalium-Ionen im Lumen des Gastrointestinaltraktes und wird zusammen mit den Fäzes ausgeschieden. Ursachen einer Hyperkaliämie können eine eingeschränkte Nierenfunktion, Hypertonie, Diabetes mellitus und Herzinsuffizienz, aber auch die Einnahme von Renin-Angiotensin-Aldosteron-System(RAAS)-Hemmern wie Inhibitoren des Angiotensin Converting Enzyms (ACE-Inhibitoren) sowie von kaliumsparenden Diuretika sein. Eine Hyperkaliämie kann mit lebensbedrohlichen kardialen Komplikationen einhergehen. Das Kationen-Austauschpolymer Patiromer enthält als Gegenion einen Calciumsorbitol-Komplex, der im Darm gegen Kalium-Ionen ausgetauscht und dann mit den Fäzes ausgeschieden wird. Als Folge sinkt die Kalium-Konzentration im Gastrointestinallumen, und es kommt gleichzeitig zu einer Erhöhung der renalen Calcium-Exkretion. Bei Patienten mit Hyperkaliämie wird eine signifikante Verringerung des Serumkalium-Spiegels erreicht. Patiromer kann als deutlicher Fortschritt eingeordnet werden. Anders als bei dem Kationenaustauscher Natriumpolystyrolsulfonat besteht kein Risiko für eine Hypernatriämie. Durch das Langzeittherapeutikum können viele Herz- oder Niereninsuffizienz-Patienten weiterhin mit RAAS-Inhibitoren behandelt werden, deren Therapie sonst wegen der Hyperkaliämie-Gefahr abgesetzt oder ständig unterbrochen werden müsste.
Varicella-Zoster-Impfstoffe
Impfstoff gegen Gürtelrose
Erwachsene im Alter von 50 Jahren und älter, die Kontakt mit dem Varicella-Zoster-Virus hatten und bereits entsprechende Antikörper aufweisen, können nun eine Impfung mit einem Varicella-Zoster-Virus-Glykoprotein-E-Antigen (Shingrix®) erhalten. Auf diese Weise wird einer Reaktivierung einer Varicella-Zoster-Virus-Infektion (Gürtelrose) vorgebeugt. Den Betroffenen bleiben durch den Subunit-Impfstoff, der kleine Mengen von viralen Oberflächenantigenen enthält, möglicherweise langanhaltende postzosterische Neuralgien und schwere, unter Umständen lebensbedrohliche Erkrankungsverläufe erspart. Der prophylaktisch einzusetzende Totimpfstoff Shingrix® stellt einen erheblichen therapeutischen Fortschritt dar. In placebokontrollierten Studien konnte eine Gürtelrose bei mehr als 90% der Personen verhindert werden. Die Erfolgsquote ist deutlich höher als bei dem bereits seit längerer Zeit eingesetzten Zoster-Impfstoff Zostavax®.
Leberfunktionstest
Methacetin
Das Diagnostikum Methacetin (LiMAxetin®) kann prä- und postoperativ zur Prognose und Überwachung der Leberfunktionskapazität im Rahmen von Leberresektionen und -transplantationen angewendet werden. Der nicht-invasive, LiMAx® genannte Atemtest auf der Basis von 13C-markiertem Methacetin dient als Orientierungshilfe für Ärzte und verbessert die Patientensicherheit und kann als relevanter klinischer Fortschritt eingestuft werden. Das Verfahren misst indirekt die Aktivität des nur in gesundem Lebergewebe exprimierten Enzyms CYP1A2 und ist daher nicht nur hochspezifisch, sondern auch innovativ. Er ermöglicht es über eine sehr kurzfristige und flexible Messung Patienten mit geringem Risiko und ausreichender Funktion der Restleber zu identifizieren, um sie direkt aus dem Aufwachraum auf die Normalstation verlegen zu können.
Sensibilisator für die photodynamische/Radio-Therapie
Padeliporfin
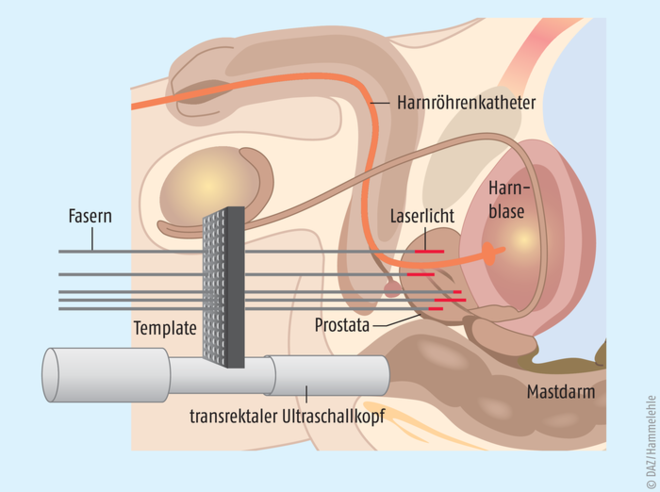
Männliche Patienten mit bislang unbehandeltem einseitigem Niedrigrisiko-Adenokarzinom der Prostata und einer Lebenserwartung von mindestens zehn Jahren können nun mit Padeliporfin (Tookad®) behandelt werden. Die Substanz wird als Einzeldosis intravenös verabreicht und als Photosensitizer im Rahmen einer gezielten vaskulären photodynamischen Therapie (VPT) eingesetzt. Nach intravenöser Applikation von Padeliporfin wird das Tumorareal mit dem darin befindlichen Wirkstoff mit Laserlicht der Wellenlänge 753 nm bestrahlt. Dies führt zur Auslösung einer Reaktionskaskade, bei der zunächst über die Bildung von Sauerstoffradikalen eine lokale Hypoxie ausgelöst wird. Dies wiederum bewirkt eine Freisetzung von kurzfristig vasodilatatorisch wirkenden Stickoxid-Radikalen. Im weiteren Verlauf kommt es allerdings rasch zu einer reflektorischen Freisetzung des Vasokonstriktors Endothelin-1, woraufhin sich die Tumor-versorgenden Blutgefäße stark verengen, sodass durch aggregierende Erythrozyten eine Okklusion der Gefäße resultiert. Bei Patienten mit lokalem Prostatakarzinom konnte die Tumorprogression verlangsamt werden, bis hin zum völligen Verschwinden des Tumors. Die fokale vaskuläre photodynamische Therapie mit dem Photosensitizer Padeliporfin gilt als relevanter Fortschritt, denn durch das gewebeschonende Verfahren können bereits sehr kleine Tumoren gezielt bekämpft werden.
Radiodiagnostika
Tilmanocept
Mit Technetium-99m radioaktiv markiertes Tilmanocept (Lymphoseek®) wird bei Erwachsenen mit Mammakarzinom, Melanom oder lokalisiertem Plattenepithelkarzinom der Mundhöhle zur prä- oder intraoperativen Detektion von Wächterlymphknoten im Lymphabflussgebiet eingesetzt (sogenanntes Wächterlymphknoten-Mapping). Die externe Bildgebung erfolgt mithilfe eines Gammastrahlendetektionsgeräts. Für eine gezielte Behandlung metastasierender Tumore ist es wichtig, die besonders gefährdeten tumornahen Lymphknoten zuverlässig zu identifizieren. Das Diagnostikum Tilmanocept wird mit radioaktivem Technetium-99m aktiviert und in den unmittelbaren Bereich des Tumors injiziert. Das Mannose-haltige Makromolekül gelangt aufgrund seiner geringen Größe rasch auf demselben Weg wie etwaiges Tumorgewebe über die Lymphbahnen in die stark Makrophagen-haltigen Wächterlymphknoten. Es bindet mit hoher Affinität an CD206-Mannoserezeptoren auf der Oberfläche der Makrophagen und reichert sich dadurch an. So können gefährdeten Wächterlymphknoten gezielt entfernt werden. Das neue Diagnostikum gilt als relevanter Fortschritt, es ist derzeit der einzige Radiotracer, der zielgerichtet an in Wächterlymphknoten in hoher Zahl vorkommende Rezeptoren bindet.
Antisense-Nucleotide
Inotersen
Die hereditäre Transthyretin(TTR)-vermittelte Amyloidose (hATTR) ist durch eine Anreicherung von Amyloidproteinen in Organen und Nervengewebe gekennzeichnet. Transthyretin ist ein in der Leber und im Plexus choroideus gebildetes, körpereigenes Protein, das für den Transport des Schilddrüsenhormons Thyroxin verantwortlich ist. Es ist auch ein Trägerprotein für das Retinol-bindende Protein 4, welches seinerseits Retinol (Vitamin A) im Blut transportiert. Bei Patienten mit hereditärer Transthyretin-vermittelter Amyloidose liegt dieses Protein aufgrund einer Genmutation in instabiler Form vor. Die modifizierten Transthyretin-Amyloidproteine zerfallen und bilden irreversible Ablagerungen im Nervensystem, Herzen, Knochenmark sowie in den Augen, Nieren und der Schilddrüse. Es kommt zu Polyneuropathien mit Lähmungen und Krämpfen, Kardiomyopathien bis zum Herzversagen, Nierenfunktionsstörungen und Demenz. Die Erkrankung führt innerhalb eines Zeitraums von 2,5 bis 15 Jahren zum Tod. Inotersen (Tegsedi®), ein 2‘-O-2-Methoxyethyl-Phosphorthioat-Antisense-Oligonucleotid, bindet im Verlauf der Transthyretin-Biosynthese selektiv an mutierte und normale Wildtyp-TTR-Messenger-RNA. Dadurch wird die Transthyretin-Bildung um mehr als die Hälfte reduziert und bei hATTR-Patienten eine Verbesserung der Symptomatik erreicht. Inotersen kann als großer therapeutischer Fortschritt, zumindest für Polyneuropathie-Stadien 1 und 2 dieser lebensbedrohenden Erkrankung angesehen werden. |
Substanz |
Handelsname |
Gruppe |
Hersteller/Vertrieb |
Einführungsdatum |
NA Nr.-Jahr |
|---|---|---|---|---|---|
Atezolizumab |
Tecentriq |
antineoplastische Arzneimittel, monoklonale Antikörper |
Roche Pharma AG |
15. Oktober 2017 |
2-18 |
Avelumab |
Bavencio®
|
andere antineoplastische Mittel, monoklonale Antikörper |
Merck Serono GmbH |
15. Oktober 2017 |
1-18 |
Benralizumab |
Fasenra®
|
Mittel bei obstruktiven Atemwegserkrankungen, andere Mittel bei obstruktiven Atemwegserkrankungen zur systemischen Anwendung |
AstraZeneca GmbH |
15. Februar 2018 |
6-18 |
Bezlotoxumab |
Zinplava®
|
Antiinfektiva für systemische Gabe, spezifische Immunglobuline |
MSD Sharp & Dohme GmbH |
1. April 2018 |
7-18 |
Bictegravir |
Biktarvy®
(Fixkombination mit Emtricitabin und Tenofoviralafenamid)
|
antivirale Mittel zur systemischen Anwendung; antivirale Mittel zur Behandlung von HIV-Infektionen, Kombinationen |
Gilead Sciences GmbH |
15. Juli 2018 |
10-18 |
Burosumab |
Crysvita®
|
Arzneimittel zur Behandlung von Knochenerkrankungen, andere Arzneimittel mit Einfluss auf die Knochenstruktur und Mineralisierung |
Kyowa Kirin GmbH |
15. April 2018 |
7-18 |
Cariprazin |
Reagila®
|
Psycholeptika,andere Antipsychotika |
Recordati Pharma GmbH |
15. April 2018 |
7-18 |
Cenegermin |
Oxervate®
|
andere Ophthalmika |
Dompe Farmaceutici S.p.A., Milano (I) |
15. November 2017 |
2-18 |
Desfesoterodin |
Tovedeso®
|
Urologika, urologische Spasmolytika |
ratiopharm GmbH |
1. März 2018 |
6-18 |
Dupilumab |
Dupixent®
|
andere Dermatika, Mittel zur Behandlung der Dermatitis, exklusiv Corticosteroide |
Sanofi-Aventis GmbH |
1. Dezember 2017 |
3-18 |
Emicizumab |
Hemlibra®
|
Antihämorrhagika, andere systemische Hämostatika |
Roche Pharma AG |
1. April 2018 |
6-18 |
Ertugliflozin |
Steglujan®(Fixkombination aus Ertugliflozin und Sitagliptin) |
Antidiabetika, Kombinationen mit oralen Antidiabetika |
MSD Sharp & Dohme GmbH |
15. Mai 2018 |
8-18 |
genetisch verändertes T-Zell-Präparat |
Zalmoxis®
|
andere antineoplastische Mittel |
Dompe Farmaceutici, S.p.A., Milano (I) |
15. Januar 2018 |
4-18 |
Gemtuzumab Ozogamicin |
Mylotarg®
|
antineoplastische Mittel, monoklonale Antikörper |
Pfizer Pharma GmbH |
1. September 2018 |
12-18 |
Glycerolphenylbutyrat |
Ravicti®
|
andere Mittel für das alimentäre System und den Stoffwechsel, sonstige Mittel für das alimentäre System und den Stoffwechsel |
Swedish Orphan Biovitrum GmbH |
1. März 2018 |
5-18 |
Guselkumab |
Tremfya®
|
Immunsuppressiva, Interleukin-Inhibitoren |
Janssen-Cilag GmbH |
15. Dezember 2017 |
4-18 |
Impfstoff gegen Gürtelrose |
Shingrix®
|
Varicella-Zoster-Impfstoffe |
GlaxoSmithKline GmbH & Co. KG |
1. Mai 2018 |
8-18 |
Inotersen |
Tegsedi®
|
Neuropathiepräparate und andere neurotrope Mittel |
Akcea Therapeutics Germany |
1. Oktober 2018 |
12-18 |
Letermovir |
Prevymis®
|
antivirale Mittel zur systemischen Anwendung, direkt wirkende Antiinfektiva |
MSD Sharp & Dohme GmbH |
15. Februar 2018 |
5-18 |
Methacetin |
LiMAxetin®
|
Leberfunktionstest |
Humedics GmbH |
1. Juni 2018 |
9-18 |
Metreleptin |
Myalepta®
|
andere Mittel für das alimentäre System und den Stoffwechsel, Aminosäuren und Derivate |
Aegerion Pharmaceuticals GmbH |
1. Oktober 2018 |
12-18 |
Niraparib |
Zejula®
|
andere antineoplastische Mittel |
Tesaro Bio Germany GmbH |
15. Dezember 2017 |
3-18 |
Ocrelizumab |
Ocrevus®
|
selektive Immunsuppressiva |
Roche Pharma AG |
1. Februar 2018 |
4-18 |
Padeliporfin |
Tookad®
|
Sensibilisatoren für die photodynamische/Radio-Therapie |
Steba Biotech SA (L) |
1. April 2018 |
9-18 |
Patiromer |
Veltassa®
|
Arzneimittel zur Behandlung von Hyperkaliämie und Hyperphosphatämie |
Vifor Fresenius Medical Care Renal Pharma (F), Fresenius Medical Care Nephrologica Deutschland GmbH |
1. April 2018 |
6-18 |
Rurioctocog alfa pegol |
Adynovi®
|
Antihämorrhagika, Blutgerinnungsfaktor VIII |
Shire Deutschland GmbH |
15. Februar 2018 |
8-18 |
Sonidegib |
Odomzo®
|
antineoplastische Mittel, andere antineoplastische Mittel |
Sun Pharmaceuticals Germany GmbH |
15. Februar 2018 |
5-18 |
Telotristatethyl |
Xermelo®
|
Antidiarrhoika und intestinale Antiphlogistika/Antiinfektiva, andere Antidiarrhoika |
Ipsen Pharma GmbH |
15. Oktober 2017 |
1-18 |
Tilmanocept |
Lymphoseek®
|
Radiodiagnostika, Tumorerkennung |
Norgine GmbH |
15. September 2018 |
11-18 |
Tisagenlecleucel |
Kymriah®
|
andere antineoplastische Mittel |
Novartis Pharma GmbH |
15. September 2018 |
11-18 |
Tivozanib |
Fotivda®
|
antineoplastische Mittel, Proteinkinase-Inhibitoren |
Eusa Pharma Ltd., Hemel Hempstead (UK) |
1. November 2017 |
1-18 |
Velmanase alfa |
Lamzede®
|
andere Mittel für das alimentäre System und den Stoffwechsel, Enzyme |
Chiesi GmbH |
1. Juli 2018 |
10-18 |
Voxilaprevir |
Vosevi®
|
direkt wirkendes antivirales Mittel |
Gilead Siences GmbH |
1. September 2017 |
2-18 |






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.