
- DAZ.online
- DAZ / AZ
- DAZ 6/2019
- Abnehmen schwer gemacht
Schwerpunkt Adipositas
Abnehmen schwer gemacht
Welche Regulationsprozesse bei Adipositas gestört sind
Adipositas und Energiehomöostase
Adipositas entwickelt sich als Folge einer längerfristig positiven Energiebilanz und ist durch pathologisch vergrößerte Fettspeicher charakterisiert. Dies bedeutet, dass die Energieaufnahme über die Nahrung den 24-Stunden-Energieverbrauch übersteigt. Der 24-Stunden-Energieverbrauch eines Menschen kann unterteilt werden in
- den Ruheenergieverbrauch,
- die nahrungsinduzierte Thermogenese und
- den Energieverbrauch für körperliche Aktivitäten.
Während der Ruheenergieverbrauch und die nahrungsinduzierte Thermogenese unter anderem vom Körpergewicht, Geschlecht und von der Genetik abhängen und willentlich nicht beeinflussbar sind, ist der Energieverbrauch für körperliche Aktivität eine variable Größe. Bei körperlich wenig aktiven Menschen beträgt der Anteil am Gesamtenergieverbrauch ca. 20 bis 30% [1]. Er kann bei hoher körperlicher Aktivität, wie beispielsweise bei manchen Handwerksberufen, stark steigen. Insgesamt haben adipöse Personen im Vergleich zu normalgewichtigen einen deutlich höheren absoluten 24-Stunden-Energieverbrauch. Das zeigen Daten, die mit der Goldstandardmethode „doppelt markiertes Wasser“ erhoben wurden, mit der sich der Energieumsatz bestimmen lässt. Der höhere absolute 24-Stunden-Energieverbrauch ist allerdings nicht auf vermehrte körperliche Aktivität zurückzuführen [2], sondern vorwiegend auf einen durch die größere Körpermasse erhöhten inhärenten Energieverbrauch.
In diesem Kontext ist anzumerken, dass eine klinisch relevante Gewichtsabnahme rein durch eine Fokussierung auf die körperliche Aktivität in der Regel nicht zu erreichen ist [3, 4], ungeachtet der vielen positiven Effekte, die körperliche Aktivität auf die metabolische Gesundheit bewirkt [5]. Insgesamt zeigt die Studienlage, dass eine positive Energiebilanz überwiegend durch eine erhöhte Energieaufnahme und weniger durch einen geringen 24-Stunden-Energieverbrauch bedingt ist. Bereits eine positive Energiebilanz von nur 50 kcal täglich entspräche einem Energieüberschuss von rund 17.000 kcal am Ende eines Jahres. Legt man nun die Annahme zugrunde, dass ein Kilogramm Körperfett einem Energieäquivalent von 7000 kcal entspricht, zieht dieser tägliche, auf den ersten Blick vernachlässigbare „50 kcal-Energieüberschuss“ eine Gewichtszunahme von 2,5 kg Körperfett am Ende des Jahres nach sich. Bei einer positiven Energiebilanz von 100 kcal am Tag ergäbe sich bereits eine Gewichtszunahme von fünf Kilogramm nach einem Jahr. Ein Energieüberschuss von 50 kcal bzw. 100 kcal pro Tag ist relativ einfach über die Nahrung erreicht, beispielsweise durch die zusätzliche Aufnahme von 10 (20) g Schokolade, 7 (14) g Butter oder 17 (34) g Pommes Frites. Dieses Beispiel verdeutlicht, wie präzise die Energiehomöostase aus Energieaufnahme und -verbrauch des Menschen im Normalfall abgestimmt ist. Die Regulation der Nahrungsaufnahme unterliegt dabei sehr komplexen und eng miteinander abgestimmten zentralnervösen und peripheren Mechanismen. Das Gehirn spielt bei dieser Regulation die zentrale Rolle, wobei homöostatische und nicht-homöostatische, belohnungsassoziierte Prozesse differenziert werden. Weiterhin sind auch bewusste sowie unbewusste kognitive Prozesse in diesem komplexen System involviert [6, 7].
Nur ein paar Stück Schokolade mehr ...
Ein Energieüberschuss von 50 kcal/Tag sind ca. 17.000 kcal/Jahr, und das ergibt eine Gewichtszunahme von 2,5 kg Körperfett, wenn man davon ausgeht, dass 1 kg Körperfett ca. 7000 kcal entsprechen. Ein Energieüberschuss von 100 kcal/Tag = 34.000 kcal/Jahr führt zu 5 kg Körperfett Gewichtszunahme im Jahr, und dabei entsprechen 100 kcal/Tag nur 20 g Schokolade oder 14 g Butter oder 34 g Pommes frites.
Homöostatische Regulation der Nahrungsaufnahme
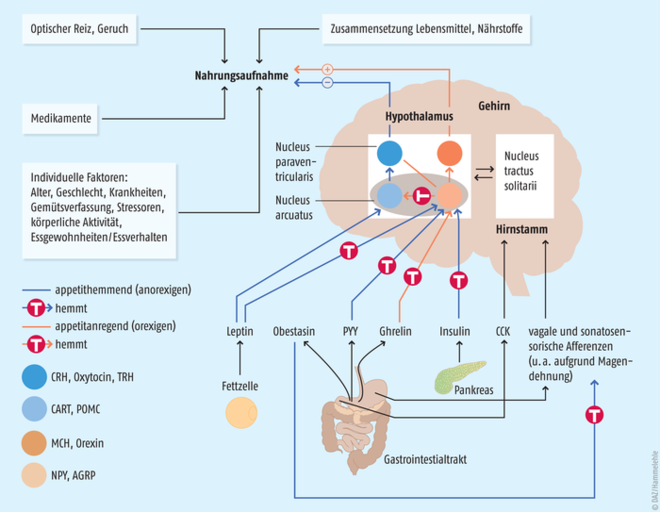
Die homöostatische Regulation findet vorwiegend in übergeordneten Zentren des Hypothalamus, aber auch im Hirnstamm statt (Abb. 1). In der Peripherie des Körpers wird eine Vielzahl von stoffwechselrelevanten Hormonen und Botenstoffen sezerniert. Die Integrierung dieser peripheren Signale erfolgt vorwiegend in den Kerngebieten des Hypothalamus, die über Assoziationsneurone wie dem Proopiomelanocortin (POMC), Agouti-related Protein (AGRP), Melanocortin und Orexin A mit weiteren Hirnregionen wie dem Mittelhirn oder Regionen des limbischen Systems verschaltet sind und daraufhin Appetit, Nahrungsaufnahme oder auch Sattheit vermitteln. Im Rahmen einer eher kurzfristigen Regulation erhalten die hypothalamischen Zentren beispielsweise Signale aus dem Magen-Darm-Trakt, vermittelt unter anderem über das Hungerhormon Grehlin sowie die Sättigungssignale Glucagon-like-peptide 1 (GLP-1), Peptid YY (PYY), pankreatisches Polypeptid (PP) oder auch Oxyntomodulin (OXM). An einer längerfristigen Kontrolle der Nahrungsaufnahme ist hingegen unter anderem das Sättigungshormon Leptin beteiligt, das vorwiegend aus den Adipozyten sezerniert wird. Nach der Entdeckung des Leptins im Jahr 1994 bestand die Hoffnung, durch die appetithemmende, anorexigene Wirkung von Leptin einen pharmakologischen Durchbruch in der Adipositasbehandlung erreicht zu haben. Die pathologische Vermehrung des Körperfettanteils bei Adipositas ist jedoch mit einer vermehrten Ausschüttung von Leptin und in dessen Folge mit einer Leptin-Resistenz verbunden, so dass eine Supplementierung sich als nicht wirksam erwies [8]. Nur beim extrem seltenen Fall einer monogenetischen Leptin-Defizienz, von der in der Literatur bislang nur wenige Fälle beschrieben sind, bewirkt eine Leptin-Substitution eine Gewichtsabnahme. Konkret konnte ein Junge, der im Alter von vier Jahren 42 kg wog, sein Körpergewicht trotz Wachstum bis zum Alter von sieben Jahren auf 32 kg reduzieren [9].
Der hedonische Hunger
Hedonisch lässt sich aus dem griechischen herleiten und bedeutet so viel wie „Lust“. An der hedonischen, das heißt der belohnungsassoziierten Regulation der Nahrungsaufnahme sind unter anderem kortikale Strukturen, die Insula und das ventrale Striatum mit dem Nucleus accumbens beteiligt. Die belohnungsassoziierte Regulation ist wesentlich durch Verfügbarkeit und Geschmack der Nahrung beeinflussbar. In diesem Zusammenhang berichten adipöse Personen, dass sie häufig nicht aufgrund von Hungergefühlen essen, sondern einen starken Drang verspüren, wohlschmeckende und in der Regel kalorienreiche Speisen und Lebensmittel zu verzehren. Dieses Phänomen wird auch als hedonischer Hunger bezeichnet. Hedonischer Hunger lässt sich mit der Power of Food Scale erfassen, einem Fragebogen, der den Einfluss des reichlichen Nahrungsangebots in unserer „obesigenen“ Gesellschaft erfasst [10, 11]. Dabei wird weniger auf den eigentlichen Verzehr, sondern vielmehr auf den Appetit fokussiert.
Es werden zudem drei Ebenen der Verfügbarkeit von Lebensmitteln und Speisen unterschieden, die immer näher an uns heranrücken:
- generell verfügbar, die Lebensmittel sind im weiteren Umfeld verfügbar und können z. B. käuflich erworben werden (sogenanntes food available);
- in der Nähe verfügbar, die Lebensmitteln sind im engeren Umfeld (z. B. in der Küche) verfügbar (sogenanntes food present), oder
- im Augenblick probiert (sogenanntes food tasted) [10, 11].
Studien belegen einen vermehrt ausgeprägten hedonischen Hunger bei Personen mit extremer Adipositas im Vergleich zu normalgewichtigen Personen [12]. Bei ehemals extrem adipösen Patienten, die nach einer Magen-Bypass-Operation deutlich an Gewicht abgenommen haben, normalisierte sich der initial gesteigerte hedonische Hunger [13].
Belohnungsassoziierte Regulation der Nahrungsaufnahme
Ein hoher Konsum an süßen Lebensmitteln und Getränken ist meist durch den angenehmen Geschmack zu begründen und wird häufig auch mit einer Art „Abhängigkeit“ oder Suchtverhalten in Verbindung gebracht. Das „Abhängigkeitspotenzial“ von Zucker bzw. Süßgeschmack wurde in einer tierexperimentellen Arbeit untersucht [14]. Die Autoren konnten zeigen, dass Ratten den Süßgeschmack einer Saccharin-Wasser-Lösung gegenüber Cocain bevorzugten. Die Süßperzeption stellte offensichtlich einen größeren „Belohnungswert“ für die Ratten dar als Cocain, und dies sogar auch bei Cocain-abhängigen Tieren.
Es gibt zunehmend Hinweise darauf, dass bei Adipositas ein verändertes Belohnungsverhalten vorliegt. Die Forschung liefert immer mehr Evidenz für die wesentliche Rolle des dopaminergen Belohnungssystems im Rahmen der Energiehomöostase und Regulation der Nahrungsaufnahme. Die Zufuhr von Nahrung dient nicht nur der Aufrechterhaltung der Energiehomöostase, sondern sie ist auch ein belohnungserzeugendes Ereignis. Somit kann die Nahrungszufuhr eine „Suchtkomponente“ erhalten, welche dann zwangsläufig in einer positiven Energiebilanz mit folgender Gewichtszunahme resultiert. Interessanterweise konnte in diesem Kontext auch gezeigt werden, dass bei Adipositas, wie auch bei substanzgebundenem Suchtverhalten (z. B. Cocain-Abhängigkeit), eine verminderte Expression von Dopamin-D2-Rezeptoren sowie eine verminderte Dopamin-Sekretion vorliegt [15, 16]. Diese Veränderungen führen dann bei einer vergleichbaren Stimulation zu einer niedrigeren Aktivierung von Hirnregionen, die mit Belohnungsverarbeitung und Handlungskontrolle assoziiert sind. Demzufolge wird eine erneute Zufuhr von Nahrung gefördert.
Aber auch die Bewertung und der Preis eines Lebensmittels spielen eine wichtige Rolle in der Regulation der Nahrungsaufnahme. Ein Wein, der als teuer angepriesen wird, wird von Probanden auf der Liking-Skala besser bewertet als der gleiche Wein, wenn er vermeintlich preiswerter ist [17]. Mittels des sogenanntes Wanting-Liking-Konstrukts können neuronale Prozesse in der Belohnungsverarbeitung quantifiziert werden. Während Wanting das Verlangen nach einer Belohnung abbildet, beschreibt Liking die Freude beim Erhalt dieser und bildet eine bewusste Wahrnehmung hedonischer Aspekte bei der Nahrungsaufnahme ab. Dieses Phänomen bei der Weinverkostung ließ sich auch mittels funktioneller Magnetresonanztomografie bestätigen, mit deren Hilfe höhere Reaktionen in orbifrontalen Hirnregionen gemessen wurden, wenn die Probanden den vermeintlich teureren Wein verkostet haben.
Welche Rolle spielt die Kognition?
Homöostatische und belohnungsassoziierte Signale in der Regulation der Nahrungsaufnahme werden durch kognitive Prozesse bewusst und unbewusst moduliert. So beeinflussen beispielsweise soziale Aspekte wie Essen in Gemeinschaft die Menge und Auswahl der verzehrten Nahrung. Bereits Anfang 1990 wurde gezeigt, dass in einer Gruppe in der Regel mehr verzehrt wird, als wenn man allein isst. Bei gemeinschaftlichem Essen in der Gruppe stieg die Mahlzeitengröße um bis zu 75% [18]. Dieser Effekt kehrt sich allerdings um, wenn Fremde oder als attraktiv wahrgenommene Personen in der Gruppe anwesend sind [19]. Aber auch die Zusammensetzung der Gruppe (gemischt- oder getrenntgeschlechtlich) scheint die Menge an verzehrter Nahrung zu beeinflussen. Während Frauen in gemischten Geschlechtergruppen in einem Fast-Food-Restaurant weniger aßen als in einer Gruppe, die nur aus Frauen bestand, verzehrten die Männer hingegen mehr in gemischten Gruppe als nur „unter Männern“ [20]. Auch beeinflusst die Information über die Menge, die andere Personen von der gleichen Mahlzeit verzehrt haben, das eigene Essverhalten [19].
Neues Pathogenese-Verständnis
Auch wenn die Ursachen der Adipositas insgesamt multifaktoriell und komplex sind, scheint bei Adipositas sowohl eine Störung homöostatischer als auch belohnungsassoziierter Regulationsprozesse der Nahrungsaufnahme vorzuliegen. Die wachsenden Erkenntnisse über die Bedeutung und Regulation hedonischer Essmotive wie beispielsweise die Perzeption von Süßgeschmack oder das dopaminerge „Belohnungssystem“ bieten ein neues Verständnis der Pathogenese der Adipositas. So ist beispielsweise die Süßperzeption in der heutigen „obesigenen“ Umwelt von großer Bedeutung. Der Verzehr von zuckerhaltigen Getränken befindet sich in Deutschland auf einem sehr hohen Niveau und ist bei den 18- bis 29-Jährigen am höchsten. Er liegt bei den Männern bei 4,5 Gläsern pro Tag und bei Frauen bei drei Gläsern [21], was einem Energieäquivalent von im Mittel zusätzlich 400 kcal bzw. 270 kcal entspricht. Ein besseres Verständnis homöostatischer, belohnungsassoziierter und kognitiver Prozesse in der Regulation von Nahrungsaufnahme und Energiebilanz wird hoffentlich zu neuen Therapieansätzen und Implikationen bei Adipositas führen. |
Literatur
[1] Müller M et al. Energieverbrauch und Energiebedarf gesunder Menschen. Aktuelle Ernährungsmedizin 2006;31(03):98-109
[2] DeLany JP et al. High energy expenditure masks low physical activity in obesity. Int J Obes 2005 2013;37(7):1006-1011
[3] Swift DL et al. The role of exercise and physical activity in weight loss and maintenance. Prog Cardiovasc Dis 2014;56(4):441-447
[4] Fogelholm M, Kukkonen-Harjula K. Does physical activity prevent weight gain – a systematic review. Obes Rev Off J Int Assoc Study Obes 2000;1(2):95-111
[5] Kennedy AB et al. Fitness or Fatness: Which Is More Important? JAMA 2018;319(3):231-232
[6] Alonso-Alonso M, Pascual-Leone A. The right brain hypothesis for obesity. JAMA 2007;297(16):1819-1822
[7] Zheng H, Berthoud HR. Neural systems controlling the drive to eat: mind versus metabolism. Physiol Bethesda Md 2008;23:75-83
[8] DePaoli AM. 20 years of leptin: leptin in common obesity and associated disorders of metabolism. J Endocrinol 2014;223(1):T71-81
[9] Farooqi IS et al. Effects of recombinant leptin therapy in a child with congenital leptin deficiency. N Engl J Med 1999;341(12):879-884
[10] Lowe MR et al. The Power of Food Scale. A new measure of the psychological influence of the food environment. Appetite 2009;53(1):114-118
[11] Lowe MR, Butryn ML. Hedonic hunger: a new dimension of appetite? Physiol Behav 2007;91(4):432-439
[12] Schultes B et al. Hedonic hunger is increased in severely obese patients and is reduced after gastric bypass surgery. Am J Clin Nutr 2010;92(2):277-283
[13] Ullrich J et al. Roux-en Y gastric bypass surgery reduces hedonic hunger and improves dietary habits in severely obese subjects. Obes Surg 2013;23(1):50-55
[14] Lenoir M et al. Intense sweetness surpasses cocaine reward. PloS One 2007;2(8):e698
[15] Grosshans M et al. Implications from addiction research towards the understanding and treatment of obesity. Addict Biol 2011;16(2):189-198
[16] Wang GJ et al. Brain dopamine and obesity. Lancet Lond Engl 2001;357(9253):354-357
[17] Plassmann H et al. Marketing actions can modulate neural representations of experienced pleasantness. Proc Natl Acad Sci USA 2008;105(3):1050-1054
[18] de Castro JM, Brewer EM. The amount eaten in meals by humans is a power function of the number of people present. Physiol Behav 1992;51(1):121-125
[19] Herman CP et al. Effects of the presence of others on food intake: a normative interpretation. Psychol Bull 2003;129(6):873-886
[20] Brindal E, Wilson C, Mohr P, Wittert G. Eating in groups: Do multiple social influences affect intake in a fast-food restaurant? J Health Psychol 2015;20(5):483–839
[21] Rabenberg M, Mensink G. Limo, Saft & Co – Konsum zuckerhaltiger Getränke in Deutschland. Zahlen und Trends aus der Gesundheitsberichterstattung des Bundes, GBE kompakt 4(1), Robert Koch-Institut 2013, www.rki.de/gbe-kompakt























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.