
- DAZ.online
- DAZ / AZ
- DAZ 19/2022
- AkdÄ bewertet Paxlovid
Pandemie Spezial
AkdÄ bewertet Paxlovid
COVID-19-Risikopatienten müssen antivirales Arzneimittel frühzeitig erhalten
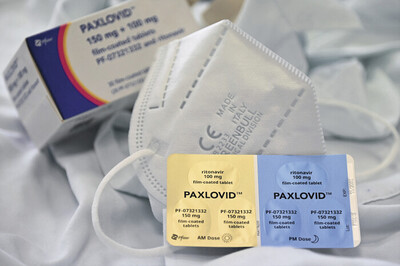
Eine Tagesdosis Paxlovid® umfasst zwei Tabletten Nirmatrelvir (jeweils 150 mg morgens und abends) kombiniert mit einer Tablette Ritonavir (100 mg).
Paxlovid®, das von der Firma Pfizer entwickelt wurde, besteht aus den beiden Wirkstoffen Nirmatrelvir und Ritonavir, die in zwei verschiedenen Tabletten möglichst früh nach Symptombeginn über fünf Tage oral verabreicht werden. Nirmatrelvir basiert auf einer Weiterentwicklung von Rupintrivir, einem bereits früher in klinischen Studien zur Behandlung von Rhinovirus-Infektionen getesteten Inhibitor viraler Proteasen. Als Inhibitor der 3-CL(chymotrypsin-like cysteine)-Protease beeinträchtigt Nirmatrelvir so die Replikation von SARS-CoV-2. Das beigefügte Ritonavir dient lediglich der Hemmung des CYP3A-vermittelten Abbaus von Nirmatrelvir. Durch die höheren Plasmaspiegel soll die Wirksamkeit von Nirmatrelvir verbessert werden. Paxlovid® ist seit dem 28. Januar 2022 bedingt zugelassen zur Behandlung von COVID-19 bei Erwachsenen, die keine zusätzliche Sauerstoffzufuhr benötigen und ein erhöhtes Risiko für einen schweren Krankheitsverlauf aufweisen. Für die Verordnung müssen bestimmte Voraussetzungen erfüllt sein (unter anderem ein positives Testergebnis, Übermittlung der Verordnung des Arztes an eine Apotheke). Rund drei Monate später hat die Arzneimittelkommission der deutschen Ärzteschaft nun ihre Erkenntnisse zur Wirksamkeit von Nirmatrelvir/Ritonavir zusammengefasst und die vorliegenden Daten bewertet. Diese beruhen vornehmlich auf der Zulassungsstudie EPIC-HR (s. Kasten).
Eckdaten der Zulassungsstudie EPIC-HR (Evaluation of Protease Inhibition for COVID-19 in High-Risk Patients)
Studiendesign: doppelblinde, randomisierte, placebokontrollierte Phase-II / III-Studie
Studienpopulation: ambulante Patienten mit nachgewiesener SARS-CoV-2-Infektion
Einschlusskriterien: u. a. Symptombeginn vor maximal fünf Tagen, Vorliegen von mindestens einem Risikofaktor für einen schweren Krankheitsverlauf (u. a. Alter ≥ 60 Jahre)
Ausschlusskriterien: u. a. Impfung gegen SARS-CoV-2 oder bereits zurückliegende Infektion mit SARS-CoV-2
Studienmedikation: Verum-Gruppe (n = 1120) fünf Tage alle zwölf Stunden jeweils 300 mg Nirmatrelvir und 100 mg Ritonavir; Placebo-Gruppe (n = 1126) Placebo fünf Tage alle zwölf Stunden
primärer Studienendpunkt: Hospitalisierungs- und/oder Sterberate innerhalb von 28 Tagen
Eintrag im US-amerikanischen Studienregister: NCT 04960202
Publikation der Studienergebnisse: Hammond JL et al. EPIC-HR Investigators: Oral nirmatrelvir for high-risk, nonhospitalized adults with covid-19. N Engl J Med 2022;386:1397-1408
Über den Einfluss des Behandlungsbeginns ...
Der kombinierte Endpunkt ergab sich überwiegend aus COVID-19-bedingten Hospitalisierungen. Insgesamt ereigneten sich zwölf Todesfälle, keiner davon in der Verum-Gruppe. Die Wirksamkeit von Nirmatrelvir/Ritonavir wurde in verschiedenen Subgruppen untersucht. Die mITT(modified intention-to-treat)-Population umfasste Patienten mit mindestens einer Einnahme der Studienmedikation und mindestens einer Studienvisite nach Baseline. In Abhängigkeit vom Beginn der Medikationseinnahme (≤ 3 oder ≤ 5 Tage nach ersten Symptomen) und dem Erhalt monoklonaler Antikörper wurden verschiedene Untergruppen der mITT-Population untersucht. Hier die wichtigsten Ergebnisse:
Bei Patienten der mITT-Population, deren Behandlung innerhalb von drei Tagen begann und bei denen zu Studienanfang keine Therapie mit monoklonalen Antikörpern erfolgte, führte Nirmatrelvir/Ritonavir zu einer absoluten Risikoreduktion für COVID-19-bedingte Hospitalisierungen oder Tod von knapp 6% (absolute Risikoreduktion 5,8%; p < 0,001). Die Number-needed-to treat (NNT, s. Kasten) betrug 18. Eine ähnliche Wirksamkeit wurde auch bei Patienten mit einem späteren Behandlungsbeginn (Tag 4 oder 5 nach Symptombeginn) und bei Patienten mit zusätzlicher Antikörper-Therapie festgestellt.
Was bedeutet die NNT?
Die Number-needed-to-treat (NNT) gib die geschätzte Zahl an notwendigen Behandlungen an, um ein unerwünschtes Ereignis zu verhindern, welches unter einer Alternativbehandlung bzw. Nichtbehandlung aufgetreten wäre.
Je höher die Number needed to treat ist, desto geringer ist der Unterschied zwischen den beiden Behandlungsmethoden. Bei einem NNT-Wert von 1 (= optimale NNT) profitiert jeder Patient von der Behandlungsmethode X gegenüber der Behandlungsmethode Y.
Subgruppenanalysen stützen die Annahme, dass der Behandlungsbeginn die Wirksamkeit von Nirmatrelvir/Ritonavir nicht wesentlich beeinflusst (≤ 3 Tage vs. > 3 Tage; absolute Risikoreduktion 5,8% vs. 5,2%).
Die Wirksamkeit von Nirmatrelvir/Ritonavir bei zusätzlicher Gabe von monoklonalen Antikörpern ließ sich nicht sicher beurteilen, da die Anzahl der Patienten zu gering war.
... sowie von Risikofaktoren und protektiven Faktoren
Weitere Subgruppenanalysen zeigten eine weitgehend konstante relative Risikoreduktion durch Nirmatrelvir/Ritonavir bei Vorliegen typischer Risikofaktoren (höheres Alter, Adipositas) bzw. protektiver Faktoren (jüngeres Alter, positive Serologie). Entsprechend dem unterschiedlichen Ausgangsrisiko schwankte die Höhe der absoluten Risikoreduktion erheblich: Während die absolute Risikoreduktion bei älteren Patienten (≥ 65 Jahre) 14% betrug (NNT = 8), lag sie bei Patienten mit positiver Serologie nur wenig über 1% (NNT = 77).
Die häufigsten unerwünschten Ereignisse unter Nirmatrelvir/Ritonavir waren Störungen des Geruchs- und Geschmackssinnes (6%) sowie Durchfall (3%). Hypertonie und Muskelschmerzen traten selten (< 1%), aber numerisch häufiger unter Nirmatrelvir/Ritonavir auf.
Wirksam auch gegen die Omikron-Variante?
Das positive Ergebnis der Zulassungsstudie – die signifikante Reduktion der Hospitalisierungsrate/Gesamtmortalität – durch Nirmatrelvir/Ritonavir wird von der AkdÄ detailliert und auf seine Übertragbarkeit auf die aktuelle virologische Situation hin untersucht. So war zu Studienbeginn die Delta-Variante des Virus vorherrschend. Ob man bei dominierenden Omikron-Varianten von der gleichen Wirksamkeit ausgehen kann, ist unklar; auch wenn die entsprechenden Mutationen überwiegend das Spike-Protein und nicht die Virusproteasen betreffen. Zudem führt die Omikron-Variante zu leichteren Krankheitsverläufen als die Delta-Variante. Durch das niedrigere Ausgangsrisiko ist bei Infektionen durch Omikron eine geringere absolute Risikoreduktion durch Nirmatrelvir/Ritonavir zu erwarten.
Keine eindeutige immunologische Ausgangslage
Ein weiterer Punkt ist die immunologische Ausgangslage der Probanden. Laut Studienprotokoll war zwar eine Teilnahme geimpfter oder genesener Probanden nicht möglich, dennoch wies die Hälfte der Patienten zum Zeitpunkt der Randomisierung einen positiven Antikörpertiter auf. Es ist unklar, ob der Antikörpernachweis auf einer früheren, nicht diagnostizierten SARS-CoV-2-Infektion beruhte oder Ausdruck einer aktuellen Immunreaktion gegen SARS-CoV-2 war. Der Schluss liegt nahe, dass ein relevanter Anteil der Patienten vor Studieneinschluss unbemerkt von COVID-19 genesen war. Die Wirksamkeit von Nirmatrelvir/Ritonavir bei immunsupprimierten Patienten oder in Kombination mit monoklonalen Antikörpern ließ sich anhand der vorliegenden Daten nicht beurteilen.
Aufgrund dieser Unklarheiten – dem Vorliegen asymptomatischer Infektionen in der Studienpopulation und der derzeitigen Dominanz der Omikron-Variante – ist in der jetzigen Situation mit einer geringeren Risikoreduktion als der in der Zulassungsstudie ermittelten auszugehen, so die AKdÄ.
Vor allem Ältere profitieren
Den Studienergebnissen zufolge profitierten vor allem ältere Probanden von einer Therapie mit Nirmatrelvir/Ritonavir (absolute Risikoreduktion 14%; NNT = 8). Da diese Patienten häufig multimorbide sind, müssen potenzielle Interaktionen mit weiteren Arzneimitteln berücksichtigt werden. Obwohl keine Daten zur Wirksamkeit von Nirmatrelvir/Ritonavir bei einem späteren Behandlungsbeginn vorliegen, ist anzunehmen, dass die Wirksamkeit mit der Zeit abnimmt. Dies kann aus Erfahrungen mit Remdesivir abgeleitet werden. Daher sollten aus Sicht der AkdÄ geeignete Hochrisikopatienten vorausschauend über die Therapieoption mit Nirmatrelvir/Ritonavir aufgeklärt werden. Bereits bei den ersten Symptomen sollte ein Test auf SARS-CoV-2 durchgeführt und der Arzt kontaktiert werden. |
Literatur
Nirmatrelvir/Ritonavir (Paxlovid®). Informationen der Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ), Neue Arzneimittel, Arzneiverordnung in der Praxis, 26. April 2022
Number needed to treat. Informationen der DocCheck Medical Services GmbH




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.