
- DAZ.online
- DAZ / AZ
- Ein Jugendlicher nach ...
Ein Jugendlicher nach Nierentransplantation
Der Patient
Von Isabel Waltering, Susanne Koling, Olaf Rose und Hartmut Derendorf unter Mitarbeit von Mathias Freitay
In der Klinischen Pharmazie dreht sich alles um den Patienten, um Leitlinien und um das klinische Ergebnis. Bearbeiten Sie mit uns diesen Patientenfall und erlernen Sie so zusätzliches therapeutisches Wissen.
In diesem Artikel lesen Sie:
- welche prophylaktischen Therapien bei der Behandlung von transplantierten Patienten notwendig sind.
- welche unerwünschten Arzneimittelwirkungen unter einer solchen Therapie auftreten können.
- zu welchen Aspekten Sie den Patienten oder seine Angehörigen schulen können.
Der Patient
Matthias Hoffmann ist ein 15-jähriger Patient, der vor drei Monaten nierentransplantiert wurde. Die Transplantation ist ohne besondere Komplikationen verlaufen und das transplantierte Organ zeigte eine gute Funktion. Nach vier Wochen wurde wegen Verdachts auf eine Abstoßungsreaktion eine hochdosierte Cortison-Therapie begonnen, die mit dem Antimykotikum Noxafil® (Posaconazol Suspension) begleitet wurde. Die Therapie mit Voriconazol musste wegen Hautreaktionen umgestellt werden.
Da Matthias die Suspension nicht gern einnimmt, bittet die Mutter die Apothekerin herauszufinden, ob es dieses Medikament nicht auch als Tablette gibt. Außerdem möchte sie noch eine Spülung gegen Zahnfleischentzündung für ihren Sohn, da das Zahnfleisch sehr angeschwollen und gerötet ist.
Als allgemeine lokale antimykotische Prophylaxe erhält Matthias Pimafucin® (Natamycin) Lutschtabletten, als Virustatikum Valtrex® (Valaciclovir) und zur Prophylaxe gegen Pneumocystis jirovecii Cotrimoxazol. Zur Therapie der posttransplantationbedingten Hypertonie wird Amlodipin eingesetzt.
Die verordnete Medikation besteht aus:
Ciclosporin (Sandimmun optoral®) 200 mg/d
Valganciclovir (Valcyte®) 2 × 500 mg/d
Natamycin (Pimafucin®) 3 × 1
Cotrimoxazol Di + Fr 2 × 960 mg
Posaconazol (Noxafil®) 2 × 200 mg/d
Amlodipin 1 × 5 mg/d
Colecalciferol (Vigantoletten®) 1 × 1000 IE/d
Eisen(II)-glycin-sulfat-Komplex (Ferrosanol duodenal mite®) 1 × 50 mg Fe²+/d
Prednisolon 10 mg/d, Reduktion nach Angabe
Diese Angaben entstammen dem Plan der Ambulanz.
Vitalparameter und Laborwerte
Diagnosen:
Nierentransplantation (vor drei Monaten)
Verdacht auf Transplantatabstoßung (vor vier Wochen)
Bluthochdruck (Posttransplantation)
Vitalparameter:
Größe 168 cm, Gewicht 61 kg
Blutdruck: 135/80 mmHg
ausgewählte Laborwerte:
Leukozyten 3700/µl
Hb: 10,6 mg/dl
Natrium: 132 mmol/l
Kalium: 5,0 mmol/l
GOT: 80 U/l
GPT: 50 U/l
Creatinin: 1,1 mg/dl
GFR: 107 ml/min/1,73 m² (nach Schwartz [1])
Körperoberfläche = 1,7 m² (Mosteller)
Harnsäure: 9 mg/dl
Ciclosporin-Tal-Spiegel 225 ng/ml (Ziel 150 ng/ml)
Klinische Pharmazie der Nierentransplantation
Epidemiologie/Pathobiochemie
Wenn bei einer Erkrankung der Nieren deren Leistungen unter 10% der normalen Funktion abfällt oder erlischt, kann eine Nierentransplantation notwendig sein. Bei Kindern ist die Transplantation immer das Behandlungsziel. Seit 1954 wurden über 300.000 Nierentransplantationen durchgeführt. In Deutschland bekommen ca. 2000 Menschen pro Jahr eine neue Niere, davon ca. 1000 Kinder [2]. Nach einer Nierentransplantation sind die konsequente Einnahme von Immunsuppressiva auf Dauer und von prophylaktischen Arzneimitteln entweder dauerhaft oder für die erste Zeit nach der Therapie notwendig [3]. Abstoßungsreaktionen können zu jedem Zeitpunkt nach der Operation auftreten und werden in hyperakute, akute, humorale und chronische Abstoßungsreaktionen unterteilt. Die Therapie beginnt hier häufig mit hochdosierten Glucocorticoiden [3]. Ziel der Therapie ist es, diese Abstoßungsreaktionen zu verhindern und das Transplantat nicht zu verlieren. Dazu ist es notwendig, ausreichend hohe Dosen der Immunsuppressiva zu verabreichen, was wiederum zu erhöhter Nephrotoxizität, Infektionen, Thrombozytopenie und Diabetes mellitus führen kann. Somit muss die Therapie genau ausbalanciert sein, um weder dem Patienten noch dem Transplantat zu schaden [4]. Erhaltungstherapie der ersten Wahl ist nach KDIGO (Kidney Disease: Improving Global Outcomes) die Kombination eines Calcineurin-Inhibitors mit einem Proliferations-Hemmer mit oder ohne Steroid.
Highlights
- Nach einer Nierentransplantation ist eine immunsuppressive Therapie notwendig. Verwendet werden Tacrolimus (Prograf®), Ciclosporin (Sandimmun Optoral®), Mycofenolatmofetil (CellCept®), Azathioprin, Sirolimus (Rapamune®) und Glucocorticoide. Meistens werden initial Kombinationen der erstgenannten Substanzen mit Glucocorticoiden eingesetzt.
- Zu Beginn der Therapie werden meist höhere Dosen verwendet. Glucocorticoide können zum Teil nach ein paar Wochen vollständig abgesetzt werden.
- Calcineurin-Inhibitoren (Ciclosporin oder Tacrolimus) können die Niere schädigen, daher ist die Dosis möglichst niedrig zu halten.
- Aufgrund der therapeutischen Immunsuppression besteht ein erhöhtes Risiko für Infektionen.
- Eine antivirale Therapie mit oralem Valganciclovir oder Ganciclovir ist mindestens für drei Monate nach Transplantation notwendig.
- Cotrimoxazol wird für drei bis sechs Monate nach der Transplantation zur Prophylaxe der Pneumocystis-jirovecii(PCJ)-Pneumonie eingesetzt, einer Pneumonie, die durch einen Pilz ausgelöst wird.
- In den ersten ein bis drei Monaten nach der Transplantation werden Antimykotika lokal eingesetzt, um oralen und oesophagialen Candida-Infektionen vorzubeugen.
- Überwachung von Blutdruck, Blutzucker, Blutfettwerten und des Körpergewichtes sowie von Creatinin-Werten, Harnsäure, Phosphat, Calcium und Eiweißen im Urin ist nach der Transplantation notwendig. Bei Kindern ist zusätzlich die Körpergröße zu überwachen.
Die Therapie ist nicht so einfach
Therapieprinzipien
Die Therapie zur Immunsuppression basiert auf einer Kombination mehrerer Wirkstoffe, eine hochdosierte Monotherapie führt zu erhöhten Nebenwirkungen und sollte vermieden werden. In den ersten drei Monaten wird üblicherweise eine erhöhte Dosis der immunsuppressiven Kombinationstherapie gewählt, ein Corticosteroid ergänzt und oft auch eine Induktion mit Biologika (Interleukin-2-Rezeptor-Antikörper oder Anti-Thymocyte Globulin [ATG]) angesetzt, danach kann reduziert werden. Die meisten Patienten erhalten zur Immunsuppression einen Calcineurin-Inhibitor und einen Antimetaboliten. In den letzten Jahren hat sich bei den Calcineurin-Inhibitoren ein Trend hin zu Tacrolimus durchgesetzt, bei den Antimetaboliten wird meist Mycophenolat-Mofetil gewählt. Diese Kombination ist die am häufigsten verwendete Basis der Therapie. Leider gibt es keinen Marker zur Dosisfindung, so dass aus Sicherheitsgründen meist zu hoch dosiert werden muss. Eine Kontrolle der Dosierung findet über die Bestimmung der Blutspiegel statt. Zusätzlich ist eine Infektionsprophylaxe erforderlich, die sich am Risikopotenzial des einzelnen Patienten orientiert und an der Spenderniere.
Immunsuppressiva
Calcineurin-Inhibitoren. Ciclosporin (CsA) und Tacrolimus (Tac) gehören zu den sogenannten Calcineurin-Inhibitoren, die bei den meisten Organtransplantierten eingesetzt werden. Die Wirkstoffe hemmen die Aktivierung von Calcineurin, einer Phosphatase, die für die Aktivierung von T-Zellen und deren Proliferation eine wichtige Rolle spielt. Ebenfalls wird die Bildung von Interleukin 2 (IL-2), einem wichtigen Faktor bei der Aktivierung von Entzündungsreaktionen, unterbunden. Beide Substanzen haben eine ähnliche Kinetik und weisen viele Interaktionen mit CYP3A4 auf, über das sie extensiv verstoffwechselt werden. Mit Inhibitoren des Glykoprotein-P (P-gp-Inhibitoren) sind ebenfalls Wechselwirkungen möglich, die zu erhöhten Blutspiegeln und damit verstärkter Toxizität führen können. Klassische Nebenwirkungen neben der Nephrotoxizität sind Neurotoxizität, Hypertonie, Hyperglykämie und Tremor. Typisch für Ciclosporin ist eine Gingiva-Hyperplasie, während Tacrolimus häufig Durchfälle verursacht [3]. Die Therapieüberwachung erfolgt durch Messung der Tal-Spiegel.
Antimetabolite. Zu den Antimetaboliten gehören Azathioprin und Mycophenolsäure (MPA), wobei letztere wegen der geringeren Nebenwirkungen und spezifischeren Wirkung heutzutage überwiegend eingesetzt wird. MPA hemmt selektiv das Enzym Inosinmonophosphat-Dehydrogenase, welches für die Biosynthese von Guanosin von Bedeutung ist. Dadurch werden die DNA-Synthese und die Proliferation von B- und T-Zellen gehemmt. Im Unterschied zu den Calcineurin-Inhibitoren ist Mycophenolsäure nicht nephro- oder neurotoxisch und verursacht keine Hypertonie. Häufig treten dosisabhängig gastrointestinale Probleme auf. Gefürchtet sind die selteneren hämatologischen Nebenwirkungen und die progressive multifokale Leukoenzephalopathie. Für Mycophenolsäure sind Wechselwirkungen mit Ciclosporin, Pantoprazol, Aciclovir und diverse Antibiotika beschrieben. Auch hier wird im Allgemeinen der Tal-Spiegel bestimmt.
Proliferationssignal-Hemmer (mTORi). Sirolimus und Everolimus binden an Immunophilin und hemmen somit die Zellantwort auf IL-2 und im Weiteren somit die T-Zell-Proliferation und den Zellzyklus [5]. Sirolimus unterscheidet sich von Everolimus durch eine deutlich längere Halbwertszeit. Die Metabolisierung erfolgt analog zu den Calcineurin-Inhibitoren über CYP3A4 und definiert somit auch das Interaktionspotenzial. Interaktionen mit P-gp sind ebenfalls beschrieben. Nebenwirkungen sind Hyperlipidämie, Thrombozytopenie und Leukopenie. Sirolimus wird einmal täglich eingenommen, Everolimus zweimal täglich. Beide Substanzen werden aber nicht in Monotherapie angewendet. Eingesetzt werden sie in der Regel bei Unverträglichkeiten der Standardtherapie.
Glucocorticoide. Glucocorticoide werden von Beginn an eingesetzt. An Tag 1 bis 3 werden 100 mg/Tag gegeben und dann sukzessive auf 15 mg/d (Monat 1), dann 10 mg/d (Monat 3) und ab dem 6. Monat nach Transplantation auf 7,5 bis 5 mg/d als Erhaltungstherapie reduziert. Besonders bei präpubertierenden Kindern sind wegen des Risikos z. B. von Wachstumshemmung möglichst geringe Dosen erstrebenswert.
Biologika. Interleukin(IL)-2-Rezeptorantagonisten gelten in der Induktionstherapie vor oder während der Transplantation als Mittel der ersten Wahl bei erhöhtem Abstoßungsrisiko.
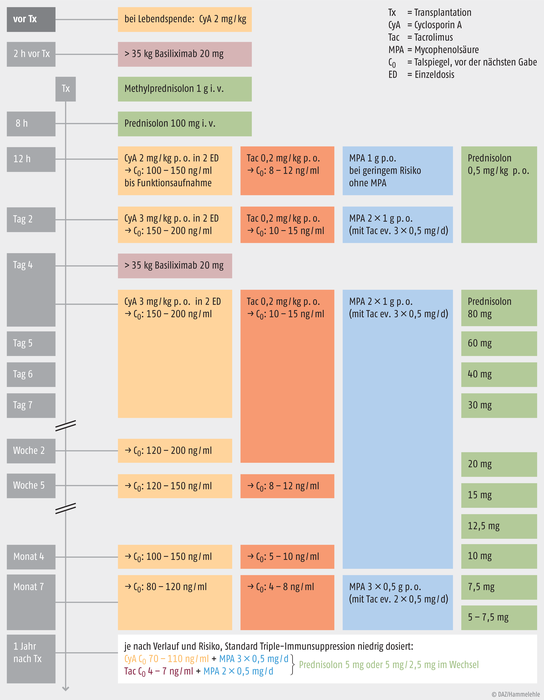
Die Abbildung 1 gibt einen Überblick über die standardmäßige immunsuppressive Therapie nach Nierentransplantation. Tabelle 1 (siehe nächste Seite) zeigt die Toxizitäten der einzelnen Substanzgruppen.
Abb. 1: Immunsuppression bei einer Transplantation Es kann je nach Transplantationszentrum Unterschiede im Therapieprotokoll geben [nach 3, 15].
| unerwünschter Effekt | Steroide | Ciclosporin | Tacrolimus | mTORi | Mycophenolsäure |
|---|---|---|---|---|---|
| Diabetes, neu | ↑ | ↑ | ↑↑ | ↑ | |
| Dyslipidämie | ↑ | ↑ | ↑↑ | ||
| Hypertension | ↑↑ | ↑↑ | ↑ | ||
| Osteopenie | ↑↑ | ↑ | (↑) | ||
| Anämie/Leukopenie | ↑ | ↑ | |||
| Wundheilungsstörungen | ↑ | ||||
| Diarrhö/Übelkeit/Erbrechen | ↑ | ↑↑ | |||
| Proteinurie | ↑↑ | ||||
| Abnahme der GFR | ↑ | ↑ | |||
↑ moderater Effekt; ↑↑ moderat-schwerwiegender Effekt; (↑) Effekt möglich, aber selten | |||||
Prophylaxe
Prophylaxe
Immunsupprimierte Patienten haben ein erhöhtes Risiko für bakterielle, virale und fungale Infektionen. In den ersten sechs Monaten nach der Transplantation ist das Erkrankungsrisiko besonders hoch [6]. Regelmäßig zur Prophylaxe eingesetzt werden die folgenden Substanzen:
Aciclovir/Valaciclovir/Valganciclovir/Ganciclovir. Diese Nukleosid-Analoga werden bei Viruserkrankungen und zu deren Prophylaxe verwendet. Die aktivierten Phosphate hemmen die Virus-DNA-Polymerase und führen zu einem Kettenabbruch bei der DNA-Synthese. Valaciclovir ist der Valin-Ester des Aciclovir und somit ein Prodrug. Beide Substanzen werden zur Prophylaxe und Therapie von Varizella-zoster-Infektionen eingesetzt. Valganciclovir und Ganciclovir werden zur Prophylaxe von Cytomegalie-Virus(CMV)-Erkrankungen eingesetzt. Die Substanzen sollen Aciclovir überlegen sein. Bei Ganciclovir ist zu bedenken, dass es eine Knochenmarkdepression auslösen kann [7, 8].
Cotrimoxazol. Cotrimoxazol wird zur Prophylaxe der Pneumocystis-jirovecii(PCJ)-Pneumonie und bei Nierentransplantierten auch zur Vermeidung von Harnwegsinfekten eingesetzt. Die vorgeschlagene Dosis beträgt 480 mg täglich für sechs Monate nach Transplantation [9]. Eine Alternative zu Cotrimoxazol zur PCJ-Prophylaxe ist Pentamidin zur Inhalation, welches aber den üblichen Substanzen nicht überlegen ist [7].
Antimykotika. Topische und systemische Antimykotika werden zur Vermeidung von oesophagialen Candida-Infektionen verwendet. Eingesetzt werden als Substanzen Nystatin, Amphotericin B und Pimafucin. Die Dauer der Prophylaxe liegt zwischen ein und sechs Monaten, in einigen Fällen werden auch zwölf Monate empfohlen.
Systemische Pilzinfektionen. Als Therapieoptionen stehen sowohl Itraconazol und Fluconazol als auch Amphotericin B und Voriconazol sowie Posaconazol zur Verfügung. Die Auswahl der jeweiligen Substanz orientiert sich am Erregerspektrum. Der Vorteil von Posaconazol und Voriconazol liegt in ihrer Wirksamkeit auch gegen Aspergillus-Arten. Die Dauer der Therapie richtet sich nach dem Schweregrad der zugrunde liegenden Erkrankung und dem klinischen Ansprechen [10].
Tabelle 2 zeigt eine Übersicht der verschiedenen Formen der Prophylaxe.
| Erreger | Überprüfungsintervalle | Prophylaxe/Therapie |
|---|---|---|
| BK-Polyoma-Virus | monatliche Überprüfung (drei bis sechs Monate nach Tx), alle drei Monate bis zum Ende des 1. Jahres, immer wenn Serumcreatinin ungewöhnlich ansteigt und nach Behandlung einer akuten Abstoßung | Reduktion der Immunsuppressiva,wenn Virenlast >107 Kopien |
| Cytomegalie-Virus (CMV) | bei CMV-Infektion wöchentliche Überprüfung | Prophylaxe mit oralem Valganciclovir oder Ganciclovir für drei Monate nach Tx oder für sechs Wochen nach Behandlung mit T-Zell-Antikörpernkeine Prophylaxe, wenn Donor und Rezipient eine CMV-negative Serologie aufweisen |
| Epstein-Barr-Virus (EBV) | Überwachung, wenn D+ und R- | Reduktion der Immunsuppressiva bei steigender Viruslast bei EBV-seronegativen RezipientenDosisreduktion oder Absetzen bei Erkrankung |
| Herpes-simplex-Virus 1 und 2 | bei Verdacht | oberflächliche Infektionen mit Aciclovir oder Valaciclovir therapieren, bis Läsionen ausgeheilt |
| Varizella-zoster-Virus | bei Verdacht | Therapie mit IV oder oralem Aciclovir, Valaciclovir und vorübergehende Reduktion der Immunsuppressiva |
| Pneumocystis-jirovecii-Pneumonie | besonders bei Sirolimus-Gabe, hochdosierter Immunsuppression, Abstoßungstherapie | Cotrimoxazol 480 mg dreimal/Woche bzw. täglich (je nach Zentrum) für vier Monate, Alternative Pentamindin-Inhalation einmal/Monat |
| Harnwegsinfekte | Cotrimoxazol 480 mg für sechs Monate als Prophylaxe, Therapie mit IV-Antibiotika | |
| Tuberkulose | Verdacht oder Vorgeschichte → Rö-Thorax | Isoniazid (INH) 5 mg/kg/Tag + Vitamin B6 100 mg/Tagbei Vorgeschichte und Reisen in Länder mit hoher Durchseuchungsrate für sechs bis zwölf Monate, je nach Höhe der Immunsuppression |
| Candida-Prophylaxe | erhöhte Immunsuppression oder nach Abstoßungsbehandlung | Nystatin, Pimafucin oder Amphotericin B drei- bis viermal täglich |
D+ = Donor positiv; R- = Empfänger negativ; Tx = Transplantation | ||
Abstoßungsreaktionen
Als erste Empfehlung zur Therapie von Abstoßungsreaktionen gelten Glucocorticoide in hoher Dosierung (Methylprednisolon 250 bis 500 mg/d für drei Tage). Empfohlen wird dann gegebenenfalls eine Umstellung von Ciclosporin auf Tacrolimus. Je nach Art der Abstoßungsreaktion werden auch Antikörper eingesetzt.
AMTS-Hinweise
Allen Substanzen gemeinsam ist, dass eine regelmäßige Einnahme unabdingbar für einen Therapieerfolg ist und bei jedem einzelnen Präparat die Galenik zu beachten ist. Zu beachten sind auch viele CYP-Interaktionen der Immunsuppressiva, insbesondere mit CYP3A4. Außerdem sollten die Patienten und bei Kindern auch die Eltern oder Betreuer auf das Infektionsrisiko hingewiesen werden. Eine engmaschige Überwachung und regelmäßige Kontrollen sind notwendig. Tabelle 3 gibt einen Überblick über einzelne Parameter, die überprüft werden sollen und die jeweiligen Zeitabstände.
| Test/Untersuchung | Intervalle nach Transplantation | |
|---|---|---|
| sieben bis zwölf Monate | > zwölf Monate | |
| Blutdruck, Puls, Größe, Gewicht, BMI | bei jedem Kontrolltermin | |
| Creatinin und GFR | monatlich | alle zwei bis drei Monate |
| Urinprotein und/oder Albumin im Urin | alle drei Monate | jährlich |
| großes Blutbild | monatlich | jährlich |
| Nüchternblutzucker, HbA1c, Glu-Toleranztest | alle drei Monate | jährlich |
| Lipide (nüchtern) | - | jährlich |
| BK-Polyoma-Virus | alle drei Monate | - |
| Epstein-Barr-Virus | alle drei Monate | - |
| Rauchen | - | jährlich |
Auf eine nicht abgesprochene Selbstmedikation sollte in den meisten Fällen verzichtet werden. Unter der Therapie mit Ciclosporin, aber auch mit Tacrolimus, ist eine gute Mundhygiene, unter Umständen unter Einbeziehung des Zahnarztes, unverzichtbar. Da unter Calcineurin-Inhibitoren eine erhöhte Inzidenz von Melanomen beobachtet wurde, ist die Anwendung eines Sonnenschutzes mit hohem Lichtschutzfaktor empfehlenswert. Die Galenik der einzelnen Arzneimittel ist ebenfalls zu beachten, auch im Hinblick auf die Einnahmezeitpunkte. Bei der Abgabe sind die Regelungen des Substitutionsverbotes zu beachten. So wird sichergestellt, dass immer dasselbe Präparat abgegeben wird und schwankende Spiegel werden vermieden. Ein Austausch im Rahmen von Rabattverträgen sollte bei diesen Präparaten gegebenenfalls unter Angabe pharmazeutischer Bedenken unterbleiben.
Als weiterer wichtiger Punkt ist das Einhalten von Impfempfehlungen ein wichtiger Beratungsaspekt in der Apotheke, ebenso wie die Unterstützung bei der Tablettengabe und einer fortlaufenden Analyse der Interaktionen.
2. Kapitel
Umfassende Medikationsanalyse
Kurzbeschreibung des Patienten (S)
Mathias Hoffmann ist ein 15-jähriger Patient nach erfolgreicher Nierentransplantation. Er leidet an einer invasiven Pilzinfektion und Gingiva-Hyperplasie. Probleme bestehen mit der Einnahme von Noxafil®-Suspension.
Objektive Parameter und relevante Ziele (O)
siehe Kasten „Vitalparameter und Laborwerte“
Gingiva-Hyperplasie
Befund (A)
Ziel
- Vermeidung der Gingiva-Hyperplasie
- Interaktionsmanagement
- Sicherstellung der Adhärenz
Abweichungen und leitliniengerechte Therapie
Laut dem Plan der Ambulanz bekommt der Patient Valcyte® 500 mg zweimal täglich. Valcyte® gibt es nicht mit 500 mg Valganciclovir. Mit 500 mg auf dem Markt ist Valtrex®, das aber als Wirkstoff Valaciclovir enthält, das nicht optimal zur CMV-Prophylaxe geeignet ist. Auf Grund der ähnlichen klingenden Handelsnamen und Inhaltsstoffe ist es zu einer Verwechslung gekommen Valcyte® (Valganciclovir) wird mit 450 mg zweimal täglich verabreicht. Die Dosisberechnung erfolgt hierbei nach der Formel 7 × KOF × CrCl (nach Schwartz). Danach ist eine Dosis von 1250 mg anzusetzen, die maximale Tagesdosis liegt aber dann bei 900 mg. Entsprechend sollte der Plan auf 450 mg Valganciclovir zweimal täglich abgeändert werden. Laut Leitlinie erfolgt die Therapie nach Nierentransplantation mit einem Calcineurin-Inhibitor, einem Antimetaboliten und Steroiden. Unter Mycophenolat traten deutlich mehr virale Infekte und ein möglicherweise erhöhtes Risiko von onkologischen Erkrankungen auf. Bei geringem immunologischem Risiko ist auch eine Monotherapie mit Tacrolimus möglich [11, 12].
Handhabungsprobleme. Matthias Mutter wünscht sich Noxafil®-Tabletten statt einer Suspension. Da Tabletten mit 100 mg Posaconazol zur Verfügung stehen, könnte hier umgestellt werden. Die Dosierung entspricht jedoch nicht den Angaben aus der Fachinformation, dort sind 300 mg Posaconazol einmal täglich angegeben, jedoch wird häufig eine andere Dosierung nach den entsprechenden Protokollen der einzelnen Behandlungszentren angesetzt. Bevor die Umstellung erfolgt, sollte dieser Umstand mit dem behandelnden Transplantationszentrum abgeklärt werden, jedoch ohne die Mutter zu verunsichern. Es sollte kein stetiger Wechsel zwischen Suspension und Tabletten stattfinden, aufgrund der unterschiedlichen Resorption.
Therapieziel. Die Harnsäurespiegel sind bei dem Patienten sehr hoch, so dass eine Therapie mit Allopurinol angesetzt werden sollte. Aufgrund der vorherigen Hautreaktion auf Voriconazol (V-fend®) wird Allopurinol einschleichend mit 100 mg/d, Steigerung in wöchentlichen Abständen auf bis zu 300 mg/d dosiert.
Nebenwirkungen. Ein Mundwasser ist nicht die optimale Therapie der Gingiva-Hyperplasie. Je nach Schweregrad sollte über eine Umstellung auf Tacrolimus nachgedacht werden, da die Hyperplasie eine häufige und spezifische Nebenwirkung von Ciclosporin ist.
Interaktionen. Weiterhin sind die Ciclosporin-Spiegel recht hoch, was an der Interaktion mit Posaconazol liegen könnte (CYP3A4- und P-gp-Hemmung) [13]. Auch hier kann sich eine Umstellung auf Tacrolimus positiv auswirken. Zu erzielende Tal-Spiegel sollten zwischen 5 und 15 ng/ml liegen. Wird Allopurinol angesetzt, sind ebenfalls keine Interaktionen mit Tacrolimus zu erwarten, ganz im Unterschied zu Ciclosporin. Allopurinol sollte angesetzt werden, nachdem die Umstellung auf Tacrolimus erfolgt ist. Die Umstellung erfolgt unter Spiegel-Kontrolle. Am Abend wird die letzte Ciclosporin-Dosis verabreicht, dann wird die Tacrolimus-Therapie mit 0,08 bis 0,1 mg/kg/Tag verteilt auf zwei Dosen begonnen. Am 3. Tag werden die Tacrolimus-Tal-Spiegel gemessen und dann je nach Spiegel weiter dosiert.
Auch bei Prednisolon sind höhere Spiegel zu erwarten. Hier wird die Therapie jedoch ohnehin herunterdosiert, daher ist keine akute Intervention notwendig. Durch den Einsatz von Methylprednisolon hätte man dieses Problem jedoch von vorneherein ausschalten können, da Methylprednisolon nur in sehr geringem Umfang über CYP3A4 verstoffwechselt wird.
Sonstige Hinweise. Einnahmehinweise und Handhabung sind bei diesen Tabletten wichtig. So sollte Tacrolimus unbedingt nüchtern und sofort nach der Entnahme aus dem Blister eingenommen werden. Auch sollten die Kapseln, ebenso wie die Noxafil®-Tabletten, auf keinen Fall geteilt oder anders manipuliert werden. Vigantoletten® müssen unbedingt im Umkarton aufbewahrt werden. Bei Noxafil® und auch Valcyte® sollte die Einnahme zum Essen erfolgen. Ein Einnahmeplan mit diesen Hinweisen ist zu erstellen.
Plan (P)
siehe Tabelle 4
| Arzneistoff | Dosierung | Kommentar | Behandlungsgrund |
|---|---|---|---|
| Tacrolimus Kapseln | 2 mg-0-2 mg eine Stunde vor oder zwei Stunden nach dem Essen | Dosierung nach Blutspiegel | Nierentransplantation |
| Valganciclovir 450 mg | 1-0-1 zum Essen | Dauer je nach Therapieprotokoll | CMV-Prophlaxe |
| Posaconazol 100 mg Tabletten | 2-0-2 zum Essen | Dauer je nach Ansprechen | Pilzinfektion |
| Prednisolon 20 mg Tabletten | 1-1-0,5 zum Essen | herunterdosieren bis auf 5 mg oder absetzen | Nierentransplantation |
| Pimafucin® LutschtablettenNatamycin | 1-1-1 eine Stunde vor oder zwei Stunden nach dem Essen | Prophylaxe ösophageale Candidose | |
| Cotrimoxazol 800/160 mg Tabletten | Di + Fr 1-0-1 zum Essen | Dauer je nach Therapieprotokoll | PCJ-Prophylaxe |
| Amlodipin 5 mg | 1-0-0 | Blutdruckkontrollen und Gewichtskontrolle | Transplantations-bedingte Hypertonie |
| Eisen-II-Sulfat 50 mg | 0-0-1 | bei Hb-Wert > 14 g/dl absetzenEinnahme vor dem Schlafen | Eisenmangelanämie |
| Allopurinol 100 mg | 0-0-1 | auf 300 mg in wöchentlichen Abständen steigern | erhöhter Harnsäurespiegel |
weitere Interventionen:
- Medikationsplan erstellen mit Einnahmezeitpunkten und Handhabung
- Grippeschutzimpfung, aber nicht vor sechs Monaten nach Transplantation, keine Lebendimpfungen
- Einhaltung von Hygienemaßnahmen
Monitoring
siehe Tabelle 5
| Parameter | Zeitpunkt | Zielwerte | durch wen | Maßnahmen |
|---|---|---|---|---|
Überwachung der Wirksamkeit | ||||
| GFR | von wöchentlich während der Monate 2 bis 3 bis alle zwei bis drei Monate nach zwölf Monaten | Normbereich | Arzt/Ambulanz | Therapie mit Glucocorticoiden bei Abstoßungsreaktion |
| Proteinurie | Normbereich | |||
unerwünschte Wirkungen | ||||
| Nierenschädigung | fortlaufend | GFR, Proteinurie, Gewicht | Arzt/Patient | bei Nierenschädigung Umstellung auf Sirolimus oder Everolimus |
| Melanome | fortlaufend | nicht vorhanden | Patient/Arzt | Sonnenschutz |
| opportunistische Infektionen | fortlaufend | BK-Virus, CMV, HSV, Hepatitis, PCJ, Pilzinfektionen | Arzt/Ambulanz | Therapie der jeweiligen Infektion |
| Diabetes | wöchentlich im ersten Monat, alle drei Monate für ein Jahr, dann jährlich bei Ansetzen oder Dosiserhöhung der Glucocorticoide oder chronischer Niereninsuffizienz | HbA1c 6,5 bis 7,5%Nüchternglucose < 110 mg/dl | Arzt | Dosisreduktion und/oder Therapie mit Antidiabetika |
| Hypertonie | bei jedem Arztbesuch | < 135/80 mmHg | Arzt/Ambulanz | Calciumkanal-Blocker oder ACE-Hemmer |
Schulung
Schulung
Matthias und seine Mutter sollten zu den korrekten Zeitpunkten der Einnahme und zur Lagerung der Arzneimittel geschult werden. Auch kann die entsprechende Mundhygiene und die Verwendung von Sonnenschutzmitteln (SPF 15 bis 25) angesprochen werden. Die Merkmale der unterschiedlichen opportunistischen Infektionen könnten ebenfalls besprochen werden. Eine Aufklärung über die richtigen Hygienemaßnahmen und der Umgang und richtige Einsatz einer Selbstmedikation ist sinnvoll. Ein Medikationsplan sollte erstellt und regelmäßig aktualisiert werden. Bei Fieber, Blutdruckanstieg und Schmerzen/Druckgefühl sollte sofort die Ambulanz aufgesucht werden [15].
Was wäre wenn ...?
… es sich bei diesem Patienten um einen Erwachsenen gehandelt hätte?
Bei einem erwachsenen Patienten wären die gleichen Änderungen vorgeschlagen worden.
Einige Dosierungen, wie z. B. von Tacrolimus wären entsprechend dem Körpergewicht verändert worden. Die 61 kg unseres Patienten sind aber auch für Erwachsene kein ungewöhnliches Körpergewicht. Wäre der Patient jedoch deutlich älter gewesen und hätte kardiovaskuläre Erkrankungen gehabt, so wären diese therapeutisch relevant gewesen. Bei vorliegenden atherothrombotischen Erkrankungen ist eine Gabe von 100 mg Acetylsalicylsäure täglich indiziert, es sei denn, es bestünden Kontraindikationen.
… bei diesem Patienten die LDL-Spiegel angestiegen wären?
LDL-Cholesterol–Spiegel sollen auch bei Heranwachsenden zwei bis drei Monate nach der Transplantation und dann jährlich bestimmt werden [3]. Wird der Grenzwert (bei Erwachsenen ein LDL-Cholesterol von > 100 mg/dl, bei Jugendlichen > 130 mg/dl) überschritten, sollten, wie bei allen anderen Patienten auch, Änderungen der Lebensgewohnheiten angeregt werden. Kommt es darunter nicht zu einer ausreichenden Reduktion der Werte, sind Statine auch in dieser Patientengruppe indiziert. Auch wenn Simvastatin im vorliegenden Fall kein Interaktionspotenzial aufweist, wäre Atorvastatin die bessere Variante. Wäre noch Ciclosporin als Immunsuppressivum vorgesehen würde optimalerweise mit Pravastatin therapiert [14].
… Posaconazol (Noxafil®) abgesetzt worden wäre?
Da unter der Posaconazol-Therapie die Tacrolimus-Dosierungen reduziert sind (ca. 1/3) müssten beim Absetzen die Dosierungen unter engmaschiger Spiegel-Kontrolle neu angepasst werden [9].
… man im vorliegenden Fall keine Daten vom Arzt vorliegen gehabt hätte?
Die Umstellung von Noxafil® Suspension auf Tabletten wäre auch ohne Laborwerte möglich gewesen, ebenso wie die Detektion der Gingiva-Hyperplasie als Nebenwirkung von Ciclosporin. Die Notwendigkeit einer Therapie mit Allopurinol wäre ohne Laborwerte nicht aufgefallen, ebenso wie die Beurteilung der Auswirkungen der Posaconazol-Gabe auf die Ciclosporin-Spiegel.
Medikationsmanagement
Medikationsmanagement
Tacrolimus wurde bei dem Patienten angesetzt und auf einen Tal-Spiegel von 10 ng/ml eingestellt. Die Gingiva-Hyperplasie hat sich zurückentwickelt. Allopurinol ist mit 100 mg als Startdosis angesetzt worden. Eine Kontrolle der Harnsäurespiegel lag noch nicht vor. Mit dem neuen Einnahmeplan wurden die Einnahmezeitpunkte von Tacrolimus auf alle zwölf Stunden festgelegt. Ein Blutdruckmessgerät mit einer Kindermanschette wurde angeschafft, um die Selbstkontrolle zu verbessern. Die Namensproblematik Valcyte®/Valtrex® wurde geklärt. Der Patient bekommt Valcyte® 450 mg zweimal täglich. Der Medikationsplan wurde ebenfalls entsprechend angepasst. Auch der Einnahmezeitpunkt von Ferrosanol® wurde in dem neuen Plan auf abends vor dem Schlafen festgelegt. Hygienemaßnahmen wurden mit Matthias besprochen, ebenso wie die Anwendung von Sonnencreme mit einem Lichtschutzfaktor von 25. Auch die Notwendigkeit des Verzichts auf Zigaretten und Alkohol wurde diskutiert. Aufgrund der Pilzinfektion wurde auch noch einmal auf Maßnahmen zur Vermeidung von Fußpilz hingewiesen. |
Literatur
[1] Homepage des National Kidney Disease Education Program (NKDEP) und des The National Institute of Diabetes and Digestive and Kidney Diseases (NIDDK), verfügbar unter http://nkdep.nih.gov/lab-evaluation/gfr-calculators/children-SI-units.asp, erfasst am 8. Mai 2015
[2] Rieger S, Tönshoff B, Schmidt. Nierentransplantation. Informationsbroschüre zum nierenkranken Kind, verfügbar unter https://www.klinikum.uni-heidelberg.de/fileadmin/Chirurgie/transplantationszentrum/PDF/broschuere_transplantation_230407.pdf, , erfasst am 8. Mai 2015
[3] Kasiske BL et al. KDIGO clinical practice guideline for the care of kidney transplant recipients: a summary. Int Soc of Nephr 2009;10:1-13
[4] Schonder KS, Johnson HJ. Solid-Organ Transplantation. In DiPiro JT. Pharmacotherapy- A pathophysiologic approach. McGraw Hill Medical. New York, 9th Edition 2014
[5] Augustine JJ Bodziak KA, Hricik DE. Use of sirolimus in solid organ transplantations. Drugs 2007;67:369-391
[6] Grim SA, Clark NM. Management of infectious complications in solid-organ transplant recipients. Clin Pharmacol Ther 2011;51:1530-1535
[7] National Comprehensive Cancer Network. Prevention and treatment of cancer-related infections. Clinical Practice Guidelines in Oncology (NCCN Guidelines®), Januar 2012, www.nccn.org/professionals/physician_gls/pdf/infections.pdf. Erfasst am 10. Mai 2015
[8] Tomblyn M, Chiller T, Einsele H et al. Guidelines for preventing infectious complications among hematopoetic cell transplantation recipient: A global perspective. Biol Blood Marrow Transplant 2009;15:1143-1238
[9] Suwelak B. Immunsuppression nach Nierentransplantation –Therapieleitlinien. www.klinikum.uni-muenster.de, Stand November 2005. Erfasst am 9. Mai 2015
[10] Fachinformation Noxafil®, Stand September 2014, www.fachinfo.de. Erfasst am 10. Mai 2015
[11] Raheem OA et al. Mycophenolate mofetil in pediatric renal transplantation: A single center experience. Paed Transpl 2011;15:240-244
[12] Peruzzi L, Amore A, Coppo R. Challenges in pediatric renal transplantation. World J Transplant 2014;4(4):222-228
[13] Saad AH, DePestel DD, Carver PL. Factors Influencing the Magnitude and Clinical Significance of Drug Interactions Between Azole Antifungals and Select Immunosuppressants. Pharmacotherapy, 2006;26(12):1730-1744
[14] Gumprecht J, Zychma M, Grzeszczak W et al. Simvastatin-induced rhabdomyolysis in a CsA-treated renal transplant recipient. Med Sci Monit, 2003,9(9):89-91
[15] Nef S, Laube G. Patientenbetreuung nach Nierentransplantation bei Kindern. Paediatrie 2013;18(3):42
[16] Suwelack B. Immunsuppression nach Nierentransplantation – Therapieleitlinie UKM, November 2005
Autoren
Isabel Waltering,Doctor of Pharmacy (USA), Studium der Pharmazie von 1987 bis 1992 an der WWU in Münster, Referentin für verschiedene Apothekerkammern im Bereich Fort- und Weiterbildung. Studium an der University of Florida, Gainesville mit dem Abschluss PharmD. Prüfungsausschuss Geriatrische Pharmazie (AKWL und LAK BW), Wissenschaftliches Mitglied und Mitinitiatorin der WestGem-Studie (MTM und sektorübergreifende Versorgungsforschung bei multimorbiden Patienten) in Zusammenarbeit mit der Bergischen Universität Wuppertal und der KatHO-NRW. Mitarbeiterin in der Ludgeri-Apotheke in Billerbeck. Wissenschaftliche Mitarbeiterin im Arbeitskreis von Prof. Hempel in Münster als AMTS-Dozentin.
Isabel Waltering, PharmD, Siemensstraße 9, 48301 Nottuln
Dr. med. Susanne Koling hat an der Westfälischen Wilhelms-Universität Münster Medizin studiert. Seit 2001 ist sie am Universitätklinikum Münster, Klinik und Poliklinik für Kinder- und Jugendmedizin, in verschiedenen Bereichen der Pädiatrischen Hämatologie und Onkologie sowie der Allgemeinen Pädiatrie tätig.
Dr. med. Susanne Koling, susanne.koling@gmx.de
Olaf Rose,Studium der Pharmazie in Münster, Forschungsaufenthalt bei Bayer, Japan, Studium zum Doctor of Pharmacy an der University of Florida, USA. Wissenschaftliches Mitglied der WestGem-Studie. Herausgeber des Buches „Angewandte Pharmakotherapie“ zusammen mit Prof. Dr. Kristina Friedland. PCNE-Mitglied seit 2015. Inhaber dreier Apotheken in Münster und im Münsterland.
Olaf Rose, PharmD, rose@elefantenapo.de
Hartmut Derendorfist Distinguished Professor und Chairman des Departments of Pharmaceutics an der University of Florida in Gainesville, wo er seit 1983 Pharmakokinetik, Pharmakodynamik und Klinische Pharmakokinetik lehrt.
Prof. Dr. Hartmut Derendorf, University of Florida, 100494, College of Pharmacy, 1600 SW Archer Road, P3-27, Gainesville, FL 32610, hartmut@cop.ufl.edu

































0 Kommentare
Das Kommentieren ist aktuell nicht möglich.