
- DAZ.online
- News
- Pharmazie
- Ocrelizumab in USA ...
Neues Arzneimittel bei MS
Ocrelizumab in USA zugelassen
29.03.2017, 16:20 Uhr
Ocrelizumab soll als CD20-Antikörper gegen B-Zellen die entzündliche Zerstörung der Myelinscheide im ZNS verlangsamen. (Foto: ag visuell / Fotolia)
Roche hat in den USA die Zulassung für seinen neuartigen MS-Antikörper Ocrelizumab erhalten. Ocrevus ist das erste Arzneimittel gegen primär progrediente MS. In einem beschleunigten Zulassungsverfahren hat die FDA nun Patienten in den Vereinigten Staaten den Zugang zur neuen Therapie geschaffen. Wann gibt es Ocrelizumab in Deutschland? Und wie kommen deutsche Patienten heute schon an das neue Arzneimittel gegen MS?
Mit einem neuen Arzneimittel gegen Multiple Sklerose will Roche die Therapie von MS-Patienten verbessern. In den Vereinigten Staaten erhielt der Antikörper Ocrelizumab die Zulassung zur Therapie der primär progredienten MS (PPMS) und der remittierend schubförmig verlaufenden MS (RRMS). Die Studien-Daten zum OcrevusTM überzeugten die FDA: Die amerikanische Zulassungsbehörde ermöglichte durch eine beschleunigte Zulassung – Prioritiy-Review-Verfahren – den Patienten die schnellstmögliche Verfügbarkeit der neuen Therapieoption mit OcrevusTM.
Was ist das Besondere an Ocrelizumab?
Ocrelizumab ist das erste und einzige Arzneimittel, das gegen beide Verlaufsformen der Multiplen Sklerose, also die schubförmige und die primär progrediente, wirkt. Insbesondere für Patienten mit primär progredienter MS ist OcrevusTM ein Therapie-Durchbruch: Diese Unterform der Multiplen Sklerose galt bis dato als nicht behandelbar. Etwa zehn bis 15 Prozent der Patienten leiden an der primär progredienten Form.
Im Gegensatz zur remittierend schubförmigen MS entwickeln sich die neurologischen Symptome bei der PPMS eher schleichend. Die PPMS beginnt meist erst in einem Alter von 40 bis 50 Jahren und trifft Männer und Frauen mit gleicher Häufigkeit – bei der RRMS erkranken Frauen im Schnitt dreimal häufiger als Männer. Auch beginnt die RRMS meist früher im Alter zwischen 20 und 40 Jahren.
Wie wirkt Ocrelizumab?
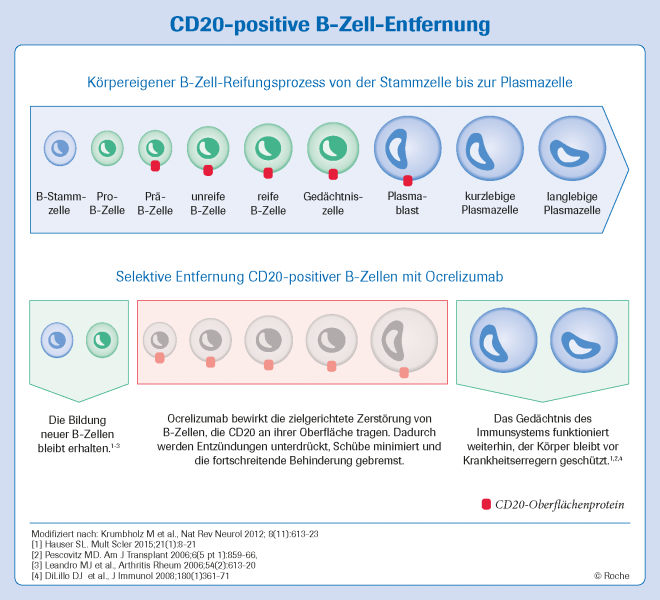
Als humanisierter, monoklonaler Antikörper richtet sich Ocrelizumab gegen das auf B-Zellen exprimierte, glykosylierte Phosphoprotein CD20. B-Zellen spielen – als Aktivatoren autoreaktiver T-Zellen – eine wichtige Rolle in der Pathogenese der Multiplen Sklerose. MS ist eine neurologische Erkrankung. Durch immunvermittelte chronische Entzündungen des Zentralnervensystems kommt es hier zu Demyelinisierung und fortschreitender Behinderung. In Deutschland sind etwa 200.000 Patienten betroffen, weltweit sind es rund 2,3 Millionen.
Wie wenden MS-Patienten Ocrevus an?
Patienten können OcrevusTM nicht selbst spritzen. Ocrelizumab muss vom Arzt verabreicht werden. Alle sechs Monate erhalten MS-Patienten eine Infusion mit 600 mg des Antikörpers. Die Startdosis wird in zwei Dosen zu je 300 mg aufgeteilt und in zweiwöchigem Abstand infundiert.
Wann gibt es Ocrevus in Deutschland?
Roche hat die Zulassungsunterlagen für Ocrevus auch bei der EMA eingereicht. „Wir rechnen noch in diesem Jahr mit der Zulassung für Ocrelizumab in der EU“, sagt Roche auf Anfrage von DAZ.online. Genau beziffern könne man das Datum allerdings leider nicht. Auch hat Roche bei der europäischen Arzneimittelagentur EMA keine beschleunigte Zulassung für seinen neuen Antikörper wie bei der FDA beantragt.
Das EMA-Äquivalent zum US-amerikanischen Priority-Review-Verfahren heißt Accelerated Access Review. Eine EU-weite beschleunigte Zulassung werde von der EMA nur akzeptiert, wenn die „Dringlichkeit gegeben ist“, erklärt Roche. Für eine der beiden Indikationen – die RRMS – haben Patienten bereits alternative Arzneimittel.
Was kostet Ocrelizumab?
Roche hält sich auf DAZ.online-Nachfrage bedeckt. Hierzu könne und dürfe man derzeit noch keine Angaben machen. „Das ist alles noch im Verfahren und wird noch verhandelt“, sagt eine Sprecherin von Roche.
Wie kommen PPMS-Patienten in Deutschland schon an Ocrevus?
Bereits heute gibt es für Patienten mit primär progredienter MS die Möglichkeit, eine Therapie mit dem neuen Antikörper zu erhalten. Im Rahmen eines Härtefallprogramms – Compassionate Use Program (CUP) – steht Ocrelizumab Patienten unter bestimmten Voraussetzungen seit Februar 2017 zur Verfügung. Solch ein CPU ermöglicht die Behandlung mit neuen und noch nicht zugelassenen Arzneimitteln. Die Voraussetzung: Die Krankheit muss schwer bis lebensbedrohlich sein, und es darf keine zufriedenstellende Behandlungsoption für die Patienten geben – was bei PPMS der Fall ist.
„Die Entscheidung über die Teilnahme am Härtefallprogramm für Ocrelizumab ist eine Einzelfall-Entscheidung“, erklärt Roche. Sie erfolge in Abstimmung mit dem behandelnden Arzt, Roche und in Abhängigkeit von lokalen Regularien und Gesetzen. Für Patienten ist die Teilnahme am Ocrelizumab-CPU kostenlos. Allerdings müssen sie sich vor Beginn der OcrevusTM-Therapie schriftlich einverstanden erklären. MS-Patienten, die Fragen zum Härtefallprogramm haben, können sich an die „Medical Information“ von Roche wenden.
Roche betont, dass die Ocrelizumab-Therapie im Rahmen des CUP zur Überbrückung bis zur offiziellen Zulassung von OcrevusTM auch nur für Patienten mit PPMS möglich ist. Patienten, die an schubförmig remittierender Multipler Sklerose leiden, haben zugelassene Therapie-Alternativen.


















10 Kommentare
M.S
von Adrian Ivescu Abager am 24.08.2017 um 22:50 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
PPMS
von Heike Kohl am 22.08.2017 um 12:17 Uhr
» Auf diesen Kommentar antworten | 1 Antwort
AW: PPMS
von Celine Müller am 23.08.2017 um 8:50 Uhr
Zulassung
von Angelika Kiefer am 22.08.2017 um 8:49 Uhr
» Auf diesen Kommentar antworten | 1 Antwort
AW: Zulassung
von Celine Müller am 23.08.2017 um 8:46 Uhr
Ocrelizumab ja oder nein
von Gabriele Hagmeyer am 28.07.2017 um 20:48 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Ocrelizumab
von Gebhardt am 06.04.2017 um 15:02 Uhr
» Auf diesen Kommentar antworten | 1 Antwort
AW: Ocrelizumab
von Celine Müller am 06.04.2017 um 16:01 Uhr
frage
von Wasner Silvia am 01.04.2017 um 12:10 Uhr
» Auf diesen Kommentar antworten | 1 Antwort
AW: frage
von Celine Müller am 06.04.2017 um 15:52 Uhr
Das Kommentieren ist aktuell nicht möglich.