
- DAZ.online
- News
- Pharmazie
- Forscher beschreiben ...
Neue Ansätze für die Insulintherapie?
Forscher beschreiben Bindungsstelle 2 des Insulinrezeptors
Remagen - 29.11.2019, 16:30 Uhr
Wie und wo wirkt Insulin? Dazu haben Forscher kürzlich ein weiteres Puzzleteil analysieren können. (m / Foto: imago images / Jochen Tack)
Vom „U“ zum „T“
Mit diesen Verfahren gelang es den Forschern laut eigener Aussage erstmals, die Bindung von Insulin an der zweiten Bindungsstelle direkt zu beobachten und zu zeigen, wie der Insulinrezeptor seine Konformation zu einer T-förmigen Struktur verändert. Dass der Rezeptor nach Bindung von Insulin vom „U“ zum „T“ transformiert wird, hatte ein ähnlich zusammengesetzte Gruppe vom Paul-Langerhans-Instituts Dresden mit Kollegen der New Yorker Rockefeller University erst vor eineinhalb Jahren erstmals beschrieben.
Sie hatte gezeigt, dass der Rezeptor in Abwesenheit von Insulin die Gestalt eines umgekehrten „U” aufweist, wobei die Kinasedomänen an den beiden Enden voneinander getrennt sind. Bei der Bindung an den Rezeptor löst das Insulin eine umfassende Restrukturierung von der „U“ in eine „T-Form“ aus. Dabei kommen die Kinasaenden miteinander in Berührung, womit die Signalweitergabe in Gang gesetzt wird.
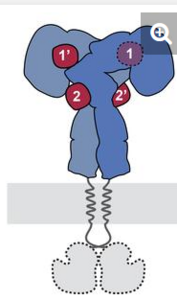
Zwei identische Teile mit jeweils zwei Insulinbindungsstellen
„Der Schlüssel lag darin, den äußeren Teil des Insulinrezeptors zu untersuchen, nachdem er mit hohen Insulinkonzentrationen gesättigt wurde“, erläutert die Mitautorin der Studie Theresia Gutmann vom Paul-Langerhans-Institut. Dafür hätten die Forscher mehr als 8.000 elektronenmikroskopische Bilder aufgenommen und mehr als 300.000 einzelne Rezeptorpartikel analysiert, fügt Co-Autor Ingmar Schäfer von der Abteilung Strukturzellbiologie am Max-Planck-Institut für Biochemie (MPIB) an. So konnten die Wissenschaftler erstmals die Struktur der gesamten dimeren Ektodomäne des Insulinrezeptors, gesättigt mit vier Insulin-Molekülen, darstellen. Nach ihrer Beschreibung besteht der Rezeptor aus zwei identischen Teilen, die jeweils zwei Insulinbindungsstellen enthalten.
Die Forscher hoffen nun, dass diese neuen Details zu den Interaktionen zwischen Insulin und seinem Rezeptor die bisherigen Modelle der Insulinbindung erweitern können. Sie könnten damit den Weg für neue Ansätze des strukturbasierten Wirkstoffdesigns ebnen.




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.