
- DAZ.online
- News
- Apotheke
- „Big Data ebnen den Weg...
Globale Kampagne zur MEldung von Nebenwirkungen
„Big Data ebnen den Weg, Arzneimittel noch sicherer zu machen“
Stuttgart - 03.12.2019, 15:19 Uhr
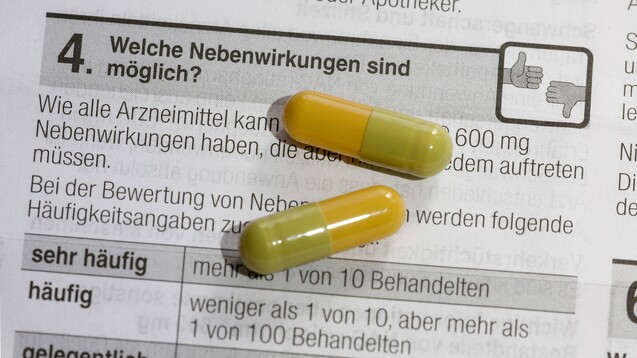
In klinischen Studien können nie alle Nebenwirkungen entdeckt werden, damit Arzneimittel sicherer werden, ist es deswegen wichtig, unerwünschte Arzneimittelwirkungen zu melden. Daran erinnern in einer gemeinsamen Kampagne weltweit die Behörden. ( r / Foto: imago images / Arnulf Hettrich)
Eine Behandlung mit mehreren Arzneimitteln birgt stets das Risiko für Wechselwirkungen und unerwünschte Arzneimittelreaktionen. Für ein Höchstmaß an Arzneimittelsicherheit ist es daher wichtig, alle vermuteten Nebenwirkungen behördlich zu melden. Dazu fordern – mittlerweile zum vierten Mal – weltweit die Arzneimittelbehörden in einer gemeinsamen Kampagne auf. Medizinisches Fachpersonal, wie Ärzte und Apotheker, und Patienten sollen so für Polypharmazie sensibilisiert werden.
Weltweit fordern Arzneimittelbehörden in einer gemeinsamen Kampagne dazu auf, ihnen Verdachtsfälle von Nebenwirkungen über die behördlichen Meldewege mitzuteilen. Bereits zum vierten Mal findet diese Kampagne statt, insgesamt partizipieren 57 Arzneimittelbehörden. Unterstützt wird die Kampagne unter anderem von der Weltgesundheitsorganisation (WHO), der Europäischen Kommission sowie der Europäischen Arzneimittel-Agentur (EMA).
Polypharmazie birgt Risiko für unerwünschte Wirkungen
Anliegen der diesjährigen Kampagne ist es, medizinisches Fachpersonal und auch Patienten und deren Angehörige für Risiken der Polypharmazie zu sensibilisieren und dafür, „dass eine gleichzeitige Behandlung mit mehreren verschiedenen Arzneimitteln möglicherweise auch zu unerwünschten Reaktionen führen kann“, heißt es in einer Mitteilung des Bundesinstitutes für Arzneimittel und Medizinprodukte (BfArM). Und weiter: „Für ein Höchstmaß an Arzneimittelsicherheit ist es daher wichtig, alle vermuteten Nebenwirkungen behördlich zu melden“. In Deutschland nehmen sowohl das BfArM als auch das Paul-Ehrlich-Institut (PEI) Meldungen zu Verdachtsfällen von unerwünschten Arzneimittelwirkungen entgegen.
„Um mögliche Risiken von Arzneimitteln früh identifizieren zu können, spielen die Meldungen eine große Rolle“, das erklärt Prof. Dr. Karl Broich, Präsident des BfArM. „Bei der Auswertung dieser Daten wird auch die Nutzung Künstlicher Intelligenz immer stärker an Bedeutung gewinnen, beispielsweise, um die Qualität der Meldungen automatisch zu bewerten. Alle Maßnahmen dienen dazu, Erkenntnisse über die Anwendung und den Gebrauch von Arzneimitteln zu gewinnen. So ist jede Meldung auch ein Beitrag für den Patientenschutz.“
Sicherere Arzneimittel durch Meldung von Nebenwirkungen
Auch der Präsident des PEI, Professor Klaus Cichutek, betont die Wichtigkeit der Meldung von Nebenwirkungen: „Das Erfassen großer Datenmengen ist eine Voraussetzung, um das Nutzen-Risiko-Profil präziser einzuschätzen und Signale zu erkennen. Big Data ebnen den Weg, Arzneimittel noch sicherer zu machen.“
Nur über BfArM- und PEI-Portale melden
Häufig sei den Menschen nicht bewusst, dass Arzneimittel sich gegenseitig beeinflussen oder ihre Kombination unerwünschte Reaktionen hervorrufen kann. Je mehr Arzneimittel Patienten für unterschiedliche Krankheiten einnähmen, desto mehr sollten sie darauf achten, ob neue Symptome aufträten und diese als Verdacht einer Nebenwirkung an die Behörden melden, erläutert Cichutek.
Die Verdachtsfälle erreichten dort schnell, direkt und sicher die Experten für Arzneimittelsicherheit und gelangten in die zentrale „Europäische Datenbank gemeldeter Verdachtsfälle von Arzneimittelnebenwirkungen. Mit dieser Datenbank steht ein umfangreicher Datenpool zur Verfügung, der es erlaubt, Arzneimittelrisiken EU-weit zu überwachen. „Nur über das gemeinsame Online-Meldeportal von BfArM und PEI kann in Deutschland sichergestellt werden, dass Verdachtsfälle von Nebenwirkungen in die EU-Datenbank einfließen", steht in der BfArM-Mitteilung. Der Datenschutz sei auf allen Meldewegen gewährleistet.
Mehr zum Thema

AMK warnt vor nebenwirkungen.de
Zusätzliche Meldewege erhöhen nicht die Meldefreudigkeit

Pharmakovigilanz
Nebenwirkungen melden – was Apotheker wissen müssen
Warum am behördlichen Nebenwirkungsmelde-System kein Weg vorbeiführt
Verdachtsfälle melden
Dies betonen die Behörden wohl, da auch ein privater Anbieter, Medikura, mit seinem Portal Nebenwirkungen.de, sehr aktiv ist und nicht nur Patienten, sondern inzwischen auch gezielt Apotheker und Ärzte zur Meldung von Nebenwirkungen auffordert. Die Verarbeitung und Vermittlung von sensiblen medizinischen Daten von einzelnen Patienten im Zusammenhang mit der Arzneimittelsicherheit durch ein gewinnorientiertes Unternehmen stößt jedoch unter anderem bei der Arzneimittelkommission der Deutschen Ärzteschaft (AkdÄ), bei der AMK und auch bei den Behörden auf vehemente Ablehnung. DAZ.online berichtete darüber.
Klinische Studien können nicht alle UAW detektieren
Viele Patienten wissen vielleicht auch nicht, dass Kenntnisse über die Sicherheit von Arzneimitteln zum Zeitpunkt ihrer erstmaligen Zulassung nicht vollständig sein können: Das Arzneimittel wird klinisch nur an einer relativ geringen Patientenzahl erprobt, sodass seltene und vor allem sehr seltene unerwünschte Wirkungen, Wechselwirkungen oder andere Risiken im Zusammenhang mit der Arzneimittelanwendung üblicherweise nicht erkannt werden können. Um beispielsweise ein Risiko von 1:1.000 zu erkennen, müssten an der klinischen Prüfung mindestens 3.000 Personen teilnehmen, erklärt das BfArM. Zudem seien Personen der klinischen Phase unter Berücksichtigung verschiedener Aspekte für die klinische Prüfung ausgewählt, was nicht notwendigerweise den Bedingungen einer breiten Anwendung des Arzneimittels entspreche.




























1 Kommentar
Arzneimittel-Verfügbarkeit
von Dr. Sauber am 04.12.2019 um 10:31 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Das Kommentieren ist aktuell nicht möglich.