
- DAZ.online
- News
- Pharmazie
- Zulassungsaus für ...
COVID-19-Impfung
Zulassungsaus für Vaxzevria – ist das ungewöhnlich?
08.05.2024, 17:00 Uhr
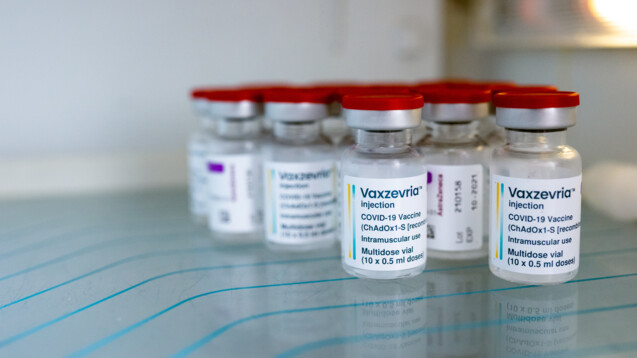
Die Rücknahme der Zulassung von Vaxzevria ist kein Einzelfall. (Foto: Sodel Vladyslav / AdobeStock)
In Deutschland wird der Corona-Impfstoff „Vaxzevria“ ohnehin schon länger nicht mehr verwendet, nun wurde auf Wunsch des Herstellers die Zulassung in der EU beendet. Warum wurde nicht einfach nur der Verkauf gestoppt, fragen sich nun manche. Doch der Schritt ist keineswegs ungewöhnlich.
Für den Corona-Impfstoff „Vaxzevria“ gibt es auf Wunsch des schwedisch-britischen Pharmaunternehmens Astrazeneca keine Zulassung in der EU mehr. Der Konzern gibt „kommerzielle Gründe“ an. In sozialen Medien wird seither über mögliche andere Ursachen spekuliert – auch wenn es von der EU-Kommission längst hieß, „dass die Entscheidung nicht auf Zweifeln an Sicherheit oder Wirksamkeit des Impfstoffes beruht“.
Womöglich ist vielen nicht klar, dass ein solcher Schritt keineswegs mysteriös ist, wie ein Fachverband erläutert: „Jährlich wird typischerweise bei 5 bis 10 Originalmedikamenten die Zulassung zurückgenommen, fast immer aus kommerziellen Gründen“, teilte Rolf Hömke, Forschungssprecher beim Verband Forschender Arzneimittelhersteller (vfa), in Berlin mit. Hintergrund sei oft, dass es mittlerweile zur Behandlung der betreffenden Krankheit noch bessere Medikamente gibt und die alten deshalb kaum noch zum Einsatz kommen und entbehrlich sind.
Mehr zum Thema

EMA und WHO empfehlen Anpassung der Corona-Impfstoffe
COVID-19: Ab Herbst wird monovalent gegen JN.1 geimpft
Bruton-Tyrosinkinase-Inhibitoren
Nach Corona-Impfung von AstraZeneca: Könnte ein Krebsarzneimittel VITT verhindern?
Zu „Vaxzevria“ hatte Astrazeneca erklärt, dass es inzwischen einen Überschuss an verfügbaren aktualisierten, also an neue Varianten angepassten Impfstoffen gebe. „Dies hat zu einem Rückgang der Nachfrage nach 'Vaxzervria' geführt, das nicht mehr hergestellt oder geliefert wird.“
Vaxzevria ist kein Einzelfall
Erst im März wurde von der Europäischen Arzneimittel-Agentur (EMA) auf Antrag des Herstellers Sanofi Pasteur die Zulassung für den Corona-Impfstoff „VidPrevtyn Beta“ beendet, im Oktober die für den Corona-Impfstoff „Valneva“ des Unternehmens Valneva Austria. In beiden Fällen wurden ebenfalls kommerzielle Gründe angegeben. Für Auffrischimpfungen zum Schutz vor schweren COVID-19-Verläufen sind inzwischen an neu aufgekommene Corona-Varianten angepasste Impfstoffe im Einsatz.
Auch bei Impfstoffen gegen andere Krankheiten gebe es Beispiele für eine Rücknahme der Zulassung, sagte Hömke. So sei etwa die Zulassung für den Impfstoff „Fluenz“ gegen saisonale Grippe (2011-2014) zurückgenommen worden, als das Nachfolgeprodukt „Fluenz4“ eingeführt wurde, das vor mehr Grippevirenstämmen schützen könne.
Warum stellen die Unternehmen nicht einfach nur die Produktion ein?
„Wir können nicht sagen, wie Unternehmen im Einzelfall zwischen einem Antrag auf Zulassungsrücknahme oder einem 'außer Vertrieb'-Stellen abwägen“, erklärte Hömke. Ein Erwägungsgrund sei aber sicherlich, dass Unternehmen eine Jahresgebühr für das Aufrechterhalten einer Zulassung bei der Arzneimittelbehörde EMA bezahlen müssen. „Ein weiterer ist, dass ein Hersteller für alle seine zugelassenen Produkte immer wieder 'Periodic Safety Update Reports' erstellen und bei der EMA anliefern muss – selbst dann, wenn er ein Produkt gar nicht vermarktet.“ Das binde Zeit und Ressourcen.
Nutzen überwiegt das Risiko
Im Frühjahr 2021 wurden „Vaxzevria“-Impfungen nach Berichten über das Thrombose-mit-Thrombozytopenie-Syndrom (TTS) und Hirnvenenthrombosen in einigen europäischen Ländern, darunter Deutschland, zeitweise ausgesetzt. Dem Paul-Ehrlich-Institut (PEI) zufolge wurden bei rund 8,5 Millionen verabreichten Impfdosen bis 25. Mai 2021 insgesamt 94 Fälle von TTS in Deutschland gemeldet, 17 Menschen starben. Zwei Drittel der Betroffenen waren jünger als 60.
Unter anderem die Arzneimittelbehörde EMA nahm die Fälle unter die Lupe. Ergebnis: Der Nutzen der Impfung überwiege eindeutig das Risiko extrem seltener potenzieller Nebenwirkungen. Bis zum Widerrufen der Zulassung mit Beschluss vom 27. März 2024 gab es eine uneingeschränkte Empfehlung der EMA.
Klagen gegen Astrazeneca
Im April erzielte eine Frau aus Oberfranken im Prozess um einen mutmaßlichen Corona-Impfschaden einen Teilerfolg gegen den Hersteller. Astrazeneca wurde zu einer umfassenden Auskunft über Nebenwirkungen von „Vaxzevria“ verurteilt. Bisher sei diese Auskunft nicht eingegangen, teilte der Anwalt der Klägerin, Volker Loeschner, am Mittwoch der Deutschen Presse-Agentur mit. Das Schadensersatz- und Schmerzensgeldverfahren der Klägerin läuft weiter. Ähnliche Klagen wurden auch andernorts eingereicht.
Schon seit längerem wird der Impfstoff hierzulande gar nicht mehr eingesetzt.





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.