
- DAZ.online
- DAZ / AZ
- DAZ 49/2022
- Was die quälende Unruhe ...
Restless-Legs-Syndrom
Was die quälende Unruhe der Beine fördert
Mit der pharmazeutischen Betreuung Probleme lösen
Die pharmazeutische Betreuung von RLS-Patienten verläuft in drei Schritten. Zunächst gilt es, anhand eines vorgelegten Rezepts von dem verordneten Arzneimittel auf die Diagnose zu schließen und die Patienten darauf anzusprechen. In den relativ häufigen Fällen, in denen das RLS die Komorbidität einer anderen chronischen Erkrankung ist, sind meist mehr als fünf Arzneimittel verordnet, was den Anspruch auf eine von der Krankenkasse bezahlte Medikationsanalyse begründet. Diese stellt den zweiten Schritt dar. Im dritten Schritt werden evidenzbasiert Nahrungsergänzungsmittel empfohlen, die geeignet sind, die Therapie effizienter und nebenwirkungsärmer zu gestalten.
Wie erkennt man RLS-Patienten am Rezept?
Im Beitrag Zieglmeier M. „Neues zu Restless Legs: Diagnostik und Therapie verändern sich durch die S2k-Leitlinie“ in dieser Ausgabe der DAZ auf S. 32 haben wir die Leitlinie vorgestellt. Anhand der darin genannten erweiterten Therapieoptionen ist es schwieriger geworden, Patienten mit einem Restless-Legs-Syndrom anhand ihrer verordneten Medikation zu identifizieren (s. Abb. 1). Gabapentin, Pregabalin und Opioide werden auch bei anderen Erkrankungen eingesetzt, und das Levodopa-Präparat, dessen Name Restex® schon unmissverständlich auf die Symptomatik eines Restless-Legs-Syndroms hinweist, verliert einen Großteil seines therapeutischen Stellenwerts. Die meisten RLS-Patienten werden jedoch nach wie vor mit Dopamin-Agonisten behandelt. Bei ihnen besteht die Aufgabe lediglich darin, die beiden Indikationen RLS und Morbus Parkinson voneinander abzugrenzen. Die zusätzliche Verordnung eines Eisen-Präparats kann der erste Hinweis auf ein RLS sein, sobald alle Hausärzte die neue Leitlinie verinnerlicht haben, in der eine Eisen-Substitution empfohlen wird [7].
Abb. 1: Ein typisches RLS-Rezept Pramipexol wird in moderater Dosierung und erst abends eingenommen. Eine weitere dopaminerge Medikation wie Levodopa in mehreren Einzelgaben tagsüber fehlt, ebenso MAO-B- oder COMT-Hemmer. Diese wären typisch für Morbus Parkinson.
Typisch beim Restless-Legs-Syndrom sind Verordnungen über vergleichsweise niedrige Dosierungen der Non-Ergot-Dopamin-Agonisten Pramipexol und Ropinirol, die in einer oder zwei Dosen abends und/oder zur Nacht gegeben werden. Patienten, die auch tagsüber RLS-Symptome haben, sind eher selten und werden vorzugsweise mit Rotigotin-Pflastern behandelt (1 bis 3 mg/Tag, höhere Dosierungen deuten auf Morbus Parkinson hin).
Levodopa-Gaben morgens und tagsüber zwischen den Mahlzeiten sowie die Hemmstoffe des Dopamin-Abbaus (die Inhibitoren der Monoaminoxidase B [MAO-B-Hemmer] Selegilin, Rasagilin und Safinamid sowie die Inhibitoren der Catechol-O-Methyl-Transferase [COMT-Hemmer] Entacapon und Tolcapon) sind bei RLS weder untersucht noch zugelassen und damit eher ein Beleg, dass ein M. Parkinson vorliegt.
„Sie haben ein Restless-Legs-Syndrom, sehe ich das richtig?“ Die Reaktion auf diese Frage ist meist respektvolles Staunen – Patienten mit Restless-Legs-Symptomen sind es nicht gewohnt, dass man das in der Apotheke auf einen Blick erkennt. Ist die Antwort ein Ja, kann man gleich zwei Fragen nachschieben: „Wissen Sie alles über Ihre Krankheit?“ und, falls kein Eisen-Präparat verordnet ist: „Haben Sie Ihre Eisen-Werte messen lassen?“ Die Selbsthilfegruppe Deutsche Restless Legs Vereinigung (RLS e. V.) bietet mit dem Vademecum RLS, das auch einen Leitfaden für Hausärzte beinhaltet, eine Broschüre an, die von Apotheken angefordert und bei Bedarf an die Patienten abgegeben werden kann (s. Kasten „Literaturtipp“).
Literaturtipp
Die Deutsche Restless Legs Vereinigung (RLS e. V.) wurde von RLS-Betroffenen 1995 als gemeinnütziger Verein gegründet und möchte Ansprechpartner für die Mitglieder der Vereinigung sowie auch für Betroffene, Ärzte, die Wissenschaftler und Interessierte sein. Sie bietet viele Informationen und praktische Hilfen rund um das Restless-Legs-Syndrom. Darunter das Vademecum RLS, ein Therapieleitfaden für Betroffene und Ärzte.
Seit November steht auch ein Heft zum Thema Eisen-Substitution zur Verfügung.
Hat der Patient fünf oder mehr verschiedene systemisch wirkende Arzneimittel einzunehmen, kann und sollte ihm eine Medikationsanalyse angeboten werden.
Medikationsanalyse – die „üblichen Verdächtigen“
Das Restless-Legs-Syndrom hält für den verordnenden Arzt und die Patienten eine Reihe von Fallen bereit, die in einer Medikationsanalyse detektiert und so umgangen werden können. Dies betrifft an erster Stelle die gleichzeitige Verordnung von Substanzen, die als Mimics Restless-Legs-Symptome auslösen oder verschlimmern können. Dabei handelt es sich z. B. um stark serotonerge Antidepressiva.
Interaktionen mit Nahrungsmitteln sind an zweiter Stelle zu nennen. Da Levodopa als eine Aminosäure mit den Aminosäuren des Nahrungsproteins um Transportenzyme konkurriert, sollte die Einnahme nüchtern erfolgen. Das ist oft schwierig im Alltag umzusetzen, da das RLS eine häufige Komorbidität einer diabetischen Polyneuropathie ist, die viele Ausprägungen hat – darunter eine Gastroparese, also die verzögerte Magenentleerung. Eine Umstellung auf Pramipexol oder (insbesondere bei Niereninsuffizienz vorzugsweise) Ropinirol ist hier zielführend, da bei diesen Wirkstoffen keine Interaktionen mit Nahrungsmitteln bekannt sind. Der Patient muss, auch wenn er die Wirkung als ungenügend empfindet, vor einer eigenmächtigen Aufdosierung gewarnt werden, die das Risiko der Augmentation in sich trägt.
Auch Eisen-Präparate sollten nüchtern eingenommen werden, aber dann werden sie oft schlecht vertragen. Einige Nahrungsergänzungsmittel können hier helfen (s. u.).
Für Rotigotin-Pflaster gilt, dass transdermale therapeutische Systeme hochgradig erklärungsbedürftige Arzneiformen sind. Sie müssen täglich auf eine andere Hautstelle aufgebracht werden, die entfettet (gewaschen) und unbehaart sein muss. Durch das Andrücken mit der warmen Hand über 30 Sekunden verflüssigt sich der Kleber, dringt in die äußeren Hautschichten ein und dient so dem Wirkstoff gewissermaßen als Schiene auf dem Weg in die Haut. Wärmeeinwirkung auf die Stelle mit dem Pflaster muss der Patient vermeiden.
Werden RLS-Patienten mit Gabapentin oder Pregabalin behandelt, empfiehlt es sich, die im Laborbefund (sofern vorhanden) ausgewiesene geschätzte glomeruläre Filtrationsrate (eGFR), die auf dem Serumkreatinin-Spiegel beruht und nach der MDRD- oder CKD-EPI-Formel berechnet wurde, nicht einfach hinzunehmen, sondern mit einem Cockcroft-Gault-Formelrechner (verfügbar im Internet oder in den einschlägigen AMTS-Programmen) nachzurechnen. Gerade bei geriatrischen Patienten mit geringer Muskelmasse wird die Nierenfunktion oft überschätzt, was dann die eine oder andere Nebenwirkung erklärt.
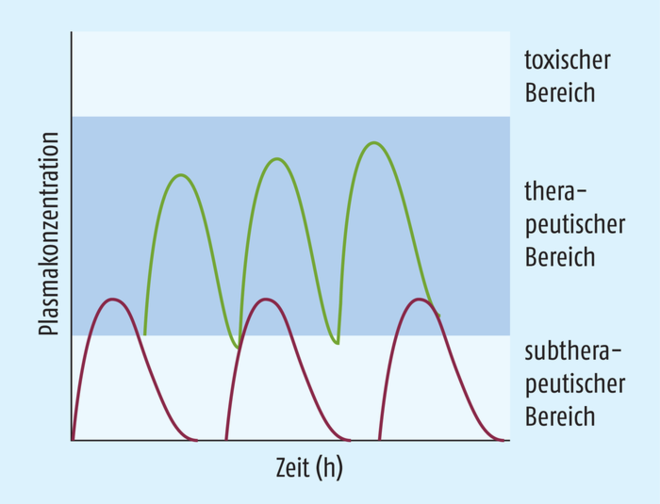
Das bevorzugte Auftreten der Restless-Legs-Symptomatik in den Abendstunden verführt viele Ärzte dazu, Opioide mit einer Zwölf-Stunden-Retardgalenik nur zur Einnahme am Abend zu verordnen. Dieses Dosierungsschema ist außerhalb der Zulassung und auch nicht sinnvoll. Etwa 16 Stunden nach der Einnahme sind die messbaren Spiegel der Substanz wieder auf Null zurückgefallen, es kann sich damit kein Steady State aufbauen (s. Abb. 2). Schlimmstenfalls wird der Patient alle 24 Stunden einer Entzugssymptomatik ausgesetzt. Aus pharmakokinetischer Sicht möglich, aber auch nicht durch die Zulassung gedeckt ist die Möglichkeit, morgens eine niedrigere und abends eine höhere Dosierung einzunehmen.
Abb. 2: Pharmakokinetik eines Opioids mit Zwölf-Stunden-Retardgalenik bei Gabe alle zwölf (grün) bzw. alle 24 Stunden (rot).
Opioide sind Substanzen, die eines intensiven Nebenwirkungsmanagements bedürfen. Während initiale Nebenwirkungen wie Sedierung und Übelkeit meist nur wenige Wochen anhalten und sich auch durch langsames Aufdosieren (start low, go slow) deutlich reduzieren lassen, bleibt die Opioid-induzierte Obstipation (OIO, Opioid-induced Constipation OIC) oft über die gesamte Therapiedauer erhalten oder verschlimmert sich sogar.
Der Naloxon-Zusatz zu Oxycodon oder Tilidin bedeutet nicht zwangsläufig, dass Laxanzien überflüssig sind. Da es vielen Patienten peinlich ist, die Obstipation von sich aus anzusprechen, ist intensives Nachfragen im Beratungsgespräch empfehlenswert.
Evidenzbasierte Zusatzempfehlungen
Nahrungsergänzungsmittel sind ein großes Thema bei RLS-Patienten. Umso wichtiger ist es, ihnen gezielt die Mittel zu empfehlen, für die zumindest ansatzweise ein klinischer Nutzen gezeigt werden konnte. Magnesium-Einnahme beispielsweise war lange Zeit eine gängige Empfehlung, die in der aktuellen Leitlinie zusammengefasste Studienlage liefert jedoch keine Belege für eine klinische Wirksamkeit.
Pycnogenol, ein antioxidativer Extrakt aus der französischen Meereskiefer, wird derzeit als wirksam zur Prävention des Restless-Legs-Syndroms beworben, obwohl die Teilnehmer der Studie, die dies beweisen soll, offenbar bereits als RLS-Patienten diagnostiziert waren. Ein Blick in das Kapitel „Material und Methoden“ zeigt, dass die Studie weder randomisiert noch verblindet durchgeführt wurde. Auch wurde zur Beurteilung der Wirksamkeit nicht wie international üblich der IRLS-Score herangezogen, vielmehr wurden die Teilnehmer nach Kribbeln, Ziehen, Schmerzen, Juckreiz, elektrischen Impulsen und Schlafproblemen befragt – Symptome, die teilweise eher nach einer Polyneuropathie klingen [1]. Prüft man die Studie nach den Kriterien der Good Clinical Practice, kommt man daher zu dem Ergebnis, dass die derzeitige Evidenz für den klinischen Nutzen von Pycnogenol beim Restles-Legs-Syndrom eher gering ist. Nach Herstellerangaben (www.pycnogenol.com) soll Pycnogenol unter anderem auch bei Erkrankungen des Auges, des Herzens, der Gelenke, der Venen und Atemwege sowie bei Diabetes, Menstruations- und menopausalen Beschwerden wirksam sein.
Deutlich besser, wenngleich nicht ausreichend für eine Erwähnung in der Leitlinie, ist die Evidenz für den Benefit einer Selen-Substitution durch eine kleine, aber methodisch saubere Studie aus dem arabischen Raum [2]. In dieser dreiarmigen randomisierten kontrollierten Studie wurde die Verbesserung des IRLS-Scores unter Placebo, Selen mit 50 sowie mit 200 µg täglich über einen Zeitraum von fünf Monaten untersucht. Es ergab sich eine hochsignifikant stärkere Senkung (12,86 bzw. 14,03 Punkte) in den Selen-Armen im Vergleich zum Placebo-Arm (6,09 Punkte). Der Unterschied zwischen 50 µg und 200 µg Selen war dagegen nicht statistisch signifikant. Langfristig erscheinen damit 50 µg Selen täglich (das entspricht in etwa dem nutritiven Tagesbedarf und gilt als unbedenkliche Dosierung) ausreichend zu sein. Da die Übertragbarkeit dieser Ergebnisse auf eine europäische Population bisher unklar ist, bereitet nach Auskunft des RLS e. V. derzeit eine schwedische Arbeitsgruppe eine Neuauflage dieser Untersuchung vor.
Dass die neue Leitlinie Eisen stark in den Vordergrund rückt, wirft die Frage auf, wie man die orale Eisen-Substitution effizienter und verträglicher gestalten kann. Ein wesentlicher limitierender Faktor ist eine Feedbackhemmung, die den Körper vor Eisen-Überladungen schützen soll: Befindet sich viel Eisen im Pfortaderblut, schüttet die Leber Hepcidin aus, das den Eisen-Transport durch die Enterozyten drosselt. Dadurch bleibt mehr Eisen im Darm, wo es die typischen Nebenwirkungen verursacht. Es gibt jedoch eine Situation, in der die Schutzfunktion dieser Feedbackhemmung nicht sinnvoll ist: Säuglinge benötigen viel Eisen. Deshalb gibt es in der Muttermilch den Eiweißstoff Lactoferrin, der die Feedbackhemmung durch Hepcidin teilweise aufhebt. Lactoferrin lässt sich aus Milch gewinnen und steht (sofern keine Milcheiweißallergie vorliegt) als Nahrungsergänzungsmittel zur Verfügung. Klinische Studien zu Lactoferrin wurden vor allem an Schwangeren durchgeführt, die ja häufig mit einer Eisenmangel-Anämie zu kämpfen haben. Es zeigte sich bei den Frauen in der Eisen-plus-Lactoferrin-Studiengruppe ein schnellerer Anstieg des Hämoglobin- und des Ferritinwerts als bei den Frauen, die nur Eisen bekamen [3, 4]. Eine andere Möglichkeit, die Eisen-Resorption laut Studiendaten um ca. 50% zu erhöhen, besteht in der Gabe von Milchsäurebakterien (Lactobacillus plantarum) zusammen mit Eisen, Folsäure und Vitamin C [5, 6]. |
Literatur
[1] Belcaro G et al. Restless legs syndrome: prevention with Pycnogenol and improvement of the venoarteriolar response. Panminerva Med 2022;64(2):253-258
[2] Rahimdel AG et al. The Effect of Selenium Administration on Restless Leg Syndrome Treatment. Iran Red Crescent Med J 2012;14(1):14–19
[3] Paesano R et al. Lactoferrin efficacy versus ferrous sulfate in curing iron disorders in pregnant and non-pregnant women. Int J Immunopathol Pharmacol 2010;23:577-587
[4] Paesano R et al. The influence of lactoferrin, orally administered, on systemic iron homeostasis in pregnant women suffering of iron deficiency and iron deficiency anemia. Biochemie 2009;91:44-51
[5] Hoppe M et al. Probiotic strain Lactobacillus plantarum 299v increases iron absorption from an iron-supplemented fruit drink: a double-isotope corss-over single-blind study in women of reproductive age. British J Nutrition 2015;114:1195-1202
[6] Axling U et al. The effect of Lactiplantibacillus plantarum 299v together with a low dose of iron on iron status in healthy pregnant women: A randomized clinical trial. Acta Obstet Gynecol Scand 2021;100:1602–1610, https://doi.org/10.1111/aogs.14153
[7] Heidbreder A, Trenkwalder C. Restless Legs Syndrom. Sk2-Leitlinie herausgegeben von der Kommission Leitlinien der Deutschen Gesellschaft für Neurologie (DGN) und der Deutschen Gesellschaft für Schlafforschung und Schlafmedizin (DGSM), AWMF-Registernummer: 030/081, Stand: Juni 2022, www.awmf.org
Weitere Artikel zum Thema "Restless-Legs-Syndrom" in dieser DAZ-Ausgabe:
- Neues zu Restless Legs: Diagnostik und Therapie verändern sich durch die neue S2k-Leitlinie
- Eisen und das Restless-Legs-Syndrom: Zwei Fallbeispiele aus der Praxis
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.