
- DAZ.online
- DAZ / AZ
- DAZ 18/2023
- Lasmiditan als ...
Neue Arzneimittel
Lasmiditan als Akuttherapeutikum bei Migräne
Neue Option bei Kontraindikation gegen Triptane
In Deutschland leiden etwa 12 bis 14% der Frauen und 6 bis 8% der Männer unter Migräne. Die heftigen, häufig einseitig-pulsierend auftretenden Kopfschmerz-Attacken werden oft von Übelkeit, Erbrechen sowie von Licht-, Lärm- und Geruchsüberempfindlichkeit begleitet und dauern vier bis 72 Stunden an. Mögliche Auslöser sind u. a. Stress, ungünstige Wetterlagen oder bestimmte Lebensmittel, aber auch ein Ungleichgewicht des Serotonin-Spiegels mit niedrigen Serotonin-Konzentrationen in der Peripherie und hohen im Zentralnervensystem. Die Betroffenen sind während eines Migräne-Anfalls sowohl im beruflichen als auch privaten Leben erheblich beeinträchtigt. Zur Akutbehandlung steht eine ganze Reihe von Wirkstoffen zur Verfügung, als Mittel der ersten Wahl Triptane, weiterhin Analgetika wie Acetylsalicylsäure, Ibuprofen, Naproxen oder Paracetamol sowie Antiemetika. Insbesondere für Patienten, die die an 5-HT1B/1D-Rezeptoren agonistisch wirkenden Triptane nicht vertragen oder auf diese nur unzureichend ansprechen, besteht weiterhin ein erheblicher therapeutischer Bedarf. Für genau diese Migräne-Patienten ist Lasmiditan, ein hochaffiner Agonist an serotoninergen 5-HT1F-Rezeptoren, vorgesehen.
Serotonin-System als erprobtes Target
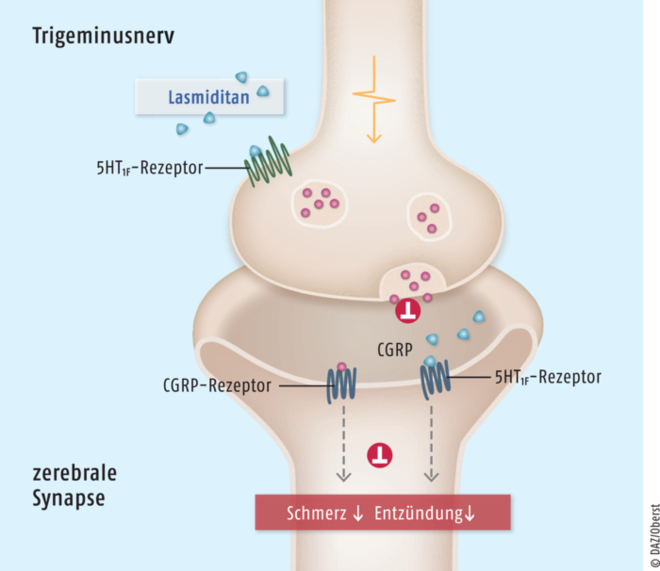
Der exakte Wirkmechanismus von Lasmiditan ist nicht bekannt, allerdings werden eine reduzierte Freisetzung von entzündungsfördernden Neuropeptiden wie Substanz P und Calcitonin Gene-Related Peptide (CGRP) sowie eine Hemmung von Schmerzbahnen im Bereich des Trigeminusnervs vermutet. Die Selektivität von Lasmiditan für den 5-HT1F-Rezeptor ist gegenüber 5-HT1B- und 5-HT1D-Rezeptoren mehr als 440-fach erhöht. Aufgrund der nahezu fehlenden Wirkung an 5-HT1B-Rezeptoren bewirkt Lasmiditan im Gegensatz zu den Triptanen keine Vasokonstriktion der Koronararterien, der inneren Brustarterien und von zerebralen Blutgefäßen wie den mittleren Meningealarterien.
Perorale Akuttherapie
Für die Behandlung einer Migräne-Attacke sollten zunächst 100 mg Lasmiditan als Initialdosis unabhängig von den Mahlzeiten eingenommen werden. Um die Verträglichkeit zu verbessern, kann bei nachfolgenden Anfällen eine Dosisreduktion auf 50 mg versucht werden, bei nicht ausreichendem Ansprechen ist eine Dosiserhöhung auf 200 mg möglich. Falls der Migräne-Kopfschmerz nach Einnahme von 50 oder 100 mg Lasmiditan innerhalb von 24 Stunden nach dem ersten Ansprechen erneut auftritt, darf frühestens zwei Stunden nach der ersten Applikation eine zweite Dosis derselben Stärke eingenommen werden. Bei fehlender Response auf die erste Dosis ist es allerdings unwahrscheinlich, dass eine zweite Dosis bei derselben Attacke von Nutzen ist. Die Tagesmaximaldosis beträgt 200 mg.
Abb. 1: Dysbalancen des serotoninergen Systems sind für die Auslösung von Migräne-Attacken mitverantwortlich. Derzeit geht man davon aus, dass der serotoninerg wirkende 5-Hydroxytriptamin-1F(5-HT1F)-Rezeptoragonist Lasmiditan zu einer reduzierten Freisetzung von entzündungsfördernden Neuropeptiden wie Calcitonin Gene-Related Peptide (CGRP) sowie einer Hemmung von Schmerzbahnen im Bereich des Trigeminusnervs führt. Bei Einnahme des 5-HT1F-Agonisten während eines Migräne-Anfalls können Schmerzen und Entzündungsreaktionen gemildert oder sogar ganz aufgehoben werden.
Keine Teilnahme am Straßenverkehr für acht Stunden
Lasmiditan wirkt zentral dämpfend und führt zu Symptomen wie Benommenheit, Koordinationsstörungen, Schläfrigkeit, Sehstörungen, Schwindel, Muskelschwäche, Halluzinationen, kognitiven Störungen und anderen mentalen Beeinträchtigungen. Nach jeder Applikation dürfen die Patienten daher für mindestens acht Stunden kein Fahrzeug führen oder anderen Aktivitäten nachgehen, die eine erhöhte Aufmerksamkeit erfordern, selbst wenn sie sich dazu in der Lage fühlen. Falls diese Anweisung nicht sicher eingehalten werden kann, muss die Anwendung von Lasmiditan unterbleiben, da der Wirkstoff insbesondere die Verkehrstüchtigkeit signifikant beeinträchtigt. Bei gleichzeitiger Anwendung von Sedativa, opioiden Analgetika oder Alkohol ist besondere Vorsicht geboten.
Vorsicht Serotonin-Syndrom!
Insbesondere wenn Lasmiditan gleichzeitig mit serotoninerg wirkenden Arzneimitteln wie selektiven Serotonin- bzw. kombinierten Serotonin-Noradrenalin-Reuptake-Hemmern, tricyclischen Antidepressiva, Monoaminoxidase(MAO)-Hemmern oder Fentanyl zur Anwendung kommt, besteht die Gefahr eines potenziell lebensbedrohlichen Serotonin-Syndroms. Entsprechende erste Anzeichen können Unruhe, Halluzinationen, Koma, Blutdruckanstiege, Tachykardie, Hyperthermie, Diarrhö und Krämpfe sein. Auch bei in zeitlicher Nähe mit Lasmiditan applizierten Triptanen sind ähnliche Effekte nicht auszuschließen. Inwiefern von Lasmiditan ein Missbrauchspotenzial ausgeht, ist noch nicht abschließend geklärt. Ein körperlicher Entzug nach abruptem Absetzen der Medikation wurde jedoch nicht beobachtet. Aufgrund bislang nur sehr begrenzter Erfahrungen wird die Anwendung von Lasmiditan während der Schwangerschaft nicht empfohlen. Falls die Substanz in der Stillzeit eingesetzt werden soll, ist für etwa 24 Stunden nach der Applikation die Einhaltung einer Stillpause angeraten.
Neue Arzneimittel 2023
In der bisher monatlich erschienenen DAZ-Beilage „Neue Arzneimittel“ stellte Apothekerin Dr. Monika Neubeck neue Wirkstoffe vor und ordnete sie in die bestehenden Therapieoptionen ein. Seit Januar 2023 finden Abonnentinnen und Abonnenten der DAZ die neuen Arzneistoffe auf DAZ.online unter www.deutsche-apotheker-zeitung.de/pharmazie/arzneimittel. Dort gibt es auch ein Archiv mit allen seit 2000 eingeführten Wirkstoffen. Im April sind neu hinzugekommen:
- Ciltacabtagen
- Dengue-Impfstoff
- Lasmiditan
Für die Offizin bedeutsame Wirkstoffe stellen wir in der Print-Ausgabe der DAZ regelmäßig in der Rubrik „Neue Arzneimittel“ vor.
Drei Phase-III-Studien
Die Zulassung von Lasmiditan beruht auf den drei randomisierten, doppelblinden, placebokontrollierten Phase-III-Studien SAMURAI, SPARTAN und CENTURION mit insgesamt etwa 6000 erwachsenen Migräne-Patienten. Zwei Stunden nach der Applikation bewerteten die Probanden das Schmerzlevel auf einer vierstufigen Skala. Bei der 200-mg-Dosis setzte die Wirkung bereits nach 30 Minuten ein, bei den niedrigeren Dosen etwas später. Zwei Stunden nach Einnahme von 100 mg Lasmiditan war bei etwa 25 bis 30% der Teilnehmer kein Schmerz mehr feststellbar. Die entsprechenden Werte nach Anwendung von 200 mg Lasmiditan betrugen ca. 30 bis 40%. Unter Placebo lag der Patientenanteil mit vollständiger Response bei 10 bis 20%, entsprechend einer signifikanten Überlegenheit von Lasmiditan (p < 0,001 für alle Vergleiche mit Placebo). Etwa 40 bis 50% der Patienten aus den Verumgruppen gaben zudem an, innerhalb von zwei Stunden von den am meisten belastenden Migräne-Symptomen wie Photophobie, Übelkeit oder Phonophobie befreit gewesen zu sein. Im Rahmen der Studie CENTURION wurden pro Patient vier Migräne-Episoden behandelt. Die Wirksamkeit von Lasmiditan blieb auch bei mehreren aufeinanderfolgenden Migräne-Attacken erhalten. Bei mindestens zwei von drei Folgeanfällen waren die Kopfschmerzen bei 14 bzw. 24% der Teilnehmer aus den Verumgruppen zwei Stunden nach Applikation der Medikation vollständig abgeklungen. Im Placebo-Arm war dies bei nur 4% der Patienten der Fall.
Ditane für Patienten mit kardiovaskulären Erkrankungen
Aufgrund ihrer über 5-HT1B vermittelten vasokonstriktorischen Wirkungen sind Triptane bei der großen Gruppe von Patienten mit kardiovaskulären Erkrankungen wie z. B. koronarer Herzkrankheit, Schlaganfall oder fortgeschrittener peripherer arterieller Verschlusskrankheit kontraindiziert. Für den ersten auf dem Markt verfügbaren reinen 5-HT1F-Agonisten Lasmiditan, der die neue Gruppe der Ditane eröffnen soll, besteht diese Einschränkung nicht. Ein gewisses Problem stellen die Lasmiditan-assoziierten zentraldämpfenden Nebenwirkungen dar. Die Beeinträchtigungen gehen so weit, dass nach jeder Applikation von Lasmiditan für mindestens acht Stunden kein Fahrzeug geführt werden darf. Letztlich muss jeder für sich entscheiden, ob er diese Einschränkung in Kauf nehmen möchte. Für Migräne-Patienten ohne Triptan-Kontraindikation sind diese erprobten Therapeutika jedoch nach derzeitigem Kenntnisstand weiterhin zu bevorzugen. In einer aktuellen Metaanalyse haben sich Wirkstoffe wie Sumatriptan, Naratriptan, Rizatriptan und Zolmitriptan dem 5-HT1F-Agonisten Lasmiditan hinsichtlich der Schmerzausschaltung überlegen gezeigt. Offenbar trägt die 5-HT1B-vermittelte Vasokonstriktion in relevantem Ausmaß zur Analgesie bei. Ergebnisse von bereits laufenden direkt vergleichenden Untersuchungen mit Lasmiditan und Sumatriptan bleiben jedoch für eine bessere Einordnung abzuwarten. |
Literatur
[1] Fachinformation zu Rayvow®, Stand August 2022
[2] Kuca B, Silberstein SD, Wietecha L et al. Lasmiditan is an effective acute treatment for migraine: A phase 3 randomized study. Neurology 2018;91(24):e2222-e2232, doi: 10.1212/WNL.0000000000006641
[3] Goadsby PJ, Wietecha LA, Dennehy EB, et al. Phase 3 randomized, placebo-controlled, double-blind study of lasmiditan for acute treatment of migraine. Brain 2019;142(7):1894-1904, doi: 10.1093/brain/awz134
[4] Ashina M, Reuter U, Smith T et al. Randomized, controlled trial of lasmiditan over four migraine attacks: Findings from the CENTURION study. Cephalalgia 2021;41(3):294-304, doi: 10.1177/0333102421989232
[5] Yang CP, Liang CS, Chang CM et al. Comparison of new pharmacologic agents with triptans for treatment of migraine: a systematic review and meta-analysis. JAMA Netw Open 2021;4(10):e2128544, doi: 10.1001/jamanetworkopen.2021.28544
[6] Rayvow® Lasmiditan. EPAR summary for the public. EMA/621260/2022, Informationen der Europäischen Arzneimittelagentur























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.