
- DAZ.online
- News
- Politik
- 10 Millionen Euro für ...
Barmer-Arzneimittelreport
10 Millionen Euro für Verwürfe
Berlin - 23.06.2017, 07:00 Uhr
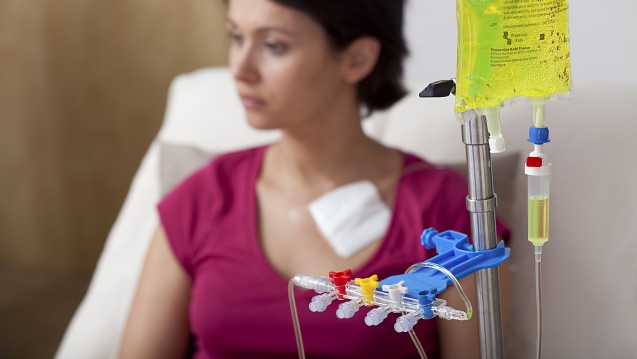
Die Kosten für Krebsmedikamente schießen in die Höhe. Die Barmer wirft Herstellern Gewinnmaximierungs-Strategien vor – auch zulasten von Apotheken. (Foto: Barmer)
Die Barmer klagt über hohe Ausgaben für onkologische Arzneimittel in der ambulanten Versorgung. Allein für ihre Versicherten seien diese seit dem Jahr 2011 um 41 Prozent gestiegen. Was die Barmer überdies ärgert, sind teure Verwürfe bei Zyto-Zubereitungen und die Herstellerangaben zur Haltbarkeit – die auch zulasten der Apotheken gingen.
Die Barmer hat am gestrigen Donnerstag in Berlin ihren Arzneimittel-Report 2017 vorgestellt. Danach sind 2016 die Ausgaben für Arzneimittel – inklusive Rezepturarzneimittel – für Barmer-Versicherte um 182 Millionen Euro auf 5,3 Milliarden Euro gestiegen (+ 4,9 Prozent). Dabei fielen 80 Prozent der Ausgaben auf nur 17 Prozent der Versicherten und 50 Prozent der Ausgaben auf 2,2 Prozent der Versicherten.
Hochpreisige Arzneimittel hat die Kasse dabei als Kostentreiber ausgemacht. Und das sind häufig Krebsarzneimittel, die in diesem Jahr Schwerpunktthema des Barmer-Reports sind. Von 2011 bis 2015 sind die Ausgaben für Onkologika demnach um 41 Prozent gestiegen, während das Plus bei allen anderen Arzneimitteln bei 20 Prozent lag. Fünf der zehn Arzneimittel mit der größten Umsatzsteigerung von 2015 zu 2016 sind Arzneimittel zur Behandlung von Tumorerkrankungen. So verzeichnete der Checkpointinhibitor Nivolumab (Opdivo®) bei der Barmer den stärksten Zuwachs – mehr als 25 Millionen Euro Mehrausgaben im Jahr 2016 fallen auf den monoklonalen Antikörper, der bei Melanom, Nierenzellkarzinom, NSCLC, Hodgkin-Lymphom, Urothelkarzinom und Tumoren des Kopf- Halsbereichs eingesetzt wird.
Späte Kosten-Nutzenbewertung gefordert
Dieser Trend lässt sich laut Barmer nicht durch eine größere Anzahl an betroffenen Patienten erklären. Vielmehr fielen die höheren Herstellerpreise ins Gewicht. Für den Barmer-Report wurden die Kosten von 31 onkologischen Arzneimitteln in Europa, Australien und Neuseeland verglichen. Demnach liegen die deutschen Preise bei 28 dieser Präparate über dem Durchschnitt, acht von ihnen kosteten hierzulande am meisten.
Nun will niemand den rund 490.000 Menschen in Deutschland, die jedes Jahr neu mit der Diagnose Krebs konfrontiert werden, die Therapie mit den vorhandenen Arzneimitteln verwehren. Auch der Barmer-Vorstandsvorsitzende Professor Dr. Christoph Straub will eine solche „unethische” Debatte nicht führen. Es müsse aber diskutiert werden, „ob die Preise in Deutschland gerechtfertigt sind“, forderte der Kassenchef. „Denn die Debatte, ob wir uns manche Therapien noch leisten können, müssen wir unter allen Umständen vermeiden.“ Er schlägt daher eine späte Kosten-Nutzen-Bewertung vor: Die Arzneimittel sollten nach fünf Jahren Versorgungserfahrung erneut auf ihren Nutzen überprüft und darauf basierend das Preis-Leistungsverhältnis neu bestimmt werden.
Orphan Drug-Status ebnet Weg in die Zulassung
Der Report geht zudem dem Orphan-Drug-Trend nach. Denn die Onkologika werden immer häufiger als Arzneimittel gegen seltene Erkrankungen zugelassen. „Die Pharmafirmen haben offenbar ein großes Interesse daran, Krebsmittel als Orphan Drugs zuzulassen. Um eine solche Zulassung zu erhalten, müssen weniger Belege über Nutzen und Sicherheit des Arzneimittels vorgelegt werden“, erläuterte einer der Studienautoren, Professor Dr. Daniel Grandt vom Klinikum Saarbrücken. So seien bei jedem dritten Orphan Drug zum Zeitpunkt der Zulassung weniger als 100 Patienten untersucht worden, randomisierte Vergleichsstudien fehlten meist. Zur Sicherheit der Patienten sollten Orphan Drugs einer regulären frühen Nutzenbewertung unterzogen werden, forderte er. Derzeit gilt ihr Zusatznutzen bereits mit der Zulassung als belegt.
Inakzptable Herstellerstrategien
Ebenfalls ein Dorn im Auge ist der Barmer, dass teure Krebsarzneien oft im Abfall landen: Nämlich die Restmengen, die bei Herstellung der Zytostatika-Rezepturen anfallen. Allein für ihre Versicherten habe die Kasse im Jahr 2015 zehn Millionen Euro für diese ungenutzten Verwürfe ausgeben müssen. Auch hierin sehen die Autoren eine weitere Strategie der Pharmaunternehmen zur Gewinnmaximierung – denn sie erzwängen den Verwurf durch praxisuntaugliche übergroße Einzeldosen. „Dass ein Hersteller beispielsweise die 1-mg-Ampulle seines Arzneimittels vom Markt nehmen kann und bei durchschnittlich pro Patient benötigter Wirkstoffmenge von 2,2 mg dieses nur noch in 3,5-mg-Ampullen anbietet (wodurch sich der Verwurf um 50 Prozent erhöht), ist inakzeptabel“, heißt es dazu im Report. Gemeint ist das zur Behandlung des multiplen Myeloms zugelassene Arzneimittel Velcade® mit dem Wirkstoff Bortezomib der Firma Janssen-Cilag.
Haftungsrisiko für Apotheker
Prof. Irene Krämer, Leiterin der Apotheke der Universitätsklinik Mainz, und Daniel Grant kritisieren in dem entsprechenden Kapitel, dass Hersteller zudem die tatsächliche Haltbarkeit angebrochener onkologischer Arzneimittelstammlösungen durch den pharmazeutischen Hersteller verschwiegen. Dass weitergehende Informationen zur physikalisch-chemischen Stabilität fehlen, führe neben den Verwürfen zu weiteren Problemen – auch für Apotheker. Diese seien, wenn sie auf Basis physikalisch-chemischer Untersuchungen und mikrobiologischer Validierung Zytostatika-Zubereitungen über die in der Fachinformation genannte Spanne hinaus verwenden, einem Haftungsrisiko ausgesetzt. Denn der Apotheker übernehme hier die Verantwortung für die Haltbarkeit der Zytostatika-Lösungen. Zudem würden die Untersuchungen komplett durch die untersuchende Einrichtung und indirekt durch die Gemeinschaft der Steuerzahler oder Versicherten finanziert.
Die Autoren fordern als Ausweg, dass die Verfügbarkeit praxistauglicher Einzeldosisstärken schon bei der Zulassung vorgeschrieben und bei der Preisfestsetzung berücksichtigt werden müsse. Auch die Durchführung von Untersuchungen zu physikalisch-chemischer Stabilität sei als Voraussetzung für die Zulassung von onkologischen Rezepturarzneimitteln vorzuschreiben.


























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.