
- DAZ.online
- News
- Pharmazie
- Cefiderocol: Antibiotikum...
CHMP empfiehlt Zulassung von Fetroja
Cefiderocol: Antibiotikum als trojanisches Pferd
Berlin - 11.03.2020, 16:30 Uhr
Fetroja: Bereits im Arzneimittelnamen versteckt Hersteller Shionogi das Besondere des neuen Cephalosporins Cefiderocol. Als Siderophor-Cephalosporin bindet es Eisen und wird, so wie ein trojansiches Pferd, über die Eisentransporter des Erregers in das Bakterium geschleust. ( r / Foto: Shionogi)
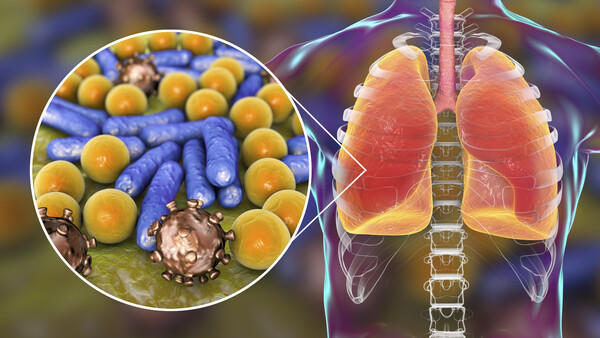
Der Humanarzneimittelausschuss der EMA empfiehlt das Cephalosporin Cefiderocol zur Zulassung. Fetroja wirkt gegen aerobe gramnegative Erreger und trickst als Siderophor-Cephalosporin gängige Resistenzmechanismen der Bakterien gegen Betalactame aus. Wie funktioniert das? Und warum nennt Shionogi sein Arzneimittel Fetroja?
Der CHMP (Committee for Medicinal Products for Human Use) sprach sich in seiner letzten Sitzung Ende Februar für die Zulassung eines neuen Antibiotikums in der EU aus. Cefiderocol soll zur Behandlung von Infektionen durch aerobe gramnegative Erreger eingesetzt werden, wenn die Behandlungsmöglichkeiten begrenzt sind. Pharmazeutischer Hersteller hinter dem neuen Reserve-Cephalosporin ist Shionogi. Handelsname ist Fetroja®.
In den USA erhielt Shionogi bereits 2019 die FDA-Zulassung. Die Indikation greift dort enger und ist auf die Behandlung von komplizierten, durch bestimmte gramnegative Bakterien verursachte Harnwegsinfektionen, inklusive der Pyelonephritis, bei Patienten ab 18 Jahren beschränkt.
Mehr zum Thema

Multiresistente Erreger
Antibiotikaforschung in den Medien: Es könnte mehr sein!

Reserve-Antibiotikum
EMA empfiehlt neues Fluorchinolon Delafloxacin zur Zulassung
EU-Zulassungsempfehlung für Meropenem/Vaborbactam
Neue Antibiotika-Hoffnung bei gramnegativen Bakterien
Folgt die Europäische Kommission der Empfehlung des Humanarzneimittelausschusses, wird Cefiderocol als Konzentrat mit 1 g Wirkstoff zu Herstellung einer intravenösen Infusion verfügbar sein. Die Zulassung umfasst, wie auch in den Vereinigten Staaten, nur Erwachsene.























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.