
- DAZ.online
- News
- Politik
- BMG will Corona-...
Änderung der MPAV
BMG will Corona-Schnelltests für Laien freigeben
Berlin - 25.01.2021, 09:15 Uhr
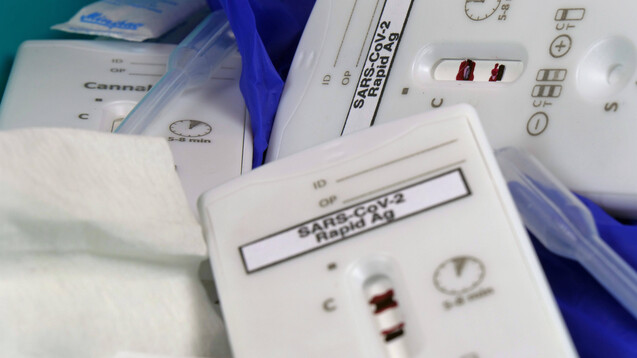
Bald sollen auch Laien Antigen-Schnelltests auf SARS-CoV-2 zur Eigenanwendung kaufen können. (Foto: imago images / Martin Wagner)
Lange hat das Bundesgesundheitsministerium die Forderung an sich abperlen lassen, Apotheken die Abgabe von Corona-Schnelltests an Laien zu ermöglichen. Doch nun scheint der Widerstand gebrochen: Nach den jüngsten Plänen aus dem Hause Spahn sollen Antigentests auf SARS-CoV-2 zur Eigenanwendung künftig wie HIV-Selbsttests zum Verkauf freigegeben werden – eine Apothekenpflicht ist nicht vorgesehen.
Der Druck ist in den vergangenen Wochen beständig gestiegen. Warum sollten nicht auch Menschen ohne medizinische Vorkenntnisse Corona-Antigen-Tests erwerben dürfen? Natürlich muss bei den derzeit erhältlichen Point-of-Care-Tests (PoC) der erforderliche Nasenabstrich sorgfältig und gewissenhaft durchgeführt werden – und man muss auch verstehen, wie mit dem Ergebnis umzugehen ist. Aber mit einer guten Beratung in der Apotheke sollten auch Laien in der Lage sein, solche Tests vorzunehmen.
Doch das Bundesgesundheitsministerium (BMG) hat die Abgabemöglichkeiten für die Tests nur zögerlich erweitert. Dazu ist stets eine Änderung der Medizinprodukte-Abgabeverordnung nötig, die genau vorschreibt, an wen In-vitro-Diagnostika (IVD) abgegeben werden dürfen. Der Arztvorbehalt für die Durchführung der Tests war bereits mit dem dritten Bevölkerungsschutzgesetz aufgehoben worden. Nach und nach kamen in den vergangenen Monaten Einrichtungen hinzu, an die Apotheken die Tests – jedenfalls zeitlich begrenzt – abgeben dürfen: zum Beispiel Heime, Schulen und erst vergangene Woche Obdachlosenunterkünfte (§ 3 Abs. 4a MPAV). Erst seit Ende vergangenen Jahres ist es Apotheker:innen und anderem pharmazeutischem Personal überdies möglich, die PoC-Tests selbst durchzuführen – eine vorherige Schulung vorausgesetzt. Und seit noch kürzerem dürfen sie auch im Auftrag des öffentlichen Gesundheitsdienstes Schnelltests durchführen.
Mehr zum Thema
IHK und HWK Südthüringen
Warten auf Schnelltests aus der Apotheke

Medizinprodukte-Abgabeverordnung
Antigen-Schnelltests jetzt auch für Schulen und Kitas
Doch die Rufe nach einem noch breiteren Einsatz der Schnelltests ebbten nicht ab. Kommenden Donnerstag steht im Bundestag ein Antrag der Grünen-Bundestagsfraktion auf der Tagesordnung, der darauf abzielt, nicht nur die Kapazitäten für Schnelltests massiv auszubauen, sondern auch die Selbstanwendung zu erlauben und Public-Health-Screenings zu ermöglichen. Auch die SPD-Gesundheitspolitikerin Hilde Mattheis forderte vergangene Woche, es müsse „dringend“ ein Antigen-Schnelltest für die Anwendung daheim zugelassen werden – auch wenn Schnelltests keine 100-prozentige Sicherheit böten. Doch: „Wenn sie zu 60 Prozent Leute herausfiltern, die Corona-positiv sind, wäre schon viel gewonnen“, so Mattheis.
In der Apothekerschaft war es vor allem Thomas Preis, Vorsitzender des Apothekerverbands Nordrhein, der sich für eine Abgabe von Schnelltests an Laien stark gemacht hat. Studien zeigten, dass auch Laien durchaus zur Durchführung der Tests in der Lage seien, erklärte er noch am vergangenen Freitag gegenüber der AZ. Und: Er könne sich vorstellen, dass die Bundesregierung die Tests bald freigeben wird. Dann sei aber wichtig, dass die Abgabe nur über Apotheken erfolgen dürfe, damit auch eine entsprechende Beratung stattfinde.
In einer Reihe mit HIV-Selbsttests
Und dann ging es ganz schnell: Seit vergangenem Freitagnachmittag gibt es einen Referentenentwurf des Bundesgesundheitsministeriums (BMG) für eine „Dritte Verordnung zur Änderung der Medizinprodukte-Abgabeverordnung im Rahmen der epidemischen Lage von nationaler Tragweite“. Dieser sieht vor, dass „In-vitro-Diagnostika für die Eigenanwendung, die für den direkten Nachweis einer SARS-CoV 2-Infektion bestimmt sind“ in Anlage 3 der Medizinprodukte-Abgabeverordnung (MPAV) aufgenommen werden. In dieser Anlage sind die IVD gelistet, die von den geltenden Abgabebeschränkungen ausgenommen sind – bislang sind das lediglich HIV-Selbsttests. Das heißt: Der Verkauf an Laien wird möglich. Und wie schon bei den Selbsttests zum Nachweis einer HIV-Infektion, will man auch bei den Corona-Schnelltests auf eine Apothekenpflicht verzichten.
Viele Antigentests zur Eigenanwendung in der Entwicklung
Offenbar geht es dem BMG nicht um die derzeit auf den Markt befindlichen PoC-Tests, sondern um Tests, die erst noch kommen müssen. In der Begründung zum Referentenentwurf heißt es, aktuell würden von einer Vielzahl von Unternehmen Antigen-Tests entwickelt, bei denen Probennahme, Testung und Bewertung des Ergebnisses durch medizinische Laien möglich sei. Solche Tests unterlägen den Vorgaben des Medizinproduktegesetzes und müssten so hergestellt sein, dass die Ergebnisqualität auch bei der Anwendung durch Laien sichergestellt ist – dass die gesetzlichen Vorgaben erfüllt sind, müsse gegenüber einer Benannten Stelle nachgewiesen werden. Zudem werde geprüft, ob die Gebrauchsinformationen den Anwender über das erhaltene Ergebnis detailliert aufklären und die Bedeutung erläutern. Werden diese Vorgaben vollumfänglich erfüllt, sei es „nicht mehr erforderlich, an der bestehenden umfassenden Abgabebeschränkung festzuhalten“. Auch die Apotheke als Beratungsinstanz hält das BMG dann nicht für nötig. Dazu heißt es:
Über die beim Selbsttest zur Verfügung gestellten Materialien (z. B. Beipackzettel) erhalten Anwender auch Präventionsinformationen, wie zum Beispiel Hinweise und Anweisungen zu den zu treffenden Maßnahmen (bei positivem, negativem oder unklarem Ergebnis) und zur Möglichkeit eines falsch positiven oder falsch negativen Ergebnisses, sowie den Hinweis, dass ohne vorherige Konsultation des Arztes keine medizinisch wichtige Entscheidung getroffen werden dürfen. Eine Auflockerung des bisherigen Grundsatzes einer verknüpften Beratung und Testung scheint daher gerechtfertigt.“
Referentenentwurf für eine Dritte Verordnung zur Änderung der Medizinprodukte-Abgabeverordnung im Rahmen der epidemischen Lage von nationaler Tragweite vom 22. Januar 2021
Dass es infolge vermehrter Schnelltests beim Melden von Infektionen zu Problemen kommt, es also Auswirkungen auf die epidemiologische Überwachung gibt, erwartet das BMG übrigens nicht. Denn nach einem positiven Selbsttestergebnis sei eine Bestätigungsdiagnostik beziehungsweise die Bestimmung weiterer diagnostischer Marker für die Erstellung einer Diagnose notwendig.
Während die Änderung in Anlage 3 der Medizinprodukte-Abgabeverordnung (MPAV) von Bestand wäre, plant das Ministerium auch noch verschiedene Änderungen an § 3 Abs. 4a MPAV. Dieser enthält einige Sonderreglungen zur Abgabe, die nur für die Zeit der „epidemischen Lage von nationaler Tragweite“ gelten sollen. So soll der Kreis der Einrichtungen, die die PoC-Tests erwerben können, weiter ausgedehnt werden, unter anderem auf sämtliche Einrichtungen nach § 36 Abs. 1 IfSG – denn ihnen ist gemein, dass hier viele Menschen in beengten räumlichen Situationen zusammenkommen.
Ferner soll auch Einrichtungen der kritischen Infrastrukturen die Möglichkeit eingeräumt werden, die Schnelltests erwerben. Dabei handelt es sich laut Verordnungsentwurf „um Einrichtungen, die den Sektoren Energie, Informationstechnik und Telekommunikation, Transport und Verkehr, Gesundheit, Wasser, Ernährung, Finanz- und Versicherungswesen, Staat und Verwaltung sowie Medien und Kultur angehören und von hoher Bedeutung für das Funktionieren des Gemeinwesens sind, weil durch ihren Ausfall oder ihre Beeinträchtigung erhebliche Versorgungsengpässe oder Gefährdungen für die öffentliche Sicherheit eintreten würden“.
Da diese Einrichtungen dann als „Betreiber“ des Medizinprodukts „PoC-Antigentest“ gelten, müssen sie sicherzustellen, dass nur solche Personen die Tests anwenden dürfen, die entsprechend eingewiesen oder geschult sind.
Nun bleibt abzuwarten, die die Stellungnahmen – etwa der ABDA – zum Referentenentwurf ausfallen.





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.