
- DAZ.online
- News
- Wirtschaft
- BAH: Im Handelsabkommen...
Wie wirkt sich der Brexit auf den Arzneimittelsektor aus?
BAH: Im Handelsabkommen „fehlen wichtige praxisgerechte Lösungen“
Dillingen/Stuttgart - 22.03.2021, 07:00 Uhr

Seit dem 1. Januar 2021 gilt zwischen der EU und Großbritannien ein Handels- und Kooperationsabkommen – vorläufig. Und das bringt Unsicherheiten auch für die Arzneimittelindustrie. (x / Foto: IMAGO / Rainer Unkel)
Seit Januar dieses Jahres gilt das vorläufige Handelsabkommen zwischen der EU und Großbritannien. Die derzeit geltenden Regelungen seien aber nur Momentaufnahmen und in einigen wichtigen Bereichen fehlten praxisgerechte Lösungen, erklärte Hubertus Cranz, Hauptgeschäftsführer des Bundesverbands der Arzneimittel-Hersteller (BAH). Eine Broschüre des BAH informiert nun über die Folgen des Brexits für die Arzneimittelindustrie und was zu beachten ist.
Am 23. Juni 2016 entschied sich eine knappe Mehrheit der Bevölkerung in Großbritannien und Nordirland für einen Austritt aus der Europäischen Union. Schon früh zeichnete sich ab, dass der sogenannte „Brexit“ auch im Hinblick auf die künftigen Handelsbeziehungen zwischen der EU und Großbritannien schwierig wird – mit regulatorischen Folgen für die Arzneimittelindustrie. Seit dem 1. Januar 2021 gilt nun zwischen der EU und dem Vereinigten Königreich ein vorläufiges Handels- und Kooperationsabkommen. Die Ratifizierung des Abkommens wird im April 2021 erwartet.
Mehr zum Thema

Erste Anmerkungen zum Handels- und Kooperationsabkommen zwischen EU und Großbritannien
Welche Folgen könnte der Brexit-Vertrag für den Arzneimittelsektor haben?

Regierung schreibt an Lieferanten
UK: Pharmaindustrie muss Vorräte für den Brexit anlegen

Brexit um Mitternacht
„No Deal-Brexit“ ist nicht aufgehoben, sondern vielleicht nur aufgeschoben
Das Handelsabkommen sei in zentralen Bereichen lückenhaft und stelle nur eine Momentaufnahme dar, so die Einschätzung von Hubertus Cranz, Hauptgeschäftsführer des BAH. „In einigen wichtigen Bereichen fehlen praxisgerechte Lösungen, beispielsweise zur vollen Anerkennung behördlicher Inspektionen der jeweils anderen Seite“, wird Cranz in einer Pressemitteilung des BAH zum Erscheinen der hauseigenen Brexit-Broschüre zitiert. „Diese und viele weitere Punkte könnten – und sollten – in einem künftigen Mutual Recognition Agreement (MRA) geregelt werden.“ Demnach sollte das MRA die gegenseitige Anerkennung von Chargen- und Importtests, amtlichen Arzneimittel-Kontrolllaboren, GMP-Inspektionen und CE-Kennzeichnungen von Medizinprodukten beinhalten.
Beobachtung der Brexit-Entwicklung
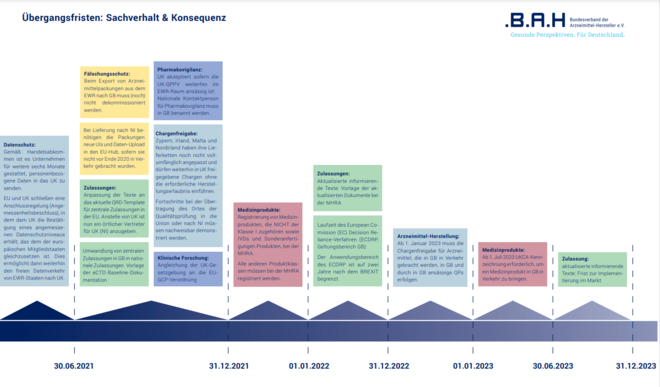
Der BAH beobachtet seit Jahren aufmerksam die Entwicklungen im Zusammenhang mit dem Brexit und hat dazu vor kurzem eine neue Broschüre mit dem Titel „Der Brexit und seine Folgen für die deutsche Arzneimittelindustrie“ herausgegeben. Das Papier soll vor allem der Orientierung dienen und informieren, worauf sich die pharmazeutischen Unternehmen einstellen müssen. In der Broschüre werden unter anderem die Besonderheiten zur Geltung des europäischen Rechtsbestands in Großbritannien, neue Übergangsfristen, Forschung, Zulassung, Herstellung und Prüfung von Arzneimitteln, Pharmakovigilanz, Fälschungs-, Patent-, Marken- und Datenschutz sowie Regelungen rund um die Medizinprodukte erläutert.
BU: Derzeit greifen noch einige Übergangsfristen, danach gelten britische Regeln, warnt der BAH. (Screenshoot: BAH/Brexit-Broschüre)
Weil das Post-Brexit-Handelsabkommen noch nicht ratifiziert wurde, empfiehlt der BAH seinen Mitgliedern, sich auf unterschiedliche Situationen einzustellen. So weist der Verband zum Beispiel daraufhin, dass möglicherweise die Regelung, wonach ein Zulassungsinhaber, der Arzneimittel im Vereinigten Königreich vertreibt, weiterhin seinen Sitz in der EU beziehungsweise dem EWR haben kann, zeitlich begrenzt sein wird. Allerdings wurden in diesem Zusammenhang bislang noch keine Fristen kommuniziert. Dennoch empfiehlt der BAH, sich darauf zeitnah vorzubereiten.
Anpassung der Datenverarbeitungsverträge
Im Bereich des Datenschutzes rät der BAH allen Unternehmen, ihre Datenverarbeitungsverträge und Datenschutz-Governance in Bezug auf ihren Datenverkehr mit dem Vereinigten Königreich zu überprüfen und im Bedarfsfalle anzupassen. Wegen der bereits gestarteten Umsetzung der EU-Datenschutz-Grundverordnung (DSGVO) in nationales Recht in Großbritannien rechnet der BAH damit, dass es zu einem Angemessenheitsbeschluss kommt.
Hintergrund: Nach Artikel 45 DSGVO kann die Europäische Kommission feststellen, dass ein Drittland ein angemessenes Datenschutzniveau gewährleistet. Wird eine Datenübermittlung von einem Angemessenheitsbeschluss umfasst, sind keine weiteren Schutzmaßnahmen notwendig.
Bisheriger EU-Fälschungsschutz ungültig
Seit dem 1. Januar 2021 ist in Großbritannien die EU-Fälschungsschutzrichtlinie 2011/62/EU ungültig. Damit ist das Vereinigte Königreich vom europäischen Fälschungsschutzsystem abgetrennt. Laut des BAH-Papiers können Unternehmen den Manipulationsschutz und den Data Matrix Code aber auf freiwilliger Basis beibehalten. Für Nordirland wird das System weiter genutzt, das heißt für Arzneimittel mit einer in Nordirland gültigen Zulassung müssen alle Bestimmungen zur EU-Fälschungsschutzrichtlinie und zur delegierten Verordnung 2016/161 weiterhin eingehalten werden.
Bis zum 31. Dezember 2021 müssen Packungen, die aus dem Europäischen Wirtschaftsraum nach Großbritannien exportiert werden, nicht dekommissioniert werden. DAZ.online berichtete darüber.
Mehr zum Thema

Securpharm und Brexit
Verifikationspflicht wird in England 2021 aufgehoben
Pharmakovigilanz: vorerst kaum Änderungen
Bei der Pharmakovigilanz geht der BAH im Großen und Ganzen davon aus, dass die bisherigen EU-Bestimmungen weiterhin gelten. Denn diese wurde auch wesentlich von der britischen Zulassungsbehörde Medicines and Healthcare Products Regulatory Agency (MHRA) geprägt . „Die MHRA wird zunächst Entscheidungen und Empfehlungen der EU-Gremien für entsprechende britische Zulassungen übernehmen bzw. sich sehr stark an diese anlehnen“, heißt es in der Broschüre. Der BAH rechnet aber mit größeren Änderungen im Bereich der Meldepflicht, weil Großbritannien künftig einen Drittstaatenstatus besitzt. Aus Sicht der Zulassungsinhaber seien jedoch zusätzliche Meldewege sowie Datenbanken und Portale der MHRA zu bedienen, da die notwendigen Einreichungen für britische Zulassungen nicht mehr über die entsprechenden EU-Portale möglich sind, erklärt der BAH. Für Nordirland werden die bisherigen EU-Regelungen zur Pharmakovigilanz beibehalten.
Wichtige Regelungen bei Medizinprodukten
CE-Kennzeichnung sowie Zertifikate, die von EU-anerkannten Benannten Stellen ausgestellt wurden, werden in Großbritannien noch bis zum 30. Juni 2023 anerkannt beziehungsweise sind weiterhin für den britischen Markt gültig. Die EU erkennt die britischen Benannten Stellen nicht mehr an. UK-Benannte Stellen können keine CE-Zertifikate ausstellen (außer für die Zwecke der „CE UK NI“-Kennzeichnung, die in Nordirland gültig ist) – und sind zu UK Approved Bodies geworden. Außerdem müssen seit dem 1. Januar 2021 alle Medizinprodukte, einschließlich In-vitro-Diagnostika (IVDs), die in Großbritannien auf den Markt gebracht werden, bei der MHRA registriert werden.
Die ausführliche Broschüre „Der Brexit und seine Folgen für die deutsche Arzneimittelindustrie“ hat der BAH zum Download bereitgestellt.





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.