
- DAZ.online
- News
- Recht
- Von der Opiumtinktur zur ...
Zukunft des Rezepturprivilegs
Von der Opiumtinktur zur allgemeinen Sorge um die Rezeptur
Süsel - 12.08.2021, 07:00 Uhr
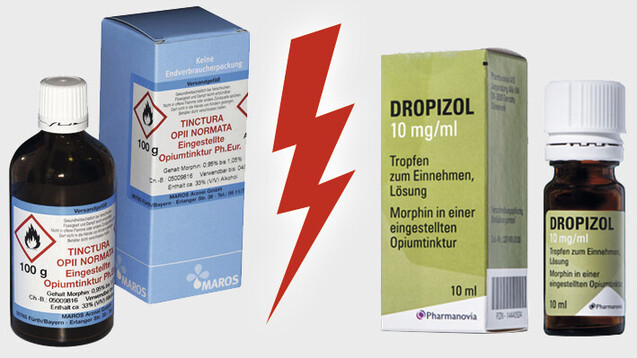
Ist abgefüllte Opiumtinktur ein zulassungspflichtiges Fertigarzneimittel? (Quellen: Maros Arznei / Screenshot www.innocur.de / DAZ)
Fertigarzneimittel mit Pharmazentralnummern von zwei Anbietern
Ein weiterer Aspekt ist die Verfügbarkeit des Fertigarzneimittels. Der bisherige deutsche Vertreiber Innocur Pharma GmbH verweist mittlerweile auf seiner Internetseite zu Fragen über Dropizol® auf Pharmanovia und bietet eine Lieferunfähigkeitsbescheinigung für die 1er-Packung (10 ml). Die größeren Packungen seien lieferbar. Auf Anfrage der DAZ erklärte Innocur dazu, dass Pharmanovia den Distributionsvertrag für Dropizol® gekündigt habe, dies sei aber Gegenstand laufender Verfahren.
Seit dem 1. Juli ist das Produkt in der Lauer-Taxe zusätzlich unter demselben Namen mit anderen Pharmazentralnummern und der Herstellerangabe Atnahs Pharma Nordics A/S zu finden. Der dänische Hersteller Pharmanovia wurde von der britischen, international tätigen Atnahs-Gruppe übernommen, die den Namen Pharmanovia seit Kurzem für das ganze international tätige Unternehmen nutzt. Es gehört mehrheitlich zum britischen Private-Equity-Unternehmen Triton.
Im jüngsten Brief von Pharmanovia an Apotheken heißt es, Dropizol® könne über Pharmanovia bestellt werden. Dazu werden die neuen Pharmazentralnummern der Atnahs Pharma Nordics A/S genannt. Auf Anfrage der DAZ erklärte Pharmanovia: „Die Distribution erfolgt durch einen vollversorgenden deutschen Großhändler.“ Es habe zu keinem Zeitpunkt eine Versorgungslücke für Dropizol® gegeben. Anderslautende Informationen seien falsch, erklärte Pharmanovia. In der vorigen Woche verliefen stichprobenweise Anfragen einer Apotheke bei drei Großhändlern nach der 1er-Packung mit der neuen Pharmazentralnummer jedoch negativ; die 10er-Packung (100 ml) war bei einem Großhändler verfügbar. Erstattungsfähig sind jedoch nur die 1er- und die 4er-Packung (10 bzw. 40 ml).
Entscheidung auf dem Verwaltungsweg möglich
So vermischen sich die aktuelle Entwicklung zur Opiumtinktur und die langfristige Sorge der Apotheker um den Bestand der Rezeptur als Institution. Die laufenden gerichtlichen Verfahren können zu einer Klärung durch ein höchstrichterliches Urteil führen. Abhängig vom Ergebnis sind auch politische Reaktionen denkbar. Doch dies alles würde Jahre dauern. Viel schneller könnte eine Entscheidung auf dem Verwaltungsweg fallen. Denn die Regierung Oberfranken hat bereits am 20. Mai 2019 gemäß § 21 Abs. 4 AMG beim Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) beantragt, die Zulassungspflicht der Opiumtinktur zu überprüfen. Eine ausführlichere Darstellung finden Sie in der aktuellen Ausgabe der DAZ.





















2 Kommentare
Rezepturprivileg?
von Roland Mückschel am 12.08.2021 um 9:53 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Privileg !?
von ratatosk am 12.08.2021 um 8:28 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Das Kommentieren ist aktuell nicht möglich.