Weitere Informationen zur Frankfurt Foundation Quality of Medicines und die Möglichkeit zur Kontaktaufnahme finden sich unter frankfurt-foundation.org.
Halsschmerzen
» Zu den Artikeln
Stuttgart - 16.11.2021, 09:15 Uhr

Der Stiftungsvorstand der Frankfurt Foundation Quality of Medicines: Dr. Dagmar Walluf-Blume, Prof. Dr. Henning Blume, Prof. Dr. Dagmar Fischer (v. l. n. r.). (Foto: Kerstin Tschuck / Frankfurt Foundation Quality of Medicines)
Jeder, der den Valsartan-Skandal verfolgt hat und nun kaum überrascht ist über weitere Funde von Verunreinigungen in Arzneimitteln, weiß, dass es mit der Arzneimittelqualität nicht immer zum Besten bestellt ist. Doch das ist nur ein Beispiel. Auch das Problem „Bioäquivalenz“ innerhalb der Flut von Generika ist nicht nachhaltig gelöst. Die 2019 von Prof. Dr. Henning Blume und seiner Frau Dr. Dagmar Walluf-Blume gegründete Stiftung „Frankfurt Foundation Quality of Medicines“ will sich diesen Fragen annehmen, indem sie Forschungsaktivitäten auf diesem Gebiet initiiert und fördert. Im Gespräch mit der DAZ erläuterte Professor Blume die Beweggründe.
Ältere Kolleginnen und Kollegen kennen Prof. Dr. Henning Blume noch aus den Zeiten, als er als Leiter des Zentrallaboratoriums Deutscher Apotheker (ZL) mit Bioäquivalenzstudien auf sich aufmerksam gemacht hat. Es war in den 1980er- und 1990er-Jahren und damit in den Zeiten, als immer mehr Originalpräparate generische Konkurrenz bekamen – so auch Euglucon®, das Original des Antidiabetikums Glibenclamid.
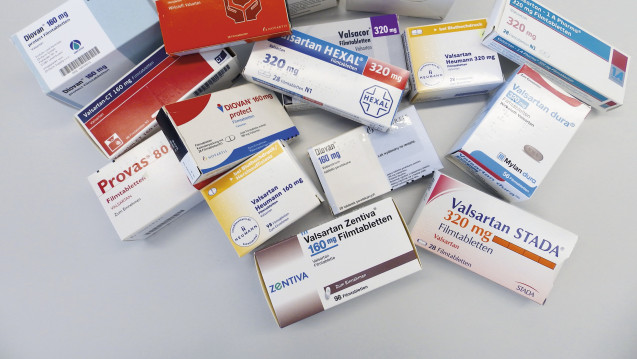
Blume konnte damals mit seiner ZL-Arbeitsgruppe zeigen, dass es zwischen den Generika teilweise erhebliche Qualitätsunterschiede nicht nur in vitro, sondern auch in vivo gab. Die Sensibilisierung für dieses Thema sorgte schließlich dafür, dass seit 1988 im Arzneimittelgesetz die Bioäquivalenz als Zulassungskriterium für Generika vorgeschrieben wurde. Nachfolgend hat man sich auch auf europäischer Ebene dieser Thematik angenommen und entsprechende Guidelines implementiert. Darauf ist Blume rückblickend besonders stolz.
Auf die Situation heute angesprochen, erklärte Blume: „Die Bioäquivalenzproblematik ist leider bis heute nicht nachhaltig gelöst geworden. Bedauerlicherweise hat offenbar niemand mehr Interesse, die Debatte zu dieser Thematik konsequent am Leben zu halten, so wie die Apothekerschaft das über viele Jahre getan hat.“
„Die Bioäquivalenzproblematik ist leider bis heute nicht gelöst!“
Prof. Dr. Henning Blume
Erklärtes Ziel der Frankfurt Foundation Quality of Medicines sei es nun, Forschungsaktivitäten zur Förderung der Arzneimittelqualität zu unterstützen. Das ist vor dem Hintergrund von Blumes Lebenswerk erst einmal nicht verwunderlich. Doch die Beweggründe des Ehepaars Blume sind tiefer: „Die derzeitige Arzneimittel-Zulassung und auch die Marktüberwachung durch die Länderbehörden stoßen an ihre Grenzen. Das hat der Valsartan-Skandal deutlich vor Augen geführt!“
Blume betont, dass man sich stets bewusst sein muss, dass Arzneimittel nur in einem „Modell“ zugelassen werden. Die klinischen Prüfungen würden dann mit einem Prototyp des Arzneimittels durchgeführt, der dabei in seiner Qualität, Pharmakokinetik und klinischen Wirksamkeit sowie Sicherheit charakterisiert werde. Die entscheidende Frage sei jedoch, wie sichergestellt werden kann, dass alle späteren Produktions-Chargen in ihrer Qualität sowie den klinischen Effekten diesem Prototyp tatsächlich entsprechen – kurz, ob sie Charge für Charge tatsächlich bioäquivalent sind.
„Vielfach sind diese In-vitro-Qualitätskontrollkriterien nicht wirklich prädikativ für das In–vivo–Verhalten der Arzneimittel!“
Prof. Dr. Henning Blume
Mit diesem Ziel würden zwar im Rahmen der Zulassung spezielle Akzeptanzkriterien für die Variabilität der Qualität definiert, von denen erwartet werde, dass sie auch später die Konstanz der Qualität während der Produktion für den Markt sicherstellen. Die Erfahrungen zeigten jedoch, dass dies nicht in allen Fällen tatsächlich gewährleistet sei. Blume: „Vielfach sind diese In-vitro-Qualitätskontrollkriterien nicht wirklich prädikativ für das In–vivo–Verhalten der Arzneimittel!“
„Die derzeitige Arzneimittel-Zulassung und auch die Marktüberwachung durch die Länderbehörden stoßen an ihre Grenzen. Das hat der Valsartan-Skandal deutlich vor Augen geführt!“
Prof. Dr. Henning Blume
Für Blume ein grundsätzliches Problem, das eine adäquate Lösung verlangt und Grundlagenforschung erfordert. Doch diese über die eigene Produktpalette hinausgehende Grundlagenforschung gehöre nicht zu den originären Aufgaben der pharmazeutischen Industrie, die schließlich Wirtschaftsunternehmen seien, erklärt Blume. Vielmehr wären solche Aktivitäten am besten an Hochschulen platziert. Doch nur wenige Hochschulinstitute in Deutschland würden sich mit solchen Fragen beschäftigen. Hier neue Anreize zu setzen, das ist ein wichtiges Anliegen der Stiftungsgründer.
Mit der Stiftung möchte das Ehepaar Blume letztlich dazu beitragen, dass die Qualität von Arzneimitteln in Deutschland optimal gesichert und ggf. weiter optimiert wird, auch wenn die Herstellung außerhalb des Landes erfolgt. Dazu sollen neue Verfahren entwickelt und innovative Technologien und Standardisierungsansätze implementiert werden. Im Idealfall ergeben sich daraus Instrumente für die Chargenfreigaben, die eine Qualitätssicherung mit prädiktivem Potenzial für die Anwendung am Patienten ermöglichen. Selbstverständlich müssen vor diesem Hintergrund auch bestehende Konzepte zur Qualitätssicherung kritisch hinterfragt werden. Mit dem Ziel, optimierte Verfahren zur Qualitätssicherung zu entwickeln und deren Anwendung in der Praxis zu verbessern, möchte die Stiftung entsprechende Doktor-, Diplom- oder Seminararbeiten an Universitäten fördern, aber auch weitere wissenschaftliche Projekte, die sich mit solchen Fragestellungen beschäftigen.
Ein besonderes Anliegen der Stifter ist die Förderung von Forschungsarbeiten, die sich mit dem Nachweis der Austauschbarkeit wirkstoffidentischer Produkte befassen, vor allem durch den Beleg der Bioäquivalenz. Damit knüpft die Stiftung an die wegweisenden Forschungsarbeiten ihres Initiators Prof. Dr. Henning Blume an. Aber auch Aktivitäten, die die Bedeutung der Arzneimittelqualität für die Arzneimitteltherapiesicherheit in das öffentliche Bewusstsein rücken, sind förderungswürdig.
Die Stiftung ist sowohl national wie international gut vernetzt. Sie kooperiert mit der European Federation for Pharmaceutical Sciences (EUFEPS) und der Deutschen Pharmazeutischen Gesellschaft (DPhG), deren Präsidentin, Prof. Dr. Dagmar Fischer, auch im Vorstand der Stiftung ist. Weiterer Kooperationspartner ist die Deutsche Plattform NanoBioMedizin.
„Die Qualität von Arzneimitteln in Deutschland muss optimal gesichert und weiter optimiert werden, auch wenn die Herstellung außerhalb des Landes erfolgt!“
Prof. Dr. Henning Blume
Im Rahmen der Förderung von Forschungsaktivitäten zur Sicherstellung und Optimierung der Arzneimittelqualität werden auch Preise ausgelobt. Ein erster Preis wurde in Kooperation mit der DPhG im Rahmen der diesjährigen DPhG-Jahrestagung an Juniorprofessor Dr. Oliver Scherf-Clavel aus Würzburg verliehen.
Scherf-Clavel hatte sich ganz im Sinne der Stiftung mit seinen Arbeiten zur Kontamination von Valsartan und weiteren Sartanen verdient gemacht. Er ist im Arbeitskreis von Prof. Dr. Ulrike Holzgrabe tätig, die parallel zu den Forschungsarbeiten von Scherf-Clavel und zusammen mit weiteren Mitstreitern wie Dr. Helmut Buschmann und Prof. Dr. Fritz Sörgel wesentlich dazu beigetragen hat, dass nicht nur in der Fachwelt für die regulatorischen Probleme sensibilisiert wurde, die diesen Skandal um verunreinigte Arzneimittel erst möglich gemacht haben.
Weitere Informationen zur Frankfurt Foundation Quality of Medicines und die Möglichkeit zur Kontaktaufnahme finden sich unter frankfurt-foundation.org.
0 Kommentare
Das Kommentieren ist aktuell nicht möglich.