
- DAZ.online
- DAZ / AZ
- DAZ 49/2004
- Vitamine in der Prä...
Ernährung heute
Vitamine in der Prävention – Qualifizierte Ernährungsberatung in der Apotheke
Vitamine einst und jetzt
Lange Zeit war der Focus in der Vitaminforschung darauf gerichtet, die Vitamine zu identifizieren und die Mengen zu definieren, die notwendig sind, um typische Mangelerscheinungen zu vermeiden. Dies erklärt sich aus der Tatsache, dass die Entdeckung praktisch aller Vitamine im Zeitraum von 1897 bis 1941 mit Erkrankungen verbunden war, die sich als Mangel an der jeweiligen Substanz entpuppten. Bekanntermaßen werden die Vitamine anhand ihres Löslichkeitsverhaltens in hydro- und lipophile Verbindungen differenziert; diese Einteilung geht allerdings nur partiell mit den physiologischen Eigenschaften einher.
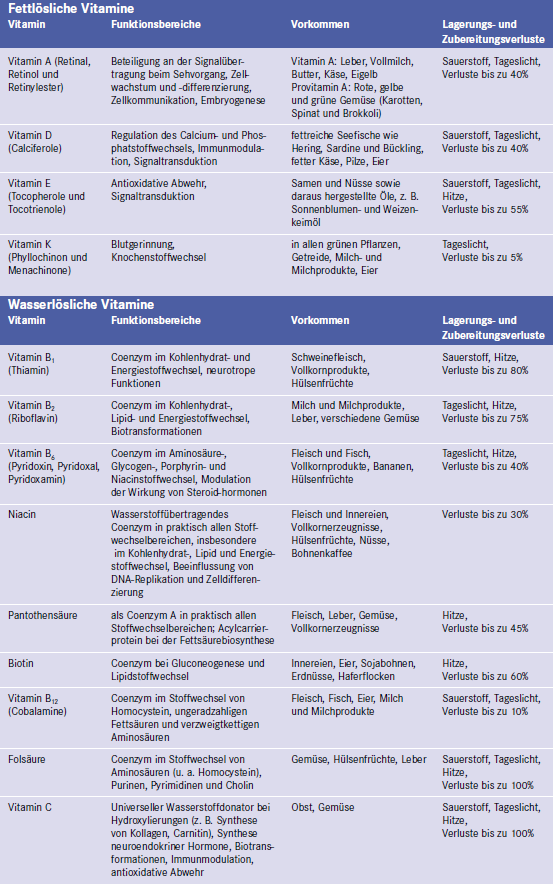
Tabelle 1 gibt einen Überblick über das Vorkommen und die wichtigsten Funktionsbereiche der verschiedenen Vitamine sowie die bei der Nahrungszubereitung auftretenden Vitaminverluste. Dabei zeigt sich bereits, dass die verschiedenen Verbindungen nicht nur, wie anfangs angenommen, vornehmlich als Cofaktoren bei enzymkatalysierten Reaktionen eine Rolle spielen, sondern einen weitaus breiteres Wirkspektrum umfassen. Hieraus erklären sich auch zunehmend die in epidemiologischen und klinischen Studien festgestellten präventiven und teilweise auch therapeutischen Effekte vieler Vitamine.
So ist beispielsweise Vitamin E nicht nur das physiologisch bedeutsamste lipophile Antioxidans, das vor allem Polyenfettsäuren vor der Peroxidation schützt. Gleichermaßen beeinflusst diese dem Vitamin-E-Molekül immanente antioxidative Eigenschaft redoxsensitive Signalkaskaden in der Zelle [1]. Dadurch wird die Expression bestimmter Proteine moduliert; dies erklärt u. a. die antiphlogistischen Eigenschaften von Vitamin E, die beispielsweise bei der diätetischen Therapie von rheumatoiden Erkrankungen genutzt werden [6].
Tab. 1: Einteilung der Votamine nach ihrem Löslichkeitsverhalten sowie Angaben zu Vorkommen, Lagerungs- und Zubereitungsverlusten einzelner Vitamine [35]
Vitaminversorgung in Deutschland
Grundsätzlich wäre es bei dem heute ganzjährig zur Verfügung stehenden reichhaltigen Lebensmittelangebots möglich, eine ausreichende Zufuhr aller Vitaminen sicherzustellen; allerdings führt die ungünstige Lebensmittelauswahl häufig dazu, dass dies nicht der Fall ist. Legt man bei der Bewertung der Vitaminversorgung die derzeitigen offiziellen Empfehlungen für die Vitaminzufuhr zugrunde, gilt die Vitaminversorgung nach Auffassung der Fachgremien in Deutschland als weitgehend gesichert. Allerdings bestehen nach neueren Daten insbesondere bei Folsäure sowie den Vitaminen D und E potenzielle Probleme einer unzureichenden Aufnahme [20].
Trotz dieses rechnerischen Defizits finden sich in der Praxis nur in seltenen Ausnahmefällen "klassische" schwerwiegende Mangelsymptome. Im Vordergrund stehen vielmehr metabolische Veränderungen, die sich bisweilen in Form unspezifischer Symptome manifestieren (z. B. Müdigkeit, Abgeschlagenheit, Schwäche und verminderter Immunabwehr) bzw., wie nachfolgend noch zu zeigen, das Risiko für bestimmte chronisch-degenerative Erkrankungen erhöhen.
LOAL = Lowest Observed Adverse Effect Level
NOAL = No Observed Adverse Effect Level
RDA = Reccommended Dietary Allowance
UL = Tolerable Level of Upper Intake
Während die Zufuhr der vorgenannten Vitamine in praktisch allen Teilen der Bevölkerung als suboptimal angesehen werden kann, ist in einigen Bevölkerungsgruppen die Versorgung mit weiteren Vitaminen nicht sichergestellt. Allen voran zu nennen sind hier ältere Menschen (Vitamin B12,) [72, 85] sowie Schwangere und Stillende (Vitamin B) [65], aber auch Personen mit besonders restriktiven Ernährungsgewohnheiten (z. B. Menschen, die eine rein pflanzlich ausgerichtete Ernährungsweise praktizieren (Veganer) (Vitamin B12, Vitamin B) [37, 78, 79, s. a. Teil 1 dieser Artikelserie, DAZ 45/2004, S. 43 ff]
Präventive Wirkungen von Vitaminen
Vitaminmangelsymptome sind also in Deutschland selten anzutreffen. Betrachtet man die Vitaminversorgung jedoch unter präventiven Gesichtspunkten, so ist sie vielfach suboptimal. Wie bereits im ersten Teil dieser Beitragsserie gezeigt, besteht das zentrale Anliegen der Ernährungswissenschaft heute vor allem darin, Nährstoffmengen zu definieren, die eine optimierte Funktion des Organismus und seine langfristige Gesunderhaltung sicherstellen. Dieser Gesichtspunkt tritt bei keiner Nährstoffgruppe derzeit auch in der öffentlichen Diskussion so stark in den Vordergrund wie bei den Vitaminen.
Kontrovers diskutiert wird dabei insbesondere die Frage, inwieweit eine zusätzliche, teilweise über den derzeitigen Empfehlungen liegende Zufuhr, dazu beitragen kann, bestimmten Erkrankungen vorzubeugen. Wie eigene Untersuchungen zeigen, verwenden auch viele Verbraucher Vitaminsupplemente primär in der Erwartung, sich hierdurch langfristig gesund zu erhalten und verschiedenen Erkrankungen vorzubeugen [84].
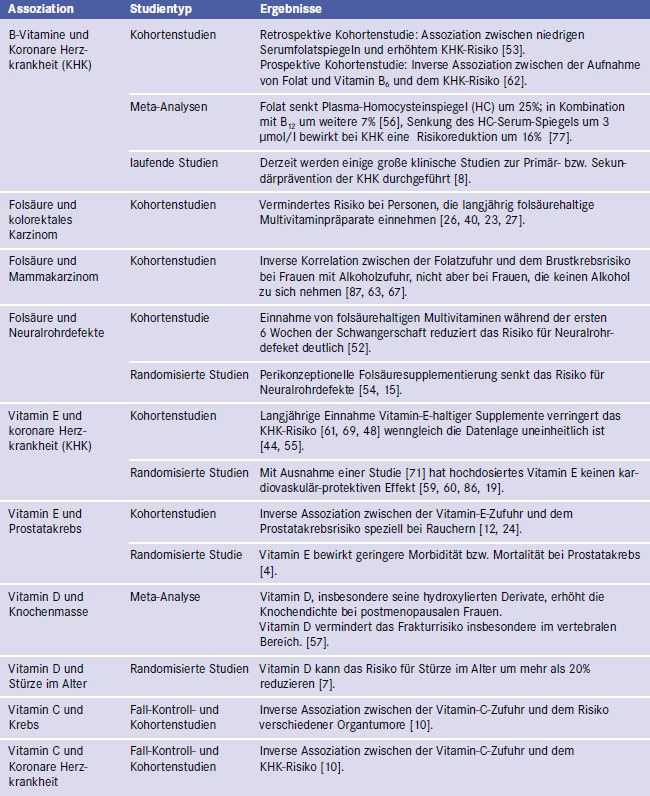
Inzwischen liegt eine nicht mehr überschaubare Zahl an Einzelstudien vor, die solche Effekte sowohl belegen als auch negieren. Unter den in Teil 1 der Beitragsserie dargestellten Evidenzgesichtspunkten sind Wirkungen vielfach (noch?) nicht hinreichend wissenschaftlich abgesichert. Wie aus der exemplarischen Aufstellung in Tabelle 3 zu entnehmen ist, liegen vor allem Daten zu den Vitaminen E, D, C und Folsäure vor. Diese entstammen vorwiegend Beobachtungsstudien, wohingegen vergleichsweise wenige bzw. widersprüchliche (z. B. bei Vitamin E) Ergebnisse aus Interventionen existieren, sodass eine abschließende Bewertung derzeit nicht möglich ist.
Ableitung der toxikologischen Eckdaten von Nährstoffen am Beispiel Vitamine
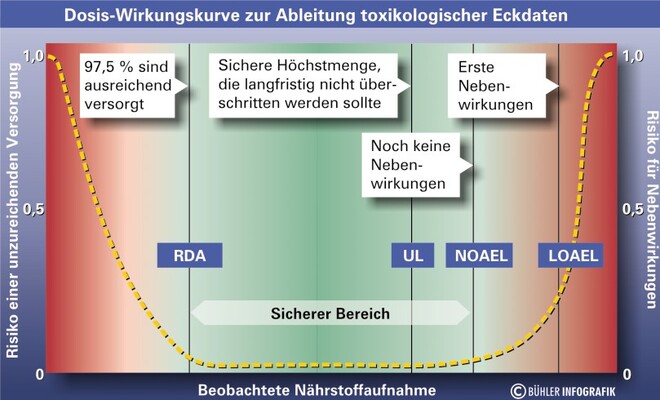
Mit steigender Aufnahme eines Nährstoffes verringert sich innerhalb einer Bevölkerungsgruppe zunächst das Risiko einer unzureichenden Versorgung (siehe Abb. 1). Der EAR (estimated average requirement) gibt die Zufuhrmenge an, bei der 50% einer Population nach allgemeiner Auffassung ausreichende Mengen des Nährstoffs erhalten. Die empfohlene Nährstoffzufuhr (RDA = Recommended Dietary Allowance) ist dagegen so beschaffen, dass "nahezu die gesamte Bevölkerung" (statistisch 97,5% eines Kollektivs) ausreichend mit Nährstoffen versorgt wird.
Mit weiter steigender Dosis wird dann ein Indifferenzbereich durchschritten, innerhalb dessen sich nach klassischem Verständnis keine weitere Funktionsverbesserung ergibt, aber auch keine unerwünschten Wirkungen auftreten. Noch höhere Zufuhren führen schließlich zu einem sukzessiv zunehmenden Risiko für unerwünschte Effekte und Nebenwirkungen.
Erste unerwünschte Wirkungen werden im Bereich des LOAEL (lowest observed adverse effect level) beobachtet. Dieser ist allerdings für viele Vitamine nicht bestimmt. Daher erfolgt eine Orientierung am NOAEL (no observed adverse effect level), der Dosis eines Vitamins, bei der keine Nebenwirkungen beobachtet wurden. Aufgrund der unterschiedlichen Qualität der vorliegenden Daten und vor dem Hintergrund, dass die beobachteten Nebenwirkungen einen unterschiedlichen Schweregrad besitzen, werden die NOAEL-Werte durch einen Faktor dividiert, der diesen Unsicherheiten Rechnung trägt.
Die resultierenden Werte werden als Tolerable Level of Upper Intake (UL) bezeichnet. Sie geben Vitamindosierungen an, die insgesamt langfristig vom Gesunden nicht überschritten werden sollte. Zu berücksichtigen ist also die Zufuhr aus allen Quellen ("normale" Lebensmittel, angereicherte Produkte, Getränke, Nahrungsergänzungsmittel). Grundsätzlich ist deshalb dringend davon abzuraten, Vitamine in Dosierungen aufzunehmen, die den UL übersteigen. Kritisch zu bewerten und auch im Sinne der lebensmittelrechtlichen Vorgaben abzulehnen sind deshalb z. B. Nahrungsergänzungsmittel, die solche extremen Dosierungen aufweisen.
Aus diesem Grund wird die generelle Verwendung von Vitaminsupplementen in der Allgemeinbevölkerung von den wissenschaftlichen Fachgremien bislang nicht empfohlen. Dies darf aber nicht dahingehend fehlinterpretiert werden, dass eine Supplementierung bestimmter Vitamine generell ohne ernährungsphysiologischen Nutzen ist. Die pauschale Aussage, Supplemente führten ausschließlich zur Bildung von teurem Urin, ist einmal mehr ein Beispiel für eine undifferenzierte und wenig ziel führende Sichtweise, wie im Laufe der Artikelserie an ausgewählten Beispielen zu zeigen sein wird. Ebenso einseitig und unbegründet ist die in einigen Kreisen verbreitete Auffassung, wonach die z. T. hoch dosierte Gabe von Vitaminen für jedermann zur Gesunderhaltung schon fast obligat sein sollte.
Vor dem Hintergrund dieser bisweilen spürbaren "Vitamin-Hysterie" gewinnt auch die Frage an Bedeutung, inwieweit eine deutlich über den Empfehlungen liegende Aufnahme von Vitaminen die Gesundheit gefährden könnte. Getreu dem Satz von Paracelsus "Dosis facit venerum – die Dosis macht das Gift" kann selbstverständlich auch eine überhöhte Zufuhr von Vitaminen mit toxischen Effekten verbunden sein. Allerdings ist die akute Toxizität von Vitaminen in der Praxis ohne Bedeutung.
Potenzielle Nebenwirkungen von Vitaminen finden sich vorwiegend bei langfristiger hochdosierter Gabe. Um die Bevölkerung vor möglichen nachteiligen Effekten einer überhöhten Vitaminzufuhr zu schützen, müssen toxikologische Eckdaten definiert werden, die eine Orientierung für die Praxis bieten. Die grundsätzlichen wissenschaftlichen Hintergründe der Ableitung von Höchstmengen sind im Kasten "Ableitung der toxikologischen Eckdaten" vereinfacht dargestellt. Insgesamt ist das gesundheitliche Risiko einer überhöhten Vitaminaufnahme wegen der großen therapeutischen Breite bei den meisten Vitaminen gering.
Tabelle 2 fasst die toxikologischen Kenndaten der einzelnen Vitamine zusammen und gibt die Zufuhrmengen an, die auch bei langfristiger Aufnahme als sicher gelten. Sie sollten bei der Verwendung von Supplementen in der Allgemeinbevölkerung keinesfalls überschritten werden. Unter therapeutischer Überwachung sind kurzfristig aber auch höhere Vitamingaben möglich.
Tab. 2: Toxikologische Kenndaten von Vitaminen [32, 20]
| Nährstoff | Einheit | Empfohlene Zufuhr (Deutsche Gesellschaft für Ernährung; Personen von 25 – 51 Jahren) | NOAEL1 | UL2 | Maximale Aufnahme über Supplemente bei Gesunden | |
|---|---|---|---|---|---|---|
| m | w | |||||
| Vitamin A | mg RÄ4 | 1,0 | 0,8 | 3,0 | 3,0 | 800 |
| Vitamin D | μg | 5 | 5 | 206 1007 | 50 | 25 |
| Vitamin E | mg TÄ5 | 14 | 12 | 8006 5007 | 300 | 250 |
| Vitamin K | μg | 70 | 60 | 300006 100007 | – | 400 |
| Vitamin B1 | mg | 1,2 | 1,0 | 506 5007 | 50 | 40 |
| Vitamin B2 | mg | 1,4 | 1,2 | 2006 4007 | 200 | 50 |
| Vitamin B6 | mg | 1,5 | 1,2 | 2006 | 200 | 15 |
| Vitamin B12 | μg | 3 | 3 | 30006 50007 | – | 500 |
| Folsäure | μg FÄ6 | 400 | 400 | 10006 | 1000 | 600 |
| Nicotinsäureamid | mg | 16 | 13 | 15006 18007 | 900 | 250 |
| Biotin | μg | 30 – 60 | 30 – 60 | 25006 | 500 | |
| Patothensäure | mg | 6 | 6 | 10006 20007 | 1000 | 200 |
| Vitamin C | mg | 100 | 100 | > 10006 | 600 | 600 |
| 1 No Observed Adverse Effect Level 2 Tolerable Upper Intake Level 3 Retinoläquivalent 4 Tocopheroläquivalent 5 Folsäureäquivalent 6 nach SCF (Scientific Committe on Food) 2003 7 nach Hathcock (Council for Responsible Nutrition) 1997 | ||||||
Vitamine in der Prävention – das Beispiel Folsäure
In der Diskussion um die präventiven Effekte von Vitaminen hat in den letzten Jahren die Folsäure ein besonderes Interesse geweckt, wie auch aus Tabelle 3 hervorgeht. Folsäure (oder auch Folate) ist die zusammenfassende Bezeichnung für eine Gruppe von rund 100 verschiedenen Verbindungen (Vitamere), die sich formal von der in der Natur nicht vorkommenden Pteroylmonoglutaminsäure ableiten. Gute Folsäurelieferanten sind insbesondere Grüngemüse wie Spinat und verschiedene Kohlarten sowie Sojabohnen und Leber (Tab. 4). Folate sind wasserlöslich, lichtempfindlich und hitzelabil.
Durch die Zubereitung von Lebensmitteln (Lagerung, Hitze, Koch- und Waschwasser) können mehr als 90% des Vitamins verloren gehen. Dies ist ein wesentlicher Grund dafür, dass die Folsäureversorgung vielfach als kritisch anzusehen ist. Von ernährungsphysiologischer Bedeutung ist neben dem Gesamtfolsäuregehalt auch die Bindungsform der in der Nahrung enthaltenen Folsäure. In einer gemischten Kost liegt nur ein geringer Anteil in "freier" Form,
d. h. als Monoglutamate, vor, der größte Teil ist als Folsäurepolyglutamate enthalten.
Tab. 3: Übersicht ausgewählter Sutdien zum präventiven Effekt einzelner Vitamine [modifiziert und erweitert nach 21]
Die Bioverfügbarkeit der Polyglutamate ist eingeschränkt, da sie zunächst in die entsprechenden Monoglutamate überführt werden müssen. Dies geschieht durch spezifische Gamma-Glutamat-Carboxypeptidasen (Konjugasen), die im Bürstensaum der Mukosazelle lokalisiert sind [13]. Allerdings ist die Aktivität dieser Enzyme begrenzt, so dass die Hydrolyse vielfach unvollständig ist und durch andere Nahrungsinhaltstoffe wie z. B. organische Säuren zusätzlich gehemmt wird [5, 80]. Aufgrund der zahlreichen Einflussfaktoren lässt sich die tatsächliche Folatabsorption nur schwer abschätzen. Bei einer gemischten Nahrung wird von einer mittleren Verwertbarkeit von nur etwa 50% ausgegangen [20].
Folsäuremonoglutamate, wie sie in Vitaminpräparaten enthalten sind, werden hingegen nahezu quantitativ absorbiert [29]. Um der unterschiedlichen Absorbierbarkeit der einzelnen Folsäureverbindungen Rechnung zu tragen, werden die Empfehlungen zur Folsäureaufnahme in Form von Folatäquivalenten (FÄ) ausgewiesen. Dabei entspricht 1 µg FÄ 1 µg Nahrungsfolat bzw. 0,5 µg synthetischer Folsäure [20].
Tab. 4: Folsäuregehalte von Lebensmitteln [45]
| Lebensmittel | Folsäure-Äquivalent (µg/100g) |
|---|---|
| Hoher Gehalt | |
| Bäckerhefe | 716 |
| Weizenkeime | 520 |
| Hühnerleber | 380 |
| Spinat | 145 |
| Endivien | 109 |
| Mittlerer Gehalt | |
| Rote Bete | 83 |
| Sauerkirschen | 75 |
| Hühnerei | 67 |
| Limburger (40% Fett i. Tr.) | 60 |
| Niedriger Gehalt | |
| Kartoffeln | 20 |
| Joghurt (3,5% Fett i. Tr.) | 13 |
| Scholle | 11 |
| Kalbfleisch | 5 |
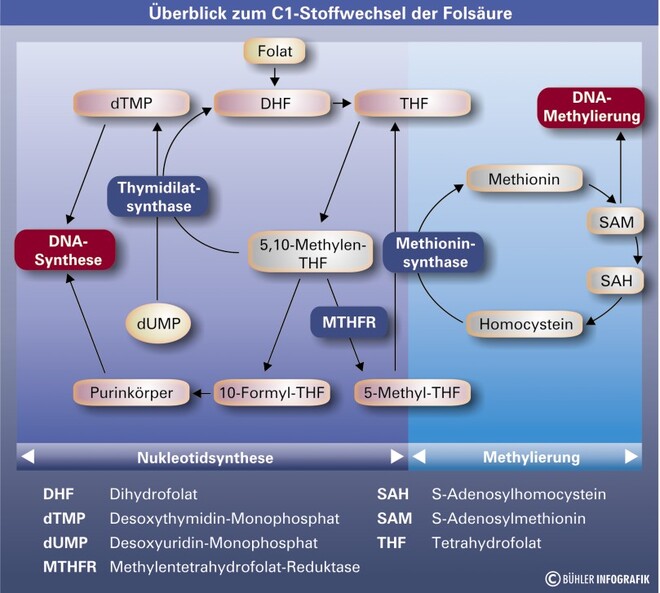
Die im Organismus aktive Folsäureverbindung ist die Tetrahydrofolsäure (THF), die durch zweifache Reduktion von Folsäure entsteht. Sie fungiert als Coenzym bei der Übertragung von C1-Substituenten im Stoffwechsel der Aminosäuren, Purine und Pyrimidine (Abb. 2). THF dient dabei als intermediärer Akzeptor bzw. Donator von Methyl-, Methylen- und anderen C1-Resten. Die Einschleusung dieser Kohlenstoffsubstituenten erfolgt vor allem über 5,10-Methylen-THF. Diese besitzt eine zentrale Stellung im intermediären C1-Stoffwechsel, da sie an drei fundamentalen Stoffwechselreaktionen beteiligt ist.
Während 5,10-Methylen-THF in die Thymidilat- und Serinsynthese eingebunden ist, fungiert ihre oxidierte Form Formyl-THF als Donator von C1-Resten bei der Purinsynthese (Abb. 2). Die Bedeutung dieser Verbindungen für die DNA-Replikation erklärt die wesentliche Funktion der Folsäure bei Zellwachstum und -teilung. Die Reduktion von 5,10-Methylen-THF führt zu 5-Methyl-THF, die für die Remethylierung von Homocystein benötigt wird. Dieser Prozess ist gleichzeitig auch auf Vitamin B12 angewiesen, das vorübergehend die Methylgruppe von Methyl-THF übernimmt und sie anschließend, unter Bildung von Methionin, auf Homocystein überträgt. Auch bei der Cholinbiosynthese stellt Methyl-THF den benötigten C1-Rest zur Verfügung [49].
Serinsynthese eingebunden, während die oxidierte Form Formyl-THF als Donator von C1-Resten bei der Purinsynthese fungiert. Die Reduktion von 5,10-Methylen-THF führt zu 5-Methyl-THF, die für die
Remethylierung von Homocystein benötigt wird. Aus dem hierbei gebildeten Methionin kann S-Adenosylmethionin (SAM) gebildet werden, das einen wichtigen Methylgruppendonator darstellt und an der Methylierung der DNA beteiligt ist.“
Folsäure und Herz-Kreislauf-Erkrankungen
Epidemiologische Untersuchungen zeigen, dass neben den etablierten Risikofaktoren wie Hypertonie, Hypercholesterolämie und Rauchen auch weitere Faktoren das Krankheitsgeschehen begünstigen. Inzwischen ist nachgewiesen, dass ein erhöhter Plasmaspiegel der nicht-proteinogenen Aminosäure Homocystein (Hyperhomocysteinämie) ebenfalls als kardiovaskulärer Risikofaktor anzusehen ist [74]. Biostatistischen Berechnungen zufolge könnten zwischen 11 und 25% der Herz-Kreislauf-Erkrankungen allein durch die Senkung erhöhter Homocysteinwerte vermieden werden [77].
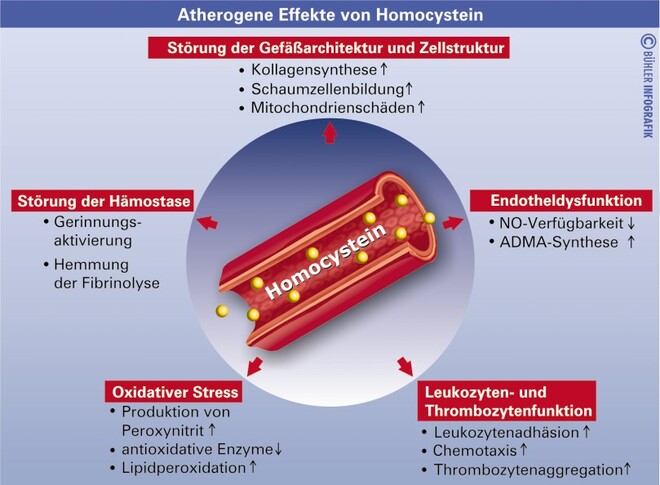
Homocystein vermittelt seine gefäßtoxische Wirkung durch eine Reihe von Mechanismen, die Abbildung 3 zu entnehmen sind. Die mit Abstand häufigste Ursache erhöhter Homocysteinspiegel ist eine unzureichende Folsäureversorgung. Etwa 5 – 7% der Allgemeinbevölkerung sind hiervon betroffen [51]. Auffällig ist die Situation bei Personen mit atherosklerotischen Erkrankungen, wo erhöhte Homocysteinwerte in 20 – 50% der Fälle zu beobachten sind [81].
Inzwischen liegen zahlreiche methodisch hochwertige, kontrollierte und randomisierte Studien vor, die zeigen, dass sich erhöhte Homocysteinwerte mit einer entsprechenden Folsäure-Supplementierung absenken lassen. Dieser Effekt lässt sich z. T. noch steigern, wenn zusätzlich die Vitamine B12 und B6 verabreicht werden, die ebenfalls am enzymatischen Abbau von Homocystein beteiligt sind [56, 11, 14]. Obwohl nicht abschließend geklärt ist, ob bzw. inwieweit eine optimierte Folsäurezufuhr das Auftreten arteriosklerotischer Erkrankungen vermindert, deuten sowohl Beobachtungsstudien als auch verschiedene klinische Untersuchungsergebnisse in diese Richtung.
So lässt sich unter Verabreichung von Folsäure u. a. die Funktion des Endothels positiv beeinflussen und das Fortschreiten der Arteriosklerose vermindern [70]. Von besonderem Interesse ist auch die Tatsache, dass eine entsprechende Vitaminsupplementierung die Plaquebildung in den Gefäßen herabsetzt [31]. Einen Aufschluss über die Reduktion so genannter. "harter Endpunktmarker" (kardiovaskuläre Morbidität und Mortalität) geben solche Untersuchungen jedoch nicht. Dieser Zusammenhang wird gegenwärtig in mehreren Interventionsstudien untersucht, deren Ergebnisse in den nächsten Jahren vorliegen werden.
Folsäure und kolorektale Tumore
Das Risiko für Dickdarm- und Mastdarmkrebs wird in erheblichem Umfang durch Ernährungsfaktoren beeinflusst. Die Mehrzahl der epidemiologischen Studien untermauert die Vermutung, dass eine unzureichende Folsäure-Versorgung ihre Entstehung begünstigt [27]. Für einen derartigen Zusammenhang sprechen insbesondere prospektive Kohortenstudien wie z. B. die Health Professionals Follow-up Study mit 47931 Männern im Alter von 40 bis 75 Jahren, bei denen das Auftreten von Kolonkarzinomen über einen Zeitraum von 6 Jahren erfasst wurde.
Während die Gesamtfolataufnahme und die Folataufnahme aus der Nahrung nicht signifikant zum Kolonkarzinom assoziiert waren, wiesen Männer, die folathaltige Multivitaminpräparate verwendeten, ein um 15% vermindertes relatives Risiko auf als Nicht-Verwender. Bei einer langfristigen Aufnahme (≥ 10 Jahre) wurde das relative Risiko sogar um rund 25% vermindert [25]. Auch Daten aus der Nurses Health Study untermauern die Hinweise auf präventive Effekte der Folsäure [26].
Bei Verwenderinnen von folsäurehaltigen Supplementen (mit mindestens 400 µg Folsäure/Tag) ergab sich im Vergleich zu den Nicht-Verwenderinnen nach mindestens 15-jähriger Einnahme ein um 75% geringeres relatives Kolonkarzinomrisiko. Dieser Effekt war bei Frauen mit positiver Familienanamnese besonders stark ausgeprägt [23]. Wie diese Studien zeigen, scheint das in Lebensmitteln natürlicherweise enthaltene Folat im Gegensatz zur synthetischen Folsäure einen vergleichsweise geringen chemopräventiven Effekt auszuüben [25, 26, 40].
Möglicherweise ist hierfür die Dosis und gute Bioverfügbarkeit der in Vitaminpräparaten enthaltenen Pteroylmonoglutamate verantwortlich. Nicht auszuschließen ist auch, dass andere Vitamine, die in den Supplementen neben Folsäure enthalten sind, Einfluss auf die Krebsentstehung nehmen. Aufgrund des Studiendesigns der erwähnten Kohortenstudien lässt sich daher nicht mit Sicherheit feststellen, ob die beobachtete Risikoreduktion ursächlich auf Folsäure zurückzuführen ist [26, 23].
Während die Daten aus Beobachtungsstudien zahlreich sind, mangelt es bislang an aussagekräftigen Interventionsstudien, die anhand definierter klinischer Endpunkte bzw. intermediärer Marker den Nutzen einer erhöhten Folsäurezufuhr mit Sicherheit belegen. Zudem zeigen tierexperimentelle Daten, dass die protektive Wirkung von Folsäure entscheidend vom Stadium der Kanzerogenese bestimmt wird. Während eine hohe Zufuhr die Bildung neoplastischer Veränderungen hemmt, kann sich dieser Effekt bei bereits bestehenden Neoplasien in sein Gegenteil umkehren und die Progression von Tumoren forcieren [41].
Embryopathien
Embryopathien, die vermutlich mit dem Folsäurestoffwechsel assoziiert sind
Orofaciale Fehlbildungen Aus experimentellen Untersuchungen ist bekannt, dass erhöhte Homocysteinspiegel sowie Störungen der indirekt von Folsäure abhängigen DNA-Methylierung teratogene Wirkungen entfalten und hierdurch vermutlich orofaciale Fehlbildungen begünstigen [43]. Sowohl Fall-Kontroll-Studien [68, 75] als auch eine Interventionsstudie [73] zeigen, dass die perikonzeptionelle Folsäuresupplementierung das Risiko für Lippen-, Kiefer- und Gaumenspalten reduzieren kann. Zum eindeutigen Beweis eines solchen Zusammenhanges sind jedoch weitere Untersuchungen erforderlich [36].
Angeborene Herzfehler und Fehlbildungen der Harnwege Zur Prävention angeborener Herzfehler [15, 9], Fehlbildungen der Harnwege und weiterer Embryopathien existieren einige Studien, die auf einen Schutzeffekt von folsäurehaltigen Multivitaminpräparaten hindeuten. So konnte z. B. gezeigt werden, dass eine Folsäuresupplementierung das Risiko für Harnwegsfehlbildungen um etwa 85% reduziert [47].
Folsäure und Neuralrohrdefekte
Die Prävention von Neuralrohrdefekten durch Folsäure kann als der am besten gesicherte präventive Effekt eines Vitamins angesehen werden [22, 76]. Dies dürfte auch darauf zurückzuführen sein, dass das Ergebnis einer Supplementierung im Gegensatz zu den oben angeführten Erkrankungen bekanntermaßen schon nach neun Monaten vorliegt. Die Ausbildung des Neuralrohrs ist ein kritischer Schritt in der frühen Embryonalentwicklung; sie beginnt ungefähr am 21. Schwangerschaftstag und ist schon sieben Tage später vollständig abgeschlossen. [64].
Ein fehlender bzw. unzureichender Schluss des Neuralrohrs ist die häufigste Fehlbildung des zentralen Nervensystems und führt zu Störungen in der Anlage des Wirbelkanals. Solche Fehlbildungen können im Bereich des Rückenmarks lokalisiert sein (Spina bifida) oder aber den cranialen Bereich betreffen und zu Entwicklungsstörungen am Gehirn führen, die bis hin zur Anenzephalie reichen können. In Deutschland werden jährlich zwischen 470 und 800 Kinder mit Neuralrohrdefekten geboren (1 – 1,5/1000 Geburten).
Bei schätzungsweise weiteren 500 Fällen erfolgt nach der Diagnose ein Schwangerschaftsabbruch [2]. Hinzu kommt eine unbekannte Anzahl von Schwangerschaften, bei denen es aufgrund unbekannter Neuralrohrdefekte frühzeitig zum Spontanabort kommt. [30]. Große Interventionsstudien haben gezeigt, dass die perikonzeptionelle Gabe von Folsäure das Risiko für einen Neuralrohrdefekt um 50 bis 70% reduzieren kann [3, 15, 16, 17]. Daher wird von entsprechenden wissenschaftlichen Fachgremien wie z. B. der Deutschen Gesellschaft für Ernährung empfohlen, dass Frauen, die schwanger werden wollen oder könnten, schon vor der Konzeption 400 µg Folsäure pro Tag als Supplement (synthetische Folsäure) aufnehmen sollen. Frauen, die bereits ein Kind mit Neuralrohrdefekten haben und erneut schwanger werden wollen, sollten zur Verhütung eines Neuralrohrdefektes beim nächsten Kind bereits vor der Konzeption 4,0 mg Folsäure pro Tag einnehmen [20]. Neuere Untersuchungen weisen außerdem darauf hin, dass das Risiko für verschiedene andere Embryopathien ebenfalls durch eine Folsäuresupplementierung gesenkt werden kann (s. Kasten "Embryopathien").
Tab. 5: Medikamente mit Einfluss auf den Folatstatus [nach 2]
| Folatanaloga bzw. -antagonisten |
|
|
|
|
|
|
| Pharmaka mit Einfluss auf Resorption/Utilisation |
|
|
|
|
|
|
Verbesserung der Folsäureversorgung in der Bevölkerung
Wie eingangs bereits dargestellt, ist die Vitaminversorgung – mit Ausnahme von Folsäure, Vitamin E und D – in der gesunden Allgemeinbevölkerung weitgehend gesichert. Problematisch ist die Versorgungssituation insbesondere bei Folsäure nicht zuletzt deshalb, weil verschiedene Erkrankungen und die Einnahme bestimmter Arzneimittel (s. Kasten "Arzneimittel-Nährstoff-Interaktionen am Beispiel Folsäure") das ohnehin vielfach vorhandende Defizit begünstigen.
So liegt die Zufuhr im Mittel nur bei etwa 250 µg/Tag [28], wobei Frauen (168 – 214 µg/Tag) deutlich schlechter abschneiden als Männer (197 – 325 µg/Tag) [18]. Wegen der sich abzeichnenden präventiven Wirkungen des Vitamins wird nach Maßnahmen gesucht, um die Folsäureversorgung zu optimieren. Verschiedene Länder wie z. B. die USA und Kanada sind dazu übergegangen, Mehl verpflichtend mit Folsäure anzureichern (s. Kasten "Folsäureanreichung von Lebensmitteln"). In Deutschland wird dies nicht praktiziert, sodass Aufklärungsmaßnahmen durch Mittlerpersonen wie z. B. Apothekern eine wichtige Rolle zukommt.
Eine Verbesserung der Folsäureversorgung wird bei der gesunden Durchschnittsbevölkerung bereits durch eine pflanzlich betonte Kostform erreicht, die einen hohen Anteil an Obst- und Gemüse sowie an Hülsenfrüchten, Vollkornprodukten und Nüssen aufweist. Hiermit verbunden ist auch eine vermehrte Zufuhr weiterer potenziell protektiv wirksamer Vitamine (z. B. Ascorbinsäure, Vitamin E) [39, 66]. Einmal mehr gilt deshalb, dass eine vielseitige Lebensmittelauswahl die beste Basis für eine ausgewogene Ernährung bildet. Sinnvoll zusammengesetzte Supplemente sind in der Lage, die Versorgung gezielt zu verbessern; ein Ersatz für eine gesunde Ernährung sind sie aber nicht.
Arzneimittel-Nährstoff-Interaktionen am Beispiel Folsäure
Zu den Nährstoffen, bei denen sich bevorzugt arzneimittelinduzierte Mangelerscheinungen zeigen, zählt das Vitamin Folsäure (s. Tab. 5). Verschiedene Pharmaka sind offenbar in der Lage, die intestinale Hydrolyse der Nahrungsfolate einzuschränken und damit die Absorption zu vermindern. So wird unter der Einnahme östrogenhaltiger Kontrazeptiva über verminderte Plasmafolsäurespiegel berichtet, die auf eine Hemmung der Folsäurepolyglutamatverwertung zurückgehen sollen [33, 34]. Über gleichartige Effekte wird bei der Therapie mit Antikonvulsiva berichtet.
Insbesondere für Phenytoin existieren zahlreiche tierexperimentelle Befunde sowie Ergebnisse aus Humanstudien [46, 85], die diesen Zusammenhang belegen. Auch Valproinsäure und Primidon, die bei der Epilepsiebehandlung eingesetzt werden, entfalten negative Effekte auf den Folsäurestoffwechsel [85]. Ein Teil der Störungen des Folathaushalts durch Pharmaka scheint nicht auf Beeinträchtigung der intestinalen Dekonjugation zurückzugehen, sondern ist durch Einschränkung der intermediären Umwandlung von Folsäure bedingt. So beruht das therapeutische Wirkprinzip einiger Medikamente auf der Hemmung des Folatstoffwechsels.
Ein typischer Folsäureantagonist ist Methotrexat, das vorwiegend zur Therapie von Karzinomen sowie bei schweren Fällen der rheumatoiden Arthritis zur Anwendung kommt. Zu den häufigsten Nebenwirkungen zählen die Schädigung der Darmmucosa sowie Störungen der Erythropoese und eine Erhöhung des Homocysteinspiegels, die allesamt auf einen Folsäuremangel zurückzuführen sind. Der negative Effekt auf die Homocysteinkonzentration gewinnt vor allem unter Langzeittherapie von Rheumapatienten an praktischer Bedeutung [85], weshalb bei diesem Personenkreis die Einnahme eines entsprechenden Supplements anzuraten ist [82].
Folsäureanreichung von Lebensmitteln
Da ein großer Teil der Bevölkerung die Zufuhrempfehlungen für Folat nicht erreicht und nur wenige Frauen im gebärfähigen Alter die Empfehlungen zur Supplementierung befolgen, befürwortet u. a. die Deutsche Gesellschaft für Kinderheilkunde und Jugendmedizin zur Verringerung des Neuralrohrdefektrisikos eine Anreicherung von Lebensmitteln mit Folsäure [42]. In einigen Ländern wurden in den vergangenen Jahren bereits Anreicherungsprogramme zur Verbesserung der Folatversorgung gestartet, um unter anderem das Auftreten von Neuralrohrdefekten zu reduzieren.
In den USA werden seit 1998 u. a. Mehle und Frühstückscerealien mit Folsäure angereichert. Die Konzentration wurde aus Sicherheitsgründen relativ gering gewählt, so dass die hierdurch erzielte Erhöhung der Folsäurezufuhr bei ca. 200 µg/Tag liegt [58]. Seit dem Zeitpunkt der Folsäureanreicherung wurde eine um 19-23% verringerte Prävalenz der Neuralrohrdefekte beobachtet [38,50]. Daneben zeigte sich eine Verminderung der Spina bifida-Prävalenz um 31% [83].
Literatur
Aus Platzgründen listen wir nachfolgend nur die wichtigsten Literaturstellen auf.
[ 7] Bischoff-Ferrari HA, Dawson-Hughes B, Willett WC, Staehelin HB, Bazemore MG, Zee RY, Wong JB: Effect of Vitamin D
on falls: a meta-analysis. JAMA 28;291(16): 1999-2006, 2004.
[ 8] Bostom AG, Garber C: Endpoints for homocysteine-lowering trials. Lancet 355: 511-512, 2000.
[10] Carr AC, Frei B: Toward a new recommended dietary allowance for vitamin C based on antioxidant and health effects in humans. Am J Clin Nutr 69(6): 1086-1107, 1999.
[14] Clarke R, Armitage J: Vitamin supplements and cardiovascular risk: review of the randomized trials of homocysteine-lowering vitamin supplements. Semin Thromb Hemost 26(3): 341-348, 2000.
[17] Czeizel AE: Primary prevention of neural-tube defects and some other major congenital abnormalities: recommendations
for the appropriate use of folic acid during pregnancy. Paediatr Drugs 2: 437-449, 2000.
[21] Fairfield KM, Fletcher RH: Vitamins for chronic disease prevention in adults: scientific review. JAMA 287(23): 3116-
3126, 2002.
[22] Fleming A: The role of folate in the prevention of neural tube defects: human and animal studies. Nutr Rev 59(8 Pt 2): 13- 20; discussion 21-23, 2001.
[27] Giovannucci E: Epidemiologic studies of folate and colorectal neoplasia: a review. J Nutr 132 (8 Suppl): 2350S-2355S, 2002.
[29] Gregory JF 3rd: Bioavailability of folate. Eur J Clin Nutr 51(Suppl)1: 54-59, 1997.
[39] Hu FB, Willett WC: Optimal diets for prevention of coronary heart disease. JAMA 27, 288(20): 2569-2578, 2002.
[40] Jacobs EJ, Connell CJ, Chao A, McCullough ML, Rodriguez C, Thun MJ, Calle EE: Multivitamin use and colorectal cancer incidence in a US cohort: does timing matter? Am J Epidemiol 158: 621-628, 2003.
[41] Kim YI: Role of folate in colon cancer development and progression. J Nutr 133 (11 Suppl 1): 3731S-3739S, 2003.
[43] Koletzko B, Pietrzik K: Gesundheitliche Bedeutung der Folsäurezufuhr. Deutsches Ärzteblatt 101(23), 1670-1681, 2004.
[46] Lewis DP, Van Dyke DC, Willhite LA, Stumbo PJ, Berg MJ.: Phenytoin-folic acid interaction. Ann Pharmacother 29(7-8):
726-735, 1995.
[49] Lucock M: Folic acid: nutritional biochemistry, molecular biology, and role in disease processes. Mol Genet Metab 71(1-
2):121-138, 2000.
[57] Papadimitropoulos E, Wells G, Shea B, Gillespie W, Weaver B, Zytaruk N, Cranney A, Adachi J, Tugwell P, Josse R,
Greenwood C, Guyatt G, Osteoporosis Methodology Group and The Osteoporosis Research Advisory Group: Meta-analyses
of therapies for postmenopausal osteoporosis. VIII: Metaanalysis of the efficacy of vitamin D treatment in preventing
osteoporosis in postmenopausal women. Endocr Rev 23(4): 560-569, 2002.
[70] Stanger O, Herrmann W, Pietrzik K, Fowler B, Geisel J, Dierkes J, Weger M: DACH-LIGA homocystein (german, austrian and swiss homocysteine society): consensus paper on the rational clinical use of homocysteine, folic acid and B-vitamins in cardiovascular and thrombotic diseases: guidelines and recommendations. Clin Chem Lab Med 41(11): 1392-1403,
2003.
[77] Wald DS, Law M, Morris JK: Homocysteine and cardiovascular disease: evidence on causality from a meta-analysis. BMJ 325 (7374): 1202, 2002.
[82] Whittle SL, Hughes RA: Folate supplementation and methotrexate treatment in rheumatoid arthritis: a review. Rheumatology (Oxford) 43(3):267-271, 2003.
1 Ein aktueller Gesamtüberblick über die Bedeutung von Vitaminen in Prävention und Therapie findet sich in dem von den Autoren des Beitrages verfassten Buch „Ernährung. Physiologische Grundlagen, Prävention, Therapie“, das in der Wissenschaftlichen Verlagsgesellschaft Stuttgart in Kürze erscheint.






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.