
- DAZ.online
- DAZ / AZ
- DAZ 40/2012
- Linaclotid gegen ...
Arzneimittel und Therapie
Linaclotid gegen Obstipationbei Reizdarmsyndrom
Funktionelle gastrointestinale Störungen zählen zu den häufigsten Beschwerden, die zum Arztbesuch führen. Innerhalb der funktionellen Magen-Darm-Erkrankungen ist das Reizdarmsyndrom (RDS) eine vielfach gestellte Diagnose. Nach epidemiologischen Schätzungen leiden in den europäischen Ländern sechs bis zwölf Prozent der Bevölkerung daran und man nimmt an, dass bei bis zu 70% der Patienten mit Reizdarmsyndrom noch keine Diagnose gestellt worden ist. Die diagnostizierten Fälle gehören zu ungefähr je einem Drittel in die Reizdarmsubgruppen Diarrhö-dominant (RDS-D), Obstipations-dominant (RDS-O) und gemischt beziehungsweise alternierend (RDS-M).
Eingeschränkte Lebensqualität
Die Ursachen sind bislang noch nicht eindeutig geklärt. Man geht davon aus, dass das Reizdarmsyndrom eine multifaktorielle, chronische Erkrankung ist, die durch drei miteinander verknüpfte Mechanismen hervorgerufen wird: psychosoziale Faktoren, Veränderungen von Darmmotilität und -transit sowie eine erhöhte Empfindlichkeit des Darms. Für die Patienten kann das Reizdarmsyndrom zu einer großen Belastung werden. Die Erkrankung macht sich nicht nur durch eine Vielzahl von Symptomen wie beispielsweise Blähungen, Obstipation, Diarrhö oder Schmerzen bemerkbar. Sie kann auch mit verschiedenen Komorbiditäten wie beispielsweise einer Gastritis, psychischen Störungen oder chronischer Müdigkeit einhergehen.
Neue Diagnosekriterien für das Reizdarmsyndrom
Die erste deutsche RDS-Leitlinie aus dem Jahr 2011 [1)] hat sich von den bisher gültigen symptombasierten Diagnosekriterien (Rom-III-Kriterien) abgewandt und das Reizdarmsyndrom neu definiert, wie Prof. Dr. Thomas Frieling, Krefeld, auf einem von Almirall veranstalteten Satellitensymposium am 20. September 2012 bei der 67. Jahrestagung der Deutschen Gesellschaft für Verdauungs- und Stoffwechselerkrankungen (DGVS) in Hamburg hervorhob. Nach den neuen, praxisorientierten Kriterien liegt bei Erwachsenen ein Reizdarmsyndrom vor, wenn:
chronische, das heißt länger als drei Monate anhaltende Darmbeschwerden (z. B. Bauchschmerzen, Blähungen) einzeln oder kombiniert vorliegen, die meist mit Stuhlveränderungen einhergehen,
die Beschwerden die Lebensqualität relevant beeinträchtigen und so stark sind, dass der Patient deswegen Hilfe sucht und
zudem andere Krankheiten symptomabhängig als Ursache für die Beschwerden ausgeschlossen worden sind.
Bisher keine Standardtherapie
Aufgrund der Heterogenität der Erkrankung gibt es weder einen therapeutischen Goldstandard noch allgemeingültige Empfehlungen zu Ernährung und Lebensstil, so Prof. Dr. Martin Storr, München. Die medikamentöse Therapie orientiert sich am Leitsymptom. Bei unzureichendem Therapieerfolg können verschiedene Medikamente sukzessiv kombiniert werden. Es stehen folgende medikamentöse Therapieoptionen zur Verfügung, wobei sich darunter Off-label-Therapien oder bislang nur im Ausland zugelassene Wirkstoffe befinden:
Leitsymptom Blähungen, abdominelle Distension und Flatulenz: Entschäumer, Phytotherapeutika, Probiotika, Rifaximin.
Leitsymptom Schmerzen: Antidepressiva (trizyklische Antidepressiva, SSRI), Phytotherapeutika, Probiotika, Spasmolytika (Mebeverin, Butylscopolamin).
Leitsymptom Diarrhö: Ballaststoffe, Colestyramin (oder Analoga), Loperamid, Probiotika, 5-HT3-Antagonist (Alosetron).
Leitsymptom Obstipation: Antidepressiva (SSRI), Ballaststoffe, 5-HT4-Agonist (Prucaloprid), osmotische Laxanzien, Probiotika, Phytotherapeutika.
Einfluss der ErnährungDer Einfluss der Ernährung auf das Reizdarmsyndrom wird kontrovers diskutiert. Neue Untersuchungen haben gezeigt, dass eine glutenfreie Ernährung in einer Subgruppe effektiv war. Auch hat eine starke Reduktion von Kohlenhydraten bei Diarrhö-RDS zu positiven Ergebnissen geführt. Diese Ergebnisse spiegeln den Eindruck vieler Reizdarmpatienten wider, die von einer Verschlechterung ihres Reizdarmsyndroms bei dem Verzehr von Kohlenhydraten beziehungsweise Gluten berichten. Die neuen Leitlinien empfehlen eine glutenreduzierte Diät ohne Vorliegen einer Zöliakie aber nur dann bei erwachsenen RDS-Patienten, wenn andere Therapieoptionen keine Symptomverbesserung gebracht haben, da der Glutenverzicht eine sehr einschneidende Maßnahme darstellt. |
Neue Therapieansätze
Fortschritte im Verständnis der pathologischen Veränderungen im Darm und im enterischen Nervensystem haben zur Entwicklung neuer, stärker zielgerichteter Medikamente für die Behandlung des Reizdarmsyndroms geführt. So konnte für Rifaximin in klinischen Studien gezeigt werden, dass es bei Reizdarmsyndrom ohne Obstipation die Darmbeschwerden über eine Modulation der Darmflora lindern kann. Rifaximin ist ein lokal wirksames Antibiotikum, das bislang für die Reisediarrhö zugelassen ist, Ein anderer Ansatz greift bei der Modulation der mukosalen Sekretion an. Neben Chloridkanal-Aktivatoren (Lubiproston) macht Linaclotid, ein Guanylatcyclase-C-Rezeptoragonist, auf sich aufmerksam.
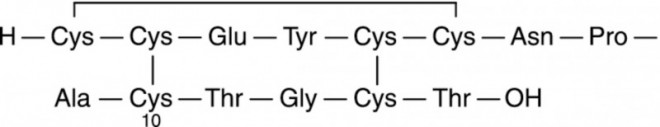
Mit Linaclotid wird ein Multi-Target-Ansatz verfolgt: Zum einen wird über Aktivierung des Cystic Fibrosis Transmembrane Conductance Regulators (CFTR), einem Chloridkanal in der Darmschleimhaut, eine vermehrte Sekretion von Wasser und Chloridionen in das intestinale Lumen erreicht, wodurch das Stuhlvolumen steigt und der Stuhltransit verbessert wird. Zum anderen scheint Linaclotid die Aktivität afferenter Nerven zu modulieren, die an der viszeralen Hypersensitivität beteiligt sind. In Phase-III-Studien [2, 3] führte Linaclotid bei RDS-Patienten mit Obstipation zu einer Verminderung abdomineller Schmerzen, einer Zunahme der Stuhlgänge und insgesamt zu einer Verbesserung der relevanten mit RDS-O- assoziierten Symptome, berichtete Dr. Viola Andresen, Hamburg. In beiden doppelblinden placebokontrollierten Studien hat sich Linaclotid gegenüber Placebo als überlegen erwiesen. Die Verbesserungen hielten während der gesamten Behandlungszeiten (12 und 26 Wochen) an. Linaclotid wird kaum resorbiert, es wirkt nach Einnahme direkt an den lumenseitigen Rezeptoren und zeigt nur eine Wirkung im Darm und keine systemischen Effekte. Die häufigste Nebenwirkung war eine Diarrhö, die meist mild bis moderat war und bei 4,5% der Studienteilnehmer zum Behandlungsabbruch führte. In den USA ist Linaclotid unter der Bezeichnung Linzess® seit August 2012 zugelassen. Dort weist in der Fachinformation ein umrahmter Warnhinweis darauf hin, dass der Wirkstoff nicht bei Patienten unter 18 Jahren eingesetzt werden darf. In Europa hofft der Hersteller nach der ausgesprochenen Zulassungsempfehlung noch in diesem Jahr die Zulassung unter dem Handelsnamen Constella® zu erhalten.
Quellen:
[1] Layer, P.; Andresen, V.; Pehl, C.; et al.: Deutsche Gesellschaft für Verdauungs- und Stoffwechselkrankheiten: S3-Leitlinie Reizdarmsyndrom. Z Gastroenterol (2011) 49(2): 237 – 293.
[2] Rao. S.; et al.: A 12-week, randomized, controlled trial with a 4-week randomized withdrawal period to evaluate the efficacy and safety of linaclotide in irritable bowel syndrome with constipation. Am J Gastroenterol, in press.
[3] Chey, W.D.; et al.: Linaclotide for irritable bowel syndrome with constipation: A 26-week, randomized, placebo-controlled trial to evaluate efficacy and safety. Am J Gastroenterol, in press.
Apothekerin Gode Meyer-Chlond






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.