
- DAZ.online
- DAZ / AZ
- DAZ 1/2022
- With a little help
Pandemie Spezial
With a little help …
Adjuvanzien in Impfstoffen sind für einen erweiterten Schutz notwendig
Eigentlich sind Adjuvanzien jegliche Art von Nebenwirkstoffen in einem Arzneimittel, die die Wirkung des jeweiligen Hauptwirkstoffes unterstützen oder verstärken sollen – gänzlich unabhängig davon, um welches Arzneimittel es sich handelt. So gesehen wird auch Ritonavir als Inhibitor des Enzyms CYP3A4 als „Adjuvans“ eingesetzt, beispielsweise im COVID-19-Medikament Paxlovid®, einer Fixkombination aus dem Protease-Inhibitor Nirmatrelvir und Ritonavir, das den Abbau von Nirmatrelvir über CYP3A4 in der Leber bremst.
Wirklich relevant sind Adjuvanzien jedoch vor allem bei den Impfstoffen. Der Erfolg der Toxoid-Impfung gegen Diphtherie war Anfang des 20. Jahrhunderts zunächst dadurch beeinträchtigt, dass wiederholte Applikationen nötig waren, um einen wirksamen und lang anhaltenden Impfschutz zu erzielen. Das änderte sich erst, als der Immunologe Alexander Glenny das Toxoid an Aluminium-Salze adsorbierte: Nicht nur, dass eine bessere Immunantwort durch die Verwendung der Adsorbatimpfstoffe resultierte, es konnte auch deutlich weniger Antigen eingesetzt werden. Dies verringerte einerseits die Herstellungskosten und verbesserte andererseits auch die Verträglichkeit. Nach wie vor sind in den heute verfügbaren Impfstoffen gegen Diphtherie und Tetanus die Toxoide an Aluminium-Salze adsorbiert.
Ein alternatives Adjuvans entwickelte der ungarische Immunologe Jules Freund in den 1940er-Jahren mit einer Paraffinöl-Emulsion, die zusätzlich auch inaktivierte Mykobakterien enthalten konnte. Dieses sogenannte inkomplette bzw. komplette Freundsche Adjuvans war derart potent, dass es zur Bildung von Abszessen oder Granulomen kommen konnte, weshalb es bereits seit Jahren nicht mehr zur Adjuvantierung von Impfstoffen verwendet wird. Allerdings war die Paraffinöl-Emulsion die Vorlage für moderne Öl-in-Wasser-Emulsionen wie das Adjuvans MF59.
Was ist die Aufgabe eines Adjuvans?
Lange Zeit war die Idee, wie ein Adjuvans – vor allem die Aluminium-Salze – wirken könnte, der Depoteffekt: Das Antigen wird am Injektionsort sukzessive freigesetzt und stimuliert das Immunsystem nachhaltig. Die beobachtete Entzündungsreaktion galt dabei eher als Nebeneffekt. Diese Erklärung greift aber viel zu kurz. Vielmehr ist die Entzündung der Haupteffekt und Zeichen dafür, dass das Adjuvans lokal Zellen des angeborenen Immunsystems stimuliert. Diese Stimulation, die vor allem auf die dendritischen Zellen abzielt, ist die Voraussetzung dafür, dass in der Folge der adaptive, also spezifische Teil des Immunsystems in Form der T- und B-Lymphozyten aktiviert wird. Erst dann kommt es zur Bildung von Antikörpern und zusammen mit den T-Lymphozyten zu einer zielgenauen Bekämpfung des Pathogens. Zusätzlich werden Gedächtniszellen der stimulierten T- und B-Zellen generiert, die bei einem neuen Kontakt mit dem Antigen schnell reaktiviert werden können.
Idealerweise sollte also ein Adjuvans dafür sorgen, dass nicht nur weniger Antigen eingesetzt werden muss, um eine gute Immunantwort zu erhalten, es sollten auch nur wenige Applikationen nötig sein. Dadurch könnte mit einer begrenzten Menge Impfstoff in kurzer Zeit eine größere Bevölkerungsgruppe immunisiert werden. Außerdem könnte es mit einem Adjuvans gelingen, auch bei älteren Personen, deren Immunsystem nicht mehr optimal reagiert, einen ausreichenden Schutz zu erzeugen.
Toll-like-Rezeptoren
Auf der Oberfläche von beispielsweise Makrophagen oder dendritischen Zellen und in der Membran von Endolysosomen befinden sich Rezeptoren, die spezifische pathogenassoziierte Muster (pathogen-associated molecular patterns; PAMP) erkennen und binden. Im Menschen sind zehn verschiedene Toll-like-Rezeptoren (TLR) bekannt, die durch bestimmte Moleküle aktiviert werden. Beispielsweise sitzt TLR4 in der Cytoplasmamembran von dendritischen Zellen und wird von Lipopolysacchariden gramnegativer Bakterien aktiviert. Demgegenüber sind TLR7, TLR8 und TLR9 in der endolysosomalen Membran lokalisiert und erkennen virale oder bakterielle RNA bzw. bakterielle DNA.
Wie funktioniert die Stimulierung des angeborenen Immunsystems?
Um die Wirkung von Impfstoff und Adjuvans zu verstehen und zu optimieren, ist es sinnvoll, sich die Vorgänge bei einer normalen Infektion zu vergegenwärtigen. Pathogene, die in unseren Körper eindringen, bringen immer irgendwelche Merkmale mit, die für unsere Zellen unbekannt sind. Das können beispielsweise Lipopolysaccharide, Lipoteichon-Säuren oder Peptidoglycane aus bakteriellen Zellwänden oder doppelsträngige RNA von Viren sein. Derartige Moleküle sind zwar typisch für bestimmte Pathogengruppen, aber nicht spezifisch für ein bestimmtes Pathogen. Deshalb werden sie als pathogenassoziierte Muster (pathogen-associated molecular patterns, PAMP) bezeichnet. Die in den vordersten Verteidigungslinien unseres Immunsystems aktiven Zellen, wie Makrophagen, dendritische Zellen und neutrophile Granulozyten, besitzen wiederum spezielle Rezeptoren, die Mustererkennungsrezeptoren (pattern recognition receptors, PRR), um diese pathogenassoziierten Muster zu erkennen und zu binden. Der Großteil der Mustererkennungsrezeptoren befindet sich auf der Oberfläche der Immunzellen, beispielsweise in Form der sogenannten Toll-like-Rezeptoren (TLR). Aber auch intrazellulär sind derartige Mustererkennungsrezeptoren anzutreffen. Kommt es zur Interaktion zwischen pathogenassoziierten Mustern und den Mustererkennungsrezeptoren werden intrazelluläre Signalwege aktiviert, die letztlich zu einer Zytokin-Expression und -Ausschüttung führen. Dadurch werden wiederum weitere Immunzellen angelockt, die ebenfalls Zytokine bilden. All das führt zu einer lokalen Entzündung und stimuliert dendritische Zellen zur Phagozytose der Pathogene und zur Präsentation einzelner Antigene. Die präsentierten Antigene sind nun die Aktivierungssignale für spezifische T-Zellen und das Bindeglied zur Mobilisierung des adaptiven Immunsystems.
Die lokale Entzündung und die ins Gewebe eingedrungenen Pathogene führen allerdings zu Stressreaktionen der umgebenden Zellen und teilweise auch zu Gewebeschädigungen. Die dabei zerstörten Zellen setzen körpereigene Moleküle frei, die als Schadens-assoziierte molekulare Muster (damage-associated molecular patterns, DAMP) bezeichnet werden und die ebenfalls von Mustererkennungsrezeptoren erkannt werden und zur Zytokinfreisetzung führen.
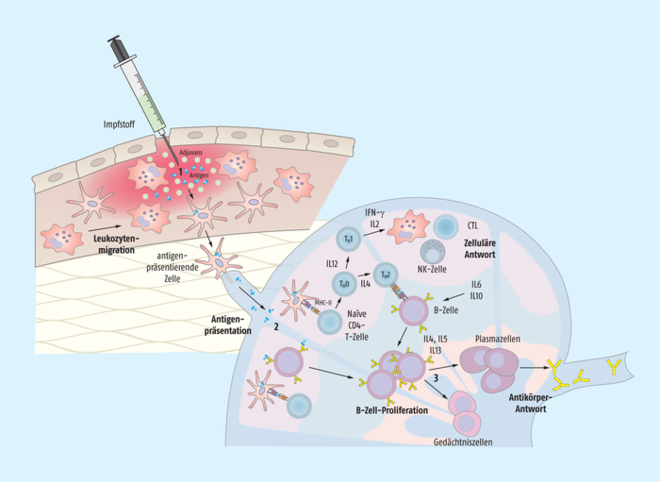
Abb.: Die Wirkung von Adjuvanzien Wird ein Impfantigen (blau) mit einem Adjuvans (hellgrünes Sechseck) verabreicht, kommt es innerhalb von Stunden an der Einstichstelle zu einer lokalen Entzündung, wobei vermehrt Leukozyten einwandern (1). Antigenpräsentierende Zellen wie die dendritischen Zellen nehmen das Antigen auf und präsentieren es im Lymphknoten über MHC-II den T-Helferzellen. Auf diesem Weg werden CD4-positive T-Helferzellen mobilisiert, die ihrerseits dazu beitragen, dass B-Zellen spezifische Antikörper gegen das Antigen bilden. B-Zellen im Lymphknoten können das Antigen direkt über ihren B-Zell-Rezeptor binden (2). Nach einigen Tagen stehen die Antikörper zur Verfügung. Alle aktivierten T- und B-Zellen proliferieren und differenzieren auch zu Gedächtniszellen (3, hier nur am Beispiel der B-Zellen gezeigt). Dadurch stehen später bei einer Infektion schnell Immunzellen zur Eliminierung des Pathogens zur Verfügung. All diese Prozessen werden über verschiedene Zytokine gesteuert. NK-Zelle: natürliche Killerzelle; CTL: zytotoxische T-Lymphozyten; IFN-γ: Interferon gamma; IL: Interleukin
Wo greifen die Adjuvanzien ein?
Anhand der molekularen Mechanismen, die bei einer Infektion zur Aktivierung des angeborenen Immunsystems führen, können die Wirkmechanismen der derzeit verwendeten Adjuvanzien (Tab.) eingeordnet werden.
Adjuvans | Zusammensetzung | Impfstoffbeispiele |
|---|---|---|
Aluminium-hydroxid | – | NeisVac-CTM (Meningokokken), Encepur® (FSME), Havrix® (Hepatitis A) |
Aluminium-phosphat | – | Synflorix® (Pneumokokken), Td-Impfstoff Mérieux®(Diphtherie/Tetanus) |
MF59 | Squalen Sorbitan-Trioleat Polysorbat 80 (O/W-Emulsion) | Fluad® (Influenza, saisonal), Aflunov®(präpandemische Influenza H5N1) |
AS04 | MPL (3-O-Desacyl-4ʼ-monophosphoryl-Lipid A) Aluminiumhydroxid oder Aluminiumphosphat | Cervarix® (humane Papillomviren), Fendrix®(Hepatitis B) |
AS03 | Squalen DL-α-Tocopherol Polysorbat 80 (O/W-Emulsion) | Pandemrix®(Influenza, pandemisch H1N1), Prepandrix®(präpandemische Influenza H5N1) |
AS01 | MPL (3-O-Desacyl-4ʼ-monophosphoryl-Lipid A) Sponinfraktion QS-21 (liposomale Formulierung) | Shingrix®(Varizella Zoster), Mosquirix® (Malaria) |
Aluminium-Salze. „Aluminium“ ist ein regelmäßiger Aufreger. Die Sicherheit von Aluminium-Verbindungen in Impfstoffen wurde letztmals im Jahr 2015 vom Paul-Ehrlich-Institut (PEI) bewertet. Aus den vorliegenden Daten ergibt sich kein Signal für eine Toxizität bei Impfungen. Die Mengen an Aluminium, die durch Impfstoffe in den Körper kommen, sind gering im Vergleich zu den Mengen, die wir über die Nahrung aufnehmen. Wie Aluminium-Salze ihre Wirkung als Adjuvans entfalten, bleibt nach wie vor eher spekulativ. Sicherlich spielt nach wie vor der Depoteffekt eine Rolle, also dass das Antigen allmählich freigesetzt wird. Hinzu kommt eventuell, dass Phagozyten an der Applikationsstelle so lange oder so viel Aluminium-Salz/Antigen-Partikel „fressen“, bis sie zugrunde gehen. Dadurch werden Schadens-assoziierte molekulare Muster freigesetzt, die wiederum das Entzündungsgeschehen induzieren. Außerdem wird diskutiert, dass durch das Adjuvans das sogenannte NLRP3-Inflammasom in Makrophagen und dendritischen Zellen aktiviert wird. Dabei handelt es sich um einen intrazellulären Komplex aus mehreren Proteinen, der eine Schlüsselrolle in der Signalweitergabe von Mustererkennungsrezeptoren zur Expression proinflammatorischer Zytokine spielt. In Mausmodellen ist zu beobachten, dass vor allem Th2-Lymphozyten aktiviert werden und die Bildung von Antikörpern gesteigert wird.
MF59. Seit über 20 Jahren wird dieses Adjuvans auf Öl-in Wasser-Basis angewendet. Die Ölphase besteht aus dem körpereigenen Stoff Squalen, dessen Tröpfchen durch die Emulgatoren Sorbitan-Trioleat und Polysorbat 80 in einem Citratpuffer stabilisiert werden. Der prominenteste Impfstoff mit MF59 ist Fluad® gegen Influenza. Durch diese Adjuvantierung konnte in einer Studie an Kindern im Alter zwischen sechs Monaten und sechs Jahren eine Verbesserung der Wirksamkeit der Influenza-Impfung von 43% auf 89% erreicht werden. Wie das Ganze letztlich funktioniert, ist nach wie vor nicht restlos aufgeklärt. In Mausmodellen konnte gezeigt werden, dass weder Toll-like-Rezeptoren noch das NLRP3-Inflammasom selbst beteiligt sind, allerdings intrazelluläre Adapterproteine dieser Signalwege aktiviert werden. Insgesamt scheint an der Einstichstelle ein immunkompetentes Milieu zu entstehen, wodurch Makrophagen und Muskelzellen dazu gebracht werden, verschiedene Zytokine zu sezernieren, die Immunzellen anlocken. In der Folge werden nicht nur spezifische Antikörper produziert, sondern auch eine Th1- und Th2-Zellantwort induziert. Inwieweit diese im Tiermodell gemachten Beobachtungen auch auf die Vorgänge im Menschen zutreffen, ist allerdings bisher unklar.
Adjuvanssysteme AS0. In den letzten Jahrzehnten wurden bestimmte Adjuvanzien kombiniert, die die Eigenschaften der einzelnen Bestandteile sinnvoll kombinieren sollen.
AS04 ist eine Kombination aus Aluminium-Salz und MPL. MPL (3-O-Desacyl-4‘-monophosphoryl-Lipid A) ist ein abgewandeltes und entgiftetes Lipopolysaccharid (LPS) aus der äußeren Membran des gramnegativen Bakteriums Salmonella enterica Serovar Minnesota Re595. Durch milde Hydrolyse fehlen im MPL verglichen mit dem natürlichen LPS ein Fettsäurerest an C3 und eine Phosphatgruppe an C1. Nach wie vor bindet aber MPL, wie auch LPS, an den Toll-like-Rezeptor 4 (TLR4) und stimuliert deshalb sehr gezielt dendritische Zellen, die wiederum Zytokine sezernieren, die weitere Immunzellen anlocken. Auch spezifische B- und T-Zellen werden dabei mobilisiert. Bei der Entwicklung von Impfstoffen gegen humane Papillomviren bzw. gegen das Hepatitis-B-Virus konnten durch AS04 deutlich mehr Antikörper induziert werden als mit einem ähnlichen Impfstoff, der nur mit Aluminium-Salzen adjuvantiert war. Die Stimulierung über den TLR4 scheint noch nachhaltiger das spezifische Immunsystem zu aktivieren.
ähnelt MF59 und basiert auf einer Öl-in-Wasser-Emulsion mit Squalen als Öl-Grundlage, stabilisiert mit Polysorbat 80. Zusätzlich ist α-Tocopherol (Vitamin E) enthalten, das einen besonderen Effekt auf das Immunsystem ausübt und eine deutliche Verbesserung im Vergleich zu MF59 bringt. In Mausmodellen modulierte α-Tocopherol die Expression bestimmter Chemokine und Zytokine, verbesserte die Antigenaufnahme in Monozyten und erhöhte die Rekrutierung von Granulozyten in die Lymphknoten. Dadurch wurde eine breite und lang anhaltende Antikörper- und CD4+-T-Zellantwort induziert.
AS03 unter Kritik
Als 2009 nach der Anwendung des Influenza-Impfstoffs Pandemrix® vermehrt Fälle einer Narkolepsie aufgetreten waren, stand das darin enthaltene Adjuvanssystem AS03 im Verdacht, dafür verantwortlich zu sein. Nach Angaben des Paul-Ehrlich-Instituts kam es durch Pandemrix® bei Erwachsenen zu 0,6 bis 1 und bei Kindern zu 2 bis 6 zusätzlichen Fällen einer Narkolepsie pro 100.000 verimpften Dosen. Zum Vergleich: Die natürliche Narkolepsie-Inzidenz liegt bei Erwachsenen bei etwa 0,7 und bei Kindern circa 0,1 pro 100.000 Personen pro Jahr. Fast alle Narkolepsie-Patienten haben eine besondere Form der MHC-II-Moleküle (MHC: major histocompatibility complex, Haupthistokompatibilitätskomplex), den sogenannten HLA-DQB1*06:02-Haplotyp. MHC-II-Moleküle präsentieren kurze Peptidsequenzen phagozytierter Pathogene bzw. von Impfantigenen. Verschiedene Theorien existieren über den Pathomechanismus der impfinduzierten Narkolepsie, von denen allerdings jede ihre Schwachpunkte hat. Ein wesentlicher Bestandteil sind jedoch immer Hypocretine, bestimmte Neuropeptide, die den Schlafrhythmus beeinflussen und deren Mangel mit einer Narkolepsie assoziiert ist.
Pandemrix® enthielt neben den üblichen Impfantigenen Hämagglutinin und Neuraminidase einen im Vergleich zu anderen Influenza-Impfstoffen deutlich höheren Anteil an Nucleoprotein A. In den Personen, die nach der Impfung eine Narkolepsie entwickelten, fanden sich Antikörper, die sowohl dieses Nucleoprotein binden als auch den Hypocretin-Rezeptor 2. Eine kurze Peptidsequenz kommt nämlich annähernd identisch in beiden Proteinen vor und war offensichtlich das Antigen, gegen das Antikörper gebildet wurden. Eine ähnliche molekulare Mimikry konnte zwischen einer Peptidsequenz im Hämagglutinin des Pandemie-Influenzavirus und dem Hypocretin festgestellt werden und wird ebenfalls als Ursache für die aufgetretenen Narkolepsiefälle gehandelt. An dieser Stelle könnte wieder der oben genannte HLA-Haplotyp relevant sein, der diese Peptidsequenzen bevorzugt präsentiert haben könnte.
Nach einer anderen Theorie induziert der AS03-Bestandteil α-Tocopherol (Vitamin E) – zumindest in vitro in menschlichen neuronalen Zellen – die Expression eines Transkriptionsfaktors, der dann wiederum die Bildung von Hypocretin und einer Untereinheit des Proteasoms fördert. Werden Hypocretin-Bruchstücke über MHC-I-Moleküle präsentiert, können zytotoxische T-Zellen mobilisiert werden, die diese neuronalen Zellen zerstören.
Ganz aufgeklärt ist das Problem immer noch nicht und die möglichen Pathomechanismen werden unter den Wissenschaftlern intensiv diskutiert.
Literatur
Aktuelle Informationen zu Narkolepsie im zeitlichen Zusammenhang mit A/H1N1-Influenzaimpfung. Informationen des Paul-Ehrlich-Instituts (PEI), aktualisiert: 28. November 2016, www.pei.de
Sohail Ahmed , Steinman L. Narcolepsy and influenza vaccination-induced autoimmunity. Ann Transl Med 2017;5:25, doi: 10.21037/atm.2016.12.63.
AS01 besteht aus MPL in Kombination mit der gereinigten Saponinfraktion QS-21 aus Extrakten der Borke des Seifenrindenbaumes Quillaja saponaria Molina. Die entscheidende Substanz ist ein stark hämolytisch wirkendes Saponin, das aus dem Triterpen Quillajasäure besteht, an das in Position C3 ein verzweigtes Trisaccharid und an Position C28 über eine Esterbindung ein lineares Tetrasaccharid gebunden ist. QS-21 liegt in AS01 an Cholesterol gebunden in Liposomen vor. Diese Bindung ist wichtig, um die hämolytische Aktivität und damit die Reaktogenität zu reduzieren. Wie genau das amphiphile Molekül QS-21 wirkt, ist nicht bekannt, allerdings verstärkt das Saponin die Antigenpräsentation und induziert im angeborenen Immunsystem die Freisetzung von IFN-γ und anderen Zytokinen, die zu einer Th1-lastigen, zellulären Immunreaktion führen. Im Mausmodell hat sich gezeigt, dass die Kombination aus MPL und QS-21 einen synergistischen Effekt hat, also stärker ist als die Summe der Einzelstoff-Wirkungen.
Ausblick
Adjuvanzien und ihre Wirkung auf das Immunsystem sind ein sehr spannendes Forschungsgebiet, das im Pandemiefall natürlich besondere Aufmerksamkeit erfährt. In den letzten Jahren versteht man immer besser, wie Adjuvanzien funktionieren und welche zellulären und molekularen Mechanismen sie bedienen. Für die zukünftige Impfstoffentwicklung wird es immer wichtiger werden, für ein Impfantigen das genau passende Adjuvans(-System) zu finden, um gezielt eine bestimmte Antwort des spezifischen Immunsystems hervorzurufen: Die Beobachtung, dass beispielsweise Antikörper gegen SARS-CoV-2 relativ schnell wieder aus der Zirkulation verschwinden, lässt Adjuvanzien interessant werden, die spezifische, follikuläre T-Helferzellen und langlebige Plasmazellen induzieren. Ein Adjuvans, das in Tiermodellen genau das gezeigt hat, ist Telratolimod (MEDI9197, 3M-052), ein synthetischer TLR-7/8-Agonist. Allerdings sind die immunologischen Ergebnisse zu Adjuvanzien aus Tiermodellen nur bedingt auf den Menschen übertragbar. Eine gerade erschienene Arbeit, an der das PEI und das Friedrich-Loeffler-Institut federführend beteiligt waren, hat sich mit dieser Problematik beschäftigt und humane In-vitro-Modelle zur Testung von Adjuvanzien etabliert. Mit diesen Modellen wird versucht, ein tieferes Verständnis für die Art der Immunantwort zu entwickeln, die verschiedene Adjuvanzien hervorrufen. Damit kommt man dem Ziel, das optimale Antigen-Adjuvanssystem für den nächsten Impfstoff zu finden, einen Schritt näher. |
Literatur
Pulendran B et al. Emerging concepts in the science of vaccine adjuvants. Nat Rev Drug Discov 2021:454-475
Reed SG et al. Key roles of adjuvants in modern vaccines. Nat Med 2013;19:597-608
Roßmann L et al. Distinct single-component adjuvants steer human DC-mediated T-cell polarization via Toll-like receptor signaling toward a potent antiviral immune response. Proc Natl Acad Sci USA 2021;118:e2103651118
Wang Y-Q et al. MPL Adjuvant Contains Competitive Antagonists of Human TLR4. Front Immunol 2020;11:577823
Winckler T. Wirkmechanismen von Adjuvanzien in Impfstoffen. Pharmakon 2020;8:312-320

























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.