
- DAZ.online
- News
- Tacpan wieder komplett ...
Mangelhafte Zulassungsstudien aus Indien
Tacpan wieder komplett verkehrsfähig – Kritik an BfArM
Jetzt hat Panacea Biotec Germany für Tacpan 5 mg Rechtsmittel eingelegt, so dass der Vollzug des Zulassungsruhens für diese Dosierung ausgesetzt ist. Mit Veröffentlichung der entsprechend aktualisierten BfArM-Liste vom 18. Dezember 2014, Stand 15:00 Uhr, darf Tacpan jetzt wieder in allen Dosierungsstärken abgegeben werden.
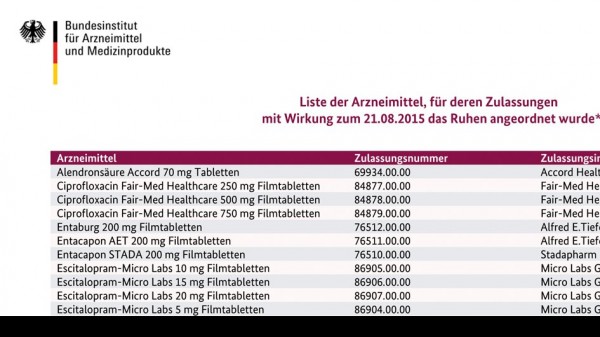
Seit dem 9. Dezember 2014 sind auf der Webseite des BfArM Arzneimittel gelistet, deren Zulassung aufgrund mangelhafter Studien der indischen Firma GVK Biosciences ruht. Da die Hersteller jedoch neue Unterlagen, Widerspruch und Rechtsmittel mit aufschiebender Wirkung gegen die entsprechenden BfArM-Bescheide einlegen können, ändert sich die Liste täglich.
Auf Seiten der Apotheker ist der Unmut groß. Kritisiert wird die unprofessionelle Informationsaufarbeitung durch das BfArM. Vermisst wird unter anderem eine chronologische Liste der Änderungen. Täglich müssen alle Apotheken auf der Internetseite des BfArM prüfen und irgendwie dokumentieren, wann ein Arzneimittel vom Ruhen der Zulassung betroffen war und damit nicht abgegeben werden durfte und zu welchem Zeitpunkt das Ruhen der Zulassung aufgehoben oder außer Vollzug gesetzt wurde. Dabei kann nur vermutet werden, dass ein ganz von der Liste verschwundenes Arzneimittel vollumfänglich rehabilitiert ist (Tacpan 0,5 und 1 mg), ein mit rotem Kasten und Hinweis auf eingelegte Rechtsmittel auf der Liste verbliebenes Arzneimittel jedoch nicht (Tacpan 5 mg). Da mit einer Aktualisierung der Liste die alte Liste vollständig verschwindet, kann nur derjenige den chronologischen Verlauf nachvollziehen, der jede Liste abgespeichert oder ausgedruckt hat.
Hier kommen Sie zur BfArM-Webseite mit dem Link zur jeweils aktuellen Liste.
























Stuttgart - 18.12.2014, 17:25 Uhr