
- DAZ.online
- News
- Pharmazie
- Sacubitril / Valsartan: ...
Nach der Zulassung in den USA
Sacubitril / Valsartan: Herzinsuffizienz-Wunderwaffe bald auch in Europa
Stuttgart - 25.09.2015, 17:15 Uhr

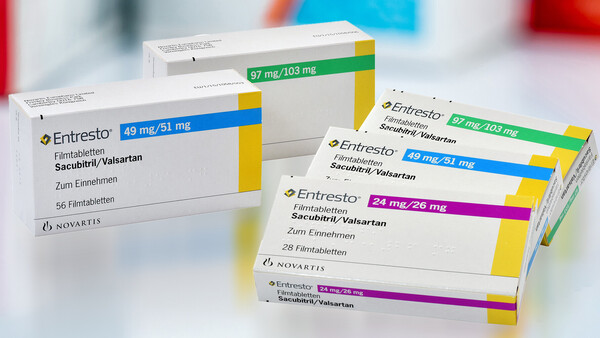
Daumen hoch für Entresto®: der CHMP empfiehlt die Zulassung. (Bild: xurzon - Fotolia.com)
In den USA ist die fixe Kombination aus dem AT1-Rezeptorblocker Valsartan und dem Neprilysin-Inhibitor Sacubitril (Entresto®) bereits seit Juli zugelassen. Jetzt wollen die Europäer nachziehen. Der Humanarzneimittelausschuss der EMA (CHMP) hat empfohlen, das Präparat auch in Europa zuzulassen. Es ist der erste Vertreter einer neuen Wirkstoffklasse, der Angiotensin-Rezeptor-Neprilysin-Inhibitoren (ARNI).
Indiziert ist Entresto® bei Erwachsenen, die unter symptomatischer chronischer Herzinsuffizienz mit reduzierter Auswurffraktion leiden. Das Wirkprinzip der Substanz, die auch als LCz696 bekannt ist, basiert zum einen auf der bei Herzinsuffizienz seit Langem als Therapieprinzip etablierten Blockade des Renin-Angiotensin-Aldosteron-Systems durch Valsartan und zum anderen auf der zusätzlichen Inhibition von Neprilysin, einem Enzym, das für den Abbau von natriuretischen Peptiden (ANP und BNP) verantwortlich ist. Hersteller Novartis plant drei Wirkstärken der Kombination Sacubitril/Valsartan auf den Markt zu bringen: 24 mg Sacubitril /26 mg Valsartan, 49 mg/51 mg und 97 mg/103 mg.
Eine Studie zum klinischen Nutzen der Pharmakotherapie bei systolischer Herzinsuffizienz – die größte, die es bislang gab – war vorzeitig gestoppt worden, da sich Entresto® bei einer Zwischenanalyse dem bisherigen Goldstandard Enalapril klar überlegen gezeigt hatte. Sowohl in Europa als auch in den USA waren die Zulassungsunterlagen in einem beschleunigten Verfahren geprüft worden. Die endgültige Entscheidung über die Zulassung obliegt nun der europäischen Kommission.
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.