
- DAZ.online
- News
- Politik
- Das sind Spahns Pläne f...
Valsartan, Lunapharm, Bottrop
Das sind Spahns Pläne für den Arzneimittelmarkt
Berlin - 16.11.2018, 13:30 Uhr

Bundesgesundheitsminister Jens Spahn (CDU) hat mit dem Entwurf zum „Gesetz für mehr Sicherheit in der Arzneimittelversorgung“ (GSAV) das erste Gesetz im Arzneimittelbereich vorgelegt und will damit insbesondere auf die Arzneimittelskandale im Sommer dieses Jahres reagieren. (m / Foto: imago)
Am heutigen Freitag schickt das Bundesgesundheitsministerium den ersten Gesetzentwurf im Arzneimittel- und Apothekenbereich dieser Legislaturperiode an die anderen Ressorts zur Abstimmung. Mit dem „Gesetz für mehr Sicherheit in der Arzneimittelversorgung“ (GSAV) will das BMG unter anderem das Zyto-Honorar reformieren und die Importförderklausel ändern. Als Reaktion auf die Arzneimittelskandale rund um den Brandenburger Händler Lunapharm und die Valsartan-Verunreinigungen plant das BMG aber noch weitere Umstellungen. DAZ.online bietet eine Übersicht.
Mit dem „Gesetz für mehr Sicherheit in der Arzneimittelversorgung“ (GSAV) legt Bundesgesundheitsminister Jens Spahn (CDU) sein erstes Gesetz für den Arzneimittelmarkt vor. In erster Linie geht es im GSAV darum, auf die Arzneimittelskandale des Sommers zu reagieren. Zur Erinnerung: Der Brandenburger Händler Lunapharm wird beschuldigt, jahrelang auf illegalem Wege Zytostatika nach Deutschland importiert zu haben. Ebenfalls im Sommer dieses Jahres wurde bekannt, dass in in China hergestelltem Valsartan das Nitrosamin NDMA festgestellt wurde. Außerdem beschäftigt das BMG auch nach wie vor der Fall des Bottroper Zyto-Apothekers Peter S.
Neuregelungen sollen im Juli 2019 in Kraft treten
Nach den Plänen des Ministeriums soll das GSAV im Juli 2019 in Kraft treten. Dadurch dass die Länder – etwa im Bereich der Arzneimittelüberwachung – unmittelbar betroffen sind, wird der Bundesrat dem Vorhaben zustimmen müssen. Aus der Lunapharm-Affäre will das BMG die folgenden Konsequenzen ziehen:
- Das Bundesinstitut für Arzneimittel und Medizinprodukte und das Paul-Ehrlich-Institut sollen bei der Arzneimittelüberwachung künftig eine größere „Koordinierungsfunktion“ erhalten, hieß es aus dem BMG. Beide Institutionen sollen künftig etwaige Rückruf-Aktionen auf Ebene der Bundesländer koordinieren. Zur Erklärung: Die von der Brandenburger Landesregierung eingesetzte Taskforce hatte kritisiert, dass die Arzneimittelüberwachung im Land schlecht organisiert sowie fehl- und unterbesetzt sei.
- Das BMG will auch die Zusammenarbeit der Behörden auf Bundes- und Landesebene verbessern. Und zwar soll es künftig eine Informationspflicht für Rückrufe geben, die zu einem Lieferengpass führen könnten.
- Die Landesbehörden sollen in ihrer Überwachungsbefugnis gleichzeitig gestärkt werden, indem es ihnen erlaubt werden soll, Unterlagen über Wirkstoffe oder andere Stoffe bei den Herstellern einzusehen.
- Außerdem sollen die EU-Vorgaben zur Kennzeichnung von Arzneimitteln mit Sicherheitsmerkmalen angepasst werden. Den Herstellern drohen Sanktionen bei Verstößen gegen die Anforderungen der EU-Verordnung. Die Kennzeichnung soll zudem vereinfacht werden.
- In der Arzneimittelüberwachung soll es in Zukunft auch sogenannte „Interessenkonflikterklärungen“ geben. Gibt es einen solchen Interessenkonflikt zwischen einem Inspektor eines Herstellers und einem Behördenmitarbeiter, soll dieser veröffentlicht werden.
Hersteller sollen Kassen bei Rückrufen Regress zahlen
So will das BMG auf den Fall Valsartan reagieren:
- Die Kassen sollen einen Anspruch auf Regress gegenüber dem pharmazeutischen Unternehmen erhalten, wenn es Produktmängel gibt, die beispielsweise zu einem Rückruf führen. Das BMG will damit ein wirtschaftliches Interesse für die Hersteller schaffen, dass Arzneimittel sicher und sauber sind.
- Die Länder sollen die Bundesbehörden über geplante Inspektionen bei Herstellern von Arzneimitteln und Wirkstoffen in Drittstaaten informieren. Die Bundesbehörden sollen an diesen Inspektionen teilnehmen dürfen.
- Informationen über den Wirkstoffhersteller von Fertigarzneimitteln sollen öffentlich einsehbar sein.
- Kommt es zu einem qualitätsbedingten Rückruf, fällt die Pflicht des Versicherten auf Zuzahlung weg.
- In Rabattverträge soll die Klausel aufgenommen werden, dass eine „unterbrechungsfreie und bedarfsgerechte“ Lieferfähigkeit zu berücksichtigen ist. Die Kassen sollen so in „Mitverantwortung“ genommen werden, um Lieferengpässe zu vermeiden.
Mehr zum Thema
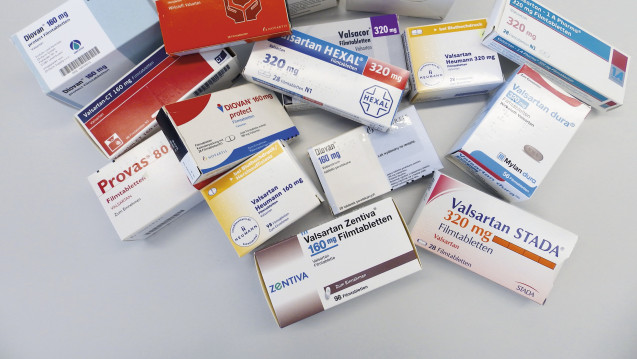
Nitrosamin-Krise
Valsartan-Rückrufe

Illegaler Arzneimittelhandel
Lunapharm-Affäre

Unterdosierte Zytostatika
Bottroper Zyto-Skandal
So reagiert das BMG auf den Fall Bottrop:
- Wie schon von DAZ.online beschrieben, soll die Honorierung der Zyto-Apotheker und das Preisbildungssystem im Zyto-Bereich komplett reformiert werden.
- Ebenso soll es häufiger zu unangemeldeten
Kontrollen in Apotheken kommen. Im Bundesgesetz sollen diese unangemeldeten
Kontrollen als verpflichtend festgeschrieben werden. Die Frequenz der
Kontrollen soll aber weiterhin durch die Landesbehörden geregelt werden. In Nordrhein-Westfalen hatte CDU-Gesundheitsminister Karl-Josef Laumann zuletzt ein gesamtes Paket zur Neuordnung der Apotheken-Kontrollen vorgestellt. Auch Apotheken, die keine Zytostatika herstellen, sollen in NRW künftig häufiger kontrolliert werden.
Pharmadialog startet gleichzeitig
Das Gesetz enthält aber noch einige weitere wichtige Regelungen
für den Arzneimittelmarkt. Dazu gehören unter anderem:
- Als Reaktion auf den Fall „Brüggen Bracht“, der seinen Patienten 3-Brompyruvat verabreichte – womöglich mit tödlichen Folgen – will das BMG die Herstellung von Rx-Arzneimitteln durch Angehörige nicht-ärztlicher Heilberufe (insbesondere Heilpraktiker) erlaubnispflichtig machen.
- Wie schon zuvor beschrieben, soll es für Biosimilars in der Apotheke eine Austauschbarkeit geben. Der Gemeinsame Bundesausschuss soll eine Richtlinie erarbeiten, in der festgelegt wird, wann welche Originale gegen welches Biosimilar ausgetauscht werden können. Der CDU-Arzneimittelexperte Michael Hennrich hatte diese Regelung bereits kritisiert und gesagt, dass die Austauschbarkeit in der Apotheke aus seiner Sicht erst in ein paar Jahren ausprobiert werden solle.
- Die Herstellung von Frischzellen zur Anwendung am Menschen soll verboten werden. In einem zweiten Schritt soll es noch eine Verordnung dazu geben.
- Sieben Monate nach Inkrafttreten des Gesetzes soll die Selbstverwaltung einen Plan dafür vorlegen, wie das E-Rezept in den Markt gebracht werden kann. Dann sollen auch die Regelungen fallen, die es bislang verhindern, dass eine Verordnung zwingend auf einem Papierrezept erfolgen muss. DAZ.online hatte über diese Pläne des BMG bereits berichtet.
- Das Fernverordnungsverbot soll ebenfalls fallen. 2016 hatte der Gesetzgeber es verboten, dass Apotheker Rezepte beliefern, die aus einem nicht-direkten Arzt-Patienten-Kontakt resultieren. Dieses Verbot soll nun wieder aufgehoben werden, damit Ärzte in Online-Sprechstunden Arzneimittel verordnen können.
- Nach einmal erfolgter Genehmigung einer Versorgung mit Medizinalhanf sollen Patienten bei weiteren Verordnungen keine neue Genehmigung beantragen müssen, wenn die Dosierung oder die Blütensorte nicht gewechselt werden. Im ambulanten Bereich müssen Patienten auch keine Anträge mehr stellen, wenn sie zuvor mit Medizinalhanf bereits stationär versorgt wurden.
- Die Hersteller können auf ihren Packungen die Angabe „verwendbar bis“ künftig mit „verw. bis“ abkürzen.
- Bei der Abgabe von Cannabis oder Cannabiszubereitungen in der Apotheke will das BMG eine Verhandlungslösung einführen. Wie bereits berichtet, sollen die bisherigen Preisbildungsmechanismen in der Arzneimittelpreisverordnung gestrichen werden. Dafür sollen Kassen und Apotheker neue Arbeitspreise aushandeln. Damit sollen pro Jahr 25 Millionen Euro eingespart werden, so die Hoffnung des Ministeriums.
- Bei Arzneimitteln für Patienten mit Hämophilie galt bislang eine Ausnahme vom Apothekenvertriebsweg – die Hersteller verkauften direkt an Ärzte und Krankenhäuser. Diese Ausnahme soll zurückgenommen werden: Nicht aus Blut gewonnene Faktor-Präparate sollen mit anderen Biologika-Arzneimitteln gleichgesetzt werden. Das BMG will somit die flächendeckende Versorgung über den regulären Apothekenvertriebsweg (über Großhandel und Apotheke) stärken.
- Bei Importarzneimitteln soll die in der Importförderklausel festgehaltene Preisabstandsgrenze von 15 Euro, damit ein Arzneimittel auf die Importquote anrechenbar ist, fallen. Der 15-Prozent-Abstand zum inländischen Original zur Anrechnung auf die Quote soll aber bleiben.
Dass Spahn sein Vorhaben unverändert durch den Bundestag und Bundesrat bekommt, ist unwahrscheinlich. Denn am heutigen Freitag ist der neue Pharmadialog gestartet, bei dem sich die Bundesregierung mit Vertretern der Pharmaindustrie austauscht. Sehr viele Punkte, die das BMG mit dem GSAV regeln will, dürften auch dort angesprochen werden.






















4 Kommentare
Hoffentlich falsch abgetippt?
von David Becker am 19.11.2018 um 8:10 Uhr
» Auf diesen Kommentar antworten | 1 Antwort
AW: Re: Hoffentlich falsch abgetippt
von Benjamin Rohrer am 19.11.2018 um 8:50 Uhr
Valsartan
von Schall am 16.11.2018 um 19:42 Uhr
» Auf diesen Kommentar antworten | 1 Antwort
AW: Valsartan
von Dr. Arnulf Diesel am 17.11.2018 um 12:19 Uhr
Das Kommentieren ist aktuell nicht möglich.