
- DAZ.online
- News
- Pharmazie
- Widersprüchliches zu ...
Beschleunigte Zulassung bei der FDA?
Widersprüchliches zu Remdesivir – hilft es bei COVID-19?
Stuttgart - 30.04.2020, 16:30 Uhr
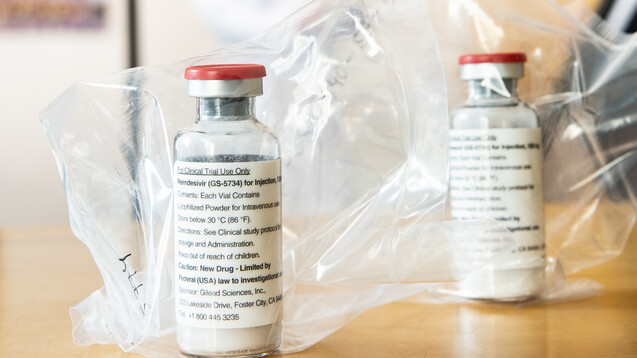
Die Studiendaten zu Remdesivir bei COVID-19 sind widersprüchlich. (m / Foto: picture alliance/Ulrich Perrey/dpa-POOL/dpa)
Fünf Tage Remdesivir genügt
Zusätzlich zu den NIAID-Zwischenanalysen der ACTT legte Gilead am 29. April 2020 Phase-3-Daten (SIMPLE-Studie) zur Behandlungsdauer mit Remdesivir von Patienten mit schwerer COVID-19-Erkrankung vor. Die Frage nach der Behandlungsdauer sei wichtig, da die Möglichkeit eines kürzeren Behandlungsverlaufs in vielerlei Hinsicht vorteilhaft sei, so Gilead-CEO Daniel O’Day in einem Offenen Brief. Die Patienten könnten früher aus dem Krankenhaus entlassen werden und Familien wieder zusammengeführt. Gesundheitsressourcen würden freigesetzt, und es stünden mehr Arzneimittel für andere bedürftige Patienten zur Verfügung, so der CEO. All dies werde in einer Zeit der Pandemie besonders wichtig.
Früher Behandlungsbeginn von Vorteil
SIMPLE zeigt bislang, dass die klinischen Verbesserungen unter Remdesivir ähnlich sind, unabhängig, ob die Patienten Remdesivir fünf oder zehn Tage erhielten.
„Aus den beiden heute vorliegenden Ergebnissen – den NIAID- und den SIMPLE-Daten – wissen wir jetzt zwei Dinge: dass Remdesivir die Zeit bis zur Genesung zu verkürzen scheint, und dass bei der Behandlung von Patienten mit schwerer Erkrankung eine fünftägige Behandlung potenziell genauso wirksam ist wie eine Behandlung über zehn Tage“, so das Fazit des CEO.
Mehr zum Thema

Remdesivir bei Covid-19
Arzneimittel gegen das Coronavirus SARS-CoV-2: Studien starten
Im Einzelfall bereits im Einsatz
Remdesivir: Zwei Studien in Deutschland starten
Auch gibt es Hinweise, dass ein früher Behandlungsbeginn mit dem Virostatikum vorteilhaft ist. COVID-19-Patienten, die Remdesivir kurz nach dem Auftreten von Symptomen erhielten, schnitten besser ab als diejenigen, die es später erhielten.





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.