
- DAZ.online
- News
- Remdesivir auch in der EU...
CHMP der EMA
Remdesivir auch in der EU zur Zulassung empfohlen
Stuttgart - 25.06.2020, 17:00 Uhr
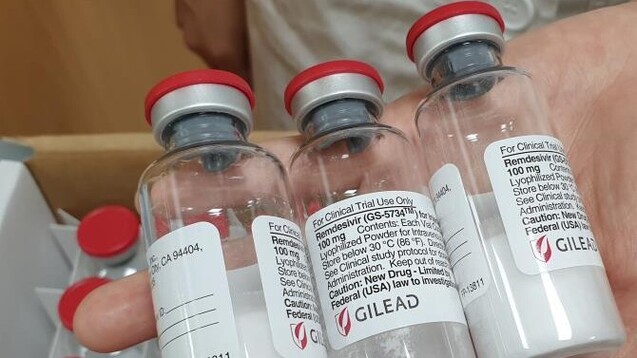
Die Europäische Arzneimittel-Agentur EMA empfiehlt die bedingte Zulassung von Remdesivir, dem ersten COVID-19-Arzneimittel, für die EU. (Foto: picture alliance / YONHAPNEWS AGENCY | Yonhap)
Schwer an COVID-19 Erkrankte mit zusätzlichem Sauerstoff
Basis für die bedingte Zulassungsempfehlung bilden Daten aus der vom US National Institute of Allergy and Infectious Diseases (NIAID) gesponserten Studie NIAID-ACTT-1 (Adaptive COVID-19 Treatment Trial, ACTT-1). Vorläufige Ergebnisse der multizentrischen, doppelblinden, randomisierten kontrollierten Phase-III-Studie bei über 1.000 hospitalisierten COVID-19 Patienten wurden unter „Remdesivir for the Treatment of Covid-19 – Preliminary Report“ am 22. Mai im NEJM veröffentlicht. Patienten, die Remdesivir erhielten, hatten eine um 31 Prozent schnellere Genesungszeit als Patienten, die Placebo erhielten. Unter Remdesivir waren die Erkrankten im Median nach elf Tagen genesen, mit Placebo dauerte die Genesung 15 Tage. Dieser Effekt wurde bei Patienten mit leichter bis mittelschwerer Erkrankung nicht beobachtet: Die Zeit bis zur Genesung betrug sowohl in der Remdsivir- als auch in der Placebogruppe fünf Tage. Bei Patienten mit schwerer Erkrankung, die etwa 90 Prozent der Studienpopulation ausmachten, betrug die Zeit bis zur Genesung zwölf Tage in der Remdesivir-Gruppe und 18 Tage in der Placebo-Gruppe.
Mehr zum Thema
Arzneimittel bei COVID-19
Wo stehen wir bei Remdesivir?
Beschleunigte Zulassung bei der FDA?
Widersprüchliches zu Remdesivir – hilft es bei COVID-19?
Als genesen galt, wer innerhalb von 28 Tagen nach Studieneinschluss nicht mehr im Krankenhaus war und keine Einschränkung der Aktivität zeigte oder nicht mehr hospitalisiert war, aber eine Einschränkung der Aktivität und/oder Sauerstoffbedarf hatte oder zwar noch hospitalisiert war, jedoch ohne Sauerstoffbedarf.
Nicht jeder Coronapatient profitiert
Am meisten scheint der Studie zufolge Remdesivir Patienten zu nutzen, die Sauerstoff benötigten, während mechanisch beatmete Patienten oder solche mit extrakorporaler Membranoxygenierung (ECMO) weniger profitierten. Das sieht auch die EMA so: Bei Patienten, die mit Remdesivir begannen, als sie bereits eine mechanische Beatmung oder ECMO erhielten, wurde kein Unterschied in der Zeit bis zur Genesung festgestellt. Daten über den Anteil der Patienten, die bis zu 28 Tage nach Behandlungsbeginn verstarben, werden laut CHMP derzeit für die abschließende Analyse gesammelt.
Insgesamt kommt das CHMP zu dem Schluss, dass sich die Bilanz von Nutzen und Risiken bei Patienten mit Lungenentzündung, die zusätzlichen Sauerstoff benötigen, also Patienten mit schwerer Erkrankung, als positiv erwiesen hat.





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.