
- DAZ.online
- News
- Pharmazie
- Erstes langwirksames, ...
EMA-Zulassungsempfehlung
Erstes langwirksames, parenterales HIV-Therapieregime
Köln - 23.10.2020, 13:45 Uhr
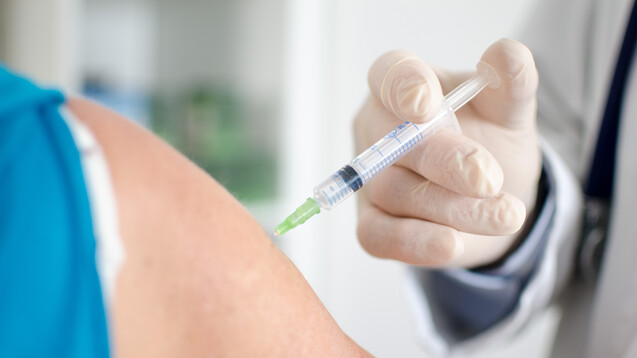
Die Kombination von Rilpivirin und Cabotegravir soll für HIV-Patienten zugelassen werden, bei denen die Viruslast unter der Nachweisgrenze (< 50 Kopien/ml) liegt und bei denen keine Resistenz gegen NNRTI und INSTI vorliegt. (Foto: thodonal / stock.adobe.com)
Daten dreier unverblindeter Phase-III-Studien
Die Kombination von Rilpivirin und Cabotegravir soll für HIV-Patienten zugelassen werden, bei denen die Viruslast unter der Nachweisgrenze (< 50 Kopien/ml) liegt und bei denen keine Resistenz gegen NNRTI und INSTI vorliegt. Zu den häufigsten Nebenwirkungen zählten neben Reaktionen an der Injektionsstelle vor allem Kopfschmerzen, Fieber, Übelkeit, Asthenie, Myalgie, Müdigkeit und Schwindel.
Mehr zum Thema

Antiretrovirale Behandlung
Erste duale HIV-Therapie erhält EU-Zulassungsempfehlung

Ein neuer Durchbruch in der AIDS-Therapie?
Die Spritze gegen HIV
Die Entscheidung des Humanarzneimittelausschusses der EMA (CHMP) basiert auf den Daten dreier randomisierter, unverblindeter, multizentrischer Phase-III-Studien, bei denen die Sicherheit und Wirksamkeit einer Kombinationstherapie aus Cabotegravir und Rilpivirin bei über 18-jährigen ART-naiven oder erfolgreich therapierten Patienten untersucht wurde. Dabei wurden beide Wirkstoffe alle vier oder acht Wochen verabreicht. Die positive Beurteilung durch den CHMP ist ein Zwischenschritt, bevor die Zulassung für Vocabria® und Rekambys® durch die Europäische Kommission erteilt werden kann.


























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.