
- DAZ.online
- News
- Pharmazie
- Erstes langwirksames, ...
EMA-Zulassungsempfehlung
Erstes langwirksames, parenterales HIV-Therapieregime
Köln - 23.10.2020, 13:45 Uhr
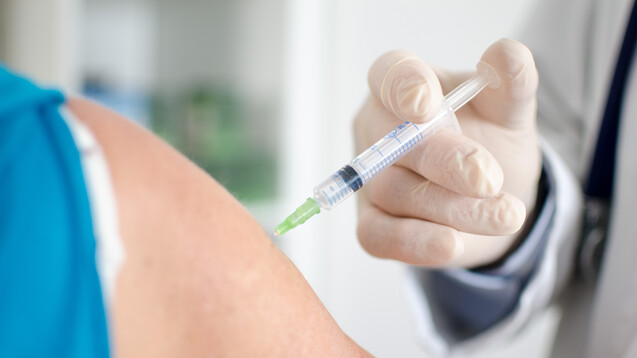
Die Kombination von Rilpivirin und Cabotegravir soll für HIV-Patienten zugelassen werden, bei denen die Viruslast unter der Nachweisgrenze (< 50 Kopien/ml) liegt und bei denen keine Resistenz gegen NNRTI und INSTI vorliegt. (Foto: thodonal / stock.adobe.com)
Die EMA hat eine Zulassungsempfehlung für Rekambys (Rilpivirin) und Vocabria (Cabotegravir) ausgesprochen. Die zwei antiretroviralen Arzneimittel werden zusammen zur Behandlung einer HIV-1-Infektion bei Erwachsenen angewendet. Sie stellen die erste langwirksame, parenteral applizierbare Form der antiretroviralen Therapie (ART) dar. Sie sollen monatlich oder alle zwei Monate intramuskulär appliziert werden.
Bei Rekambys® (von Janssen-Cilag) handelt es sich um eine neue langwirksame Formulierung des altbewährten nichtnukleosidischen Reversetranskriptaseinhibitors (NNRTI) Rilpivirin, welcher seit 2011 als Edurant® beziehungsweise später als Teil der Kombipräparate Eviplera®, Odefesey® und Juluca® vertrieben wird. Cabotegravir in Vocabria® (von ViiV Healthcare) hingegen ist zwar ein neuer Vertreter aus der Gruppe der Integrase-Strangtransfer-Inhibitoren (INSTI), allerdings unterscheidet sich die chemische Struktur nur kaum zu Dolutegravir, welches seit 2014 als Tivicay® die Marktzulassung erhalten hat und neben diversen Kombinationspräparaten den Ansatz der dualen Therapie ermöglicht hat.
Die zwei antiretroviralen Arzneimittel – Rilpivirin und Cabotegravir – sollen nun auf Empfehlung der EMA zusammen zur Behandlung einer HIV-1-Infektion bei Erwachsenen zugelassen werden. Damit stellen sie die erste langwirksame, parenteral applizierbare Form der antiretroviralen Therapie (ART) dar.
Mehr zum Thema

Einmal monatlich spritzen statt mehrmals täglich schlucken
HIV-Therapie 2.0

Zulassung in Kanada
Erstes vollständiges, langwirksames Regime zur Behandlung von HIV

FDA versagt Zulassung
Rückschlag für GSKs Depot-HIV-Arznei
Laut WHO sind 38 Millionen Menschen mit dem humanen Immunodefizienzvirus infiziert, davon leben laut den Daten des RKI 87.900 in Deutschland. Obwohl es bis heute noch keine Heilungsmöglichkeit gibt, ermöglicht die antiretrovirale Therapie eine virale Suppression und verursacht damit eine Verlängerung des Überlebens und eine Verminderung des Transmissionsrisikos. Damit die virale Replikation gehemmt wird und die Zahl der CD4-positiven T-Helferzellen nicht weiter abnimmt – wodurch eine weitere Schädigung des Immunsystems voranschreiten würde – müssen aktuell mindestens zwei antiretrovirale Wirkstoffklassen in Form von einer oder mehreren Tabletten eingenommen werden. Die Einnahme erfolgt meistens einmal täglich.
Tägliche Tabletten-Einnahme durch monatliche intramuskuläre Injektion ersetzt
Durch das neue von der EMA zur Zulassung empfohlene Therapieregime wird die tägliche Tabletten-Einnahme von einer monatlichen beziehungsweise zweimonatlichen intramuskulären Injektion ersetzt. Da beide Wirkstoffe (Rilpivirin und Cabotegravir) sehr langsam metabolisiert werden, ist die Adhärenz außerordentlich wichtig, weil es sonst über einen langen Zeitraum zu subtherapeutischen Konzentrationen beider Wirkstoffe kommen würde, wodurch das Risiko einer Resistenzentwicklung stark erhöht ist. Ein weiteres Problem sind in diesem Zusammenhang auch mögliche Wechselwirkungen mit anderen Medikamenten, welche noch lange Zeit nach dem Therapiewechsel zu bedenken sind.
Daten dreier unverblindeter Phase-III-Studien
Die Kombination von Rilpivirin und Cabotegravir soll für HIV-Patienten zugelassen werden, bei denen die Viruslast unter der Nachweisgrenze (< 50 Kopien/ml) liegt und bei denen keine Resistenz gegen NNRTI und INSTI vorliegt. Zu den häufigsten Nebenwirkungen zählten neben Reaktionen an der Injektionsstelle vor allem Kopfschmerzen, Fieber, Übelkeit, Asthenie, Myalgie, Müdigkeit und Schwindel.
Mehr zum Thema

Antiretrovirale Behandlung
Erste duale HIV-Therapie erhält EU-Zulassungsempfehlung

Ein neuer Durchbruch in der AIDS-Therapie?
Die Spritze gegen HIV
Die Entscheidung des Humanarzneimittelausschusses der EMA (CHMP) basiert auf den Daten dreier randomisierter, unverblindeter, multizentrischer Phase-III-Studien, bei denen die Sicherheit und Wirksamkeit einer Kombinationstherapie aus Cabotegravir und Rilpivirin bei über 18-jährigen ART-naiven oder erfolgreich therapierten Patienten untersucht wurde. Dabei wurden beide Wirkstoffe alle vier oder acht Wochen verabreicht. Die positive Beurteilung durch den CHMP ist ein Zwischenschritt, bevor die Zulassung für Vocabria® und Rekambys® durch die Europäische Kommission erteilt werden kann.





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.