
- DAZ.online
- News
- Spektrum
- Ein Wirkstoff, zwei ...
Warum sich Fachinformationen teils stark unterscheiden
Ein Wirkstoff, zwei Hersteller – neun unterschiedliche Kontraindikationen
Rosenheim - 16.02.2022, 09:15 Uhr
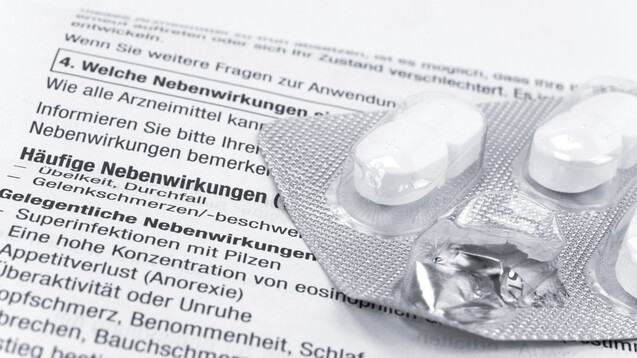
Die begleitenden Informationen zu einem Wirkstoff können sich je nach Arzneimittelpräparat unterscheiden. (c / Foto: VRD / AdobeStock)
Originatoren sollten Fachinfos harmonisieren – müssen aber nicht
„Bei einem Lisinopril-enthaltenden Präparat wurde beispielsweise als Gegenanzeige schwere Niereninsuffizienz, Dialyse, eine Verengung der Nierenarterie und spezielle Erkrankungen der Herzklappen genannt, die bei der Fachinformation eines anderen Lisinopril-enthaltenden Präparats fehlten“, schilderte Almuth Wolf in einer Pressemitteilung der Universität Ulm Ende Januar. Sie hat die Auswertung der Fachinformationen durchgeführt. Diese Diskrepanzen gefährden nicht nur die Adhärenz, sondern bürgen auch haftungsrechtliche Probleme für Ärzte. Denn seit 2002 müssen Apotheken in der Regel einen generischen Austausch vornehmen, wodurch der verordnende Arzt in der Regel gar nicht erfährt, welches genaue Präparat abgegeben wurde. Schlimmstenfalls ist es für die Indikation nicht zugelassen.
Mehr zum Thema
Rechtliche Grundlagen von Arzneimittelinformation und Kennzeichnung
Packungsbeilage - Fachinformation
Teil 1: Nationale Zulassung von neuen und bekannten Stoffen, Zulassung von Generika
Arzneimittelzulassung
Teil 2: Europäisches Zulassungssystem, Änderungen an Arzneimitteln nach der Zulassung
Arzneimittelzulassung
Wie zu erwarten, traten in der Ulmer Studie die meisten Abweichungen bei vor Jahrzehnten zugelassenen Arzneimitteln auf. Sie wurden überwiegend national zugelassen, statt – wie heute üblich – im Anerkennungsverfahren oder EU-zentral. Daher erscheint es plausibel, dass das Zulassungsverfahren ursächlich mit den Diskrepanzen zusammenhängt. Leider haben die Wissenschaftler in ihrer Untersuchung keine Daten erhoben, um diese Vermutung zu stützen. Sie deckt sich jedoch mit der Auskunft des BfArM (siehe Seite 1). Die Ursache des Problems ist laut Behörde nicht bei den Generika-Herstellern zu suchen, sondern muss bei den historisch-bedingten, nicht harmonisierten Originatoren gesucht werden. „Die CMDh (Coordination Group for mutual Recognition and Decentralised Procedures – human) bewirbt seit Jahren intensiv das Harmonisierungsverfahren durch das sogenannte Variation-Worksharing für Originatoren“, erklärt das BfArM. „Das Worksharing-Verfahren ist allerdings noch freiwillig, sodass man die Originatoren nicht verpflichten kann.“ Eine Änderung der Gesetzgebung sei bereits auf Arbeitsebene angestoßen. Wann diese greifen wird, ist jedoch zeitlich noch nicht absehbar.





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.