
- DAZ.online
- News
- Politik
- Innovative Förderung fü...
Entwurf der EU-Kommission
Innovative Förderung für bis zu zehn neue Antibiotika
Süsel - 09.02.2023, 15:15 Uhr
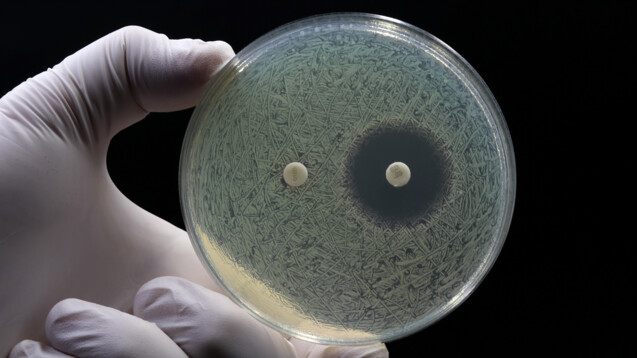
Wie lässt sich die Entwicklung neuer Antibiotika fördern? (Foto: TopMicrobialStock / AdobeStock)
Die EU-Kommission will die Entwicklung neuer Antibiotika fördern, die wesentliche Vorteile im Kampf gegen Antibiotikaresistenzen bieten. Gemäß einem Verordnungsentwurf sollen die Hersteller mit einem übertragbaren Voucher belohnt werden, der die Patentlaufzeit eines beliebigen Arzneimittels um ein Jahr verlängert. Innerhalb von 15 Jahren sollen so allerdings höchstens zehn Arzneimittel gefördert werden. Auch die übrigen Hürden erscheinen hoch.
Für die Suche nach neuen Antibiotika hat die EU-Kommission in ihrem Entwurf zur Revision der EU-Arzneimittelgesetzgebung einen neuen Anlauf gemacht. Der Verordnungsentwurf sieht einen „Exklusivitätsvoucher“ vor. Allerdings sind die geplanten Hürden hoch, und das im Entwurf formulierte Modell wird keinen großen neuen Markt öffnen, wie dies bei Arzneimitteln gegen seltene Erkrankungen zu beobachten ist.
Enge Voraussetzungen für „priority antimicrobials“
Der Vorschlag ist in den Artikeln 40 bis 42 der geplanten neuen EU-Verordnung über die Zulassung von Arzneimitteln formuliert. Diese Verordnung soll künftig die bisherige Verordnung ersetzen. Demnach soll ein Hersteller eines neuen Antibiotikums unter eng gefassten Voraussetzungen einen Voucher erhalten, der die Zeit des Unterlagenschutzes für dieses oder ein beliebiges anderes zentral zugelassenes Arzneimittel um ein Jahr verlängert. Dies soll nur für „priority antimicrobials“ gelten. Dies sollen Antibiotika sein, deren präklinische und klinische Daten einen signifikanten klinischen Vorteil hinsichtlich der Antibiotikaresistenz aufzeigen und die außerdem mindestens eine der folgenden drei Bedingungen erfüllen: Das Antibiotikum
- muss eine neue Antibiotikaklasse bilden oder
- sein Wirkungsmechanismus muss sich wesentlich von allen anderen in der EU zugelassenen Antibiotika unterscheiden oder
- sein Wirkstoff darf in der EU noch nicht zugelassen sein und er muss zur Behandlung einer mehrfach-resistenten Infektion oder einer schweren oder lebensbedrohlichen Erkrankung vorgesehen sein.
Außerdem muss der Hersteller die Fähigkeit zur Belieferung des europäischen Marktes mit dem neuen Arzneimittel belegen und die Quellen aller Forschungsgelder offenlegen, die für das Produkt verwendet wurden.
Ein Jahr mehr Patentschutz für ein beliebiges Arzneimittel
Der Voucher soll seinem Verwender erlauben, den Unterlagenschutz eines beliebigen in der EU zentral zugelassenen Arzneimittels um ein Jahr zu verlängern. Allerdings soll er nur innerhalb der ersten vier Jahre des Unterlagenschutzes anwendbar sein, also nicht für Produkte, die bereits kurz vor dem Ablauf der Schutzfrist stehen. Offenbar soll diese Einschränkung sicherstellen, dass potenzielle Generikahersteller ihren Markteintritt planen können. Der Verkauf des Vouchers an andere Hersteller ist ausdrücklich vorgesehen und soll sogar beliebig oft möglich sein. Allerdings soll der Voucher nach fünf Jahren ungültig werden. Bis dahin muss er also genutzt werden.
Mehr zum Thema

Vorschlag der Kommission
EU will europäischen Gesundheits-Datenraum schaffen
Dokument der EU-Kommission
Lieferengpässe mit Digitalisierung und grüner Arzneimittel-Produktion bekämpfen?
Die ganze Idee zielt darauf, dass ein anderes Arzneimittel dem Hersteller einen wirtschaftlichen Vorteil verschaffen soll, weil das neue Antibiotikum wirtschaftlich nicht attraktiv ist. Darum erscheint auch der Weiterverkauf konsequent. Denn möglicherweise hat der Hersteller kein passendes Arzneimittel in seinem Produktionsprogramm, um den Vorteil nutzen zu können.
Nur für maximal zehn Arzneimittel in 15 Jahren
Offensichtlich geht die EU-Kommission selbst davon aus, dass die Regelung nur ein Instrument für ganz besondere Fälle wird. Denn es sollen insgesamt über einen Zeitraum von 15 Jahren höchstens zehn Voucher ausgegeben werden. Es geht also um maximal zehn neue Arzneimittel, die auf diese Weise gefördert werden sollen. Demnach kann die Regelung nur punktuelle Forschungsanreize setzen, aber nicht den Markt insgesamt prägen. Allerdings sollen das EU-Parlament und der Rat die Dauer der Maßnahme und die Zahl der Voucher später auf der Grundlage der Erfahrungen erweitern können.
Preisbildung wie bei Versteigerung zu erwarten
Ein Markt, an dem sich ein fairer Preis für einen Voucher bildet, wie etwa bei Verschmutzungszertifikaten, wird unter diesen Bedingungen nicht entstehen. Dies wäre auch nur vorstellbar, wenn sich das Recht jeweils auf einen bestimmten Umsatz bezieht. Doch bei insgesamt höchstens zehn Fällen wird sich nicht fortlaufend ein Marktpreis bilden, sondern jeder einzelne Fall wird praktisch wie eine Versteigerung ablaufen. Voraussichtlich wird der Voucher bei dem Arzneimittelhersteller ankommen, der zum betreffenden Zeitpunkt den größten finanziellen Vorteil dadurch hat.

Europäischer Antibiotikatag
„Reserveantibiotika raus aus der industriellen Tierhaltung“

Umweltbelastung durch Medikamente
EU-Kommission will Arzneimittel-Rückstände eindämmen

Studie der EU-Kommission
Woher kommen Antibiotika ohne Rezept?
Er wird wahrscheinlich für das patentgeschützte Arzneimittel genutzt, das höchstens seit vier Jahren Unterlagenschutz hat, auch künftig eine gute Marktposition verspricht und von allen diesen Produkten den höchsten Gewinn abwirft. Der Hersteller dieses Arzneimittels wird den höchsten Preis zahlen. Nach der ökonomischen Theorie wird sich der Preis am Jahresgewinn des zweitlukrativsten Arzneimittels orientieren, weil etwas unterhalb dieses Betrages der vorletzte Wettbewerber um den Voucher aussteigt.
Bei einem EU-weiten Jahresumsatz erfolgreicher Arzneimittel im Milliardenbereich und ohne neue Forschungskosten könnte ein solcher Voucher durchaus für einen hohen dreistelligen Millionenbetrag gehandelt werden. Dies wäre also ein wirksamer Forschungsanreiz. Die Finanzierung ginge später zulasten der Beitragszahler, weil die Krankenversicherungen länger einen hohen Preis für das betreffende Arzneimittel aufbringen müssten. Die transparentere Alternative wäre eine direkte Subvention, die sofort von den Steuerzahlern finanziert werden müsste und vermutlich nicht ins Konzept der EU passen würde.






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.