
- DAZ.online
- DAZ / AZ
- DAZ 36/2018
- Weitaus mehr als grau in ...
Bildgebende Verfahren
Weitaus mehr als grau in grau
Die Sonografie ist aus dem Klinikalltag nicht wegzudenken
Die Sonografie ist somit in Kliniken und Praxen „ohne Überweisung“ rasch verfügbar und im Vergleich zu Schnittbildverfahren wie CT oder MRT relativ kostengünstig. Daher hat sie sich gewissermaßen zu einer unmittelbaren Ergänzung der körperlichen Untersuchung entwickelt. Dennoch gilt, dass ein Ultraschallbild keine wirklich präzise Wiedergabe „realer“ Anatomie oder Pathologie leisten kann. Die sonografische Darstellung kann auch Artefakte und „Störer“ beinhalten, die die Interpretation des Bildes erschweren können. Die Treffsicherheit hängt daher sehr von der Erfahrung des Untersuchers und seinen Kenntnissen der physikalischen Voraussetzungen ab.
Das Prinzip der Sonographie beruht auf dem Einsatz von Schallwellen, deren Frequenz oberhalb des vom menschlichen Gehör wahrnehmbaren Bereichs von 20 Hz bis 20 kHz liegt:
Ultraschallwellen zeigen einen Frequenzbereich zwischen 20 kHz und 1 GHz. Sie sind an Materie gebunden und breiten sich in Luft, Flüssigkeit sowie biologischem Gewebe in Form mechanischer Longitudinalwellen aus. Erzeugt werden die Schallwellen in einer (in der Regel auswechselbaren) Ultraschallsonde, die über ein Kabel mit dem Ultraschallgerät verbunden ist. Alternativ spricht man auch vom Schallkopf oder Transducer.
Von der Fledermaus über das Echolot zum Schallkopf
Der Gedanke, anatomische Strukturen durch Schall sichtbar zu machen, beruht letztendlich auf der Erkenntnis, dass Tiere wie die Fledermaus sich im dreidimensionalen Raum mithilfe von Ultraschall orientieren und fortbewegen können.
Zunächst wurde dieses Prinzip allerdings zu nautischen und militärischen Zwecken genutzt. Basierend auf den im Jahr 1880 von den Brüdern Jacques und Pierre Curie entdeckten piezoelektrischen Schallwellen wurde um die Zeit des Ersten Weltkriegs in mehreren Ländern mit Ultraschallwellen experimentiert, die durch Quarzkristalle erzeugt und unter die Wasseroberfläche ausgesendet wurden. Aus der Laufzeit (Zeit zwischen dem ausgesandten und dem wieder zurückgekehrten Signal) kann bei bekannter Schallgeschwindigkeit die Entfernung des reflektierenden Körpers errechnet werden.
Während das Echolot noch heute der elektroakustischen Bestimmung von Wassertiefen dient, ermöglichte die Weiterentwicklung zum Sonar-System (sound navigation and ranging) die Ortung von Unterseebooten. In den 1930er-Jahren wurden in Russland sowie den USA ultraschallbasierte Verfahren entwickelt, um Materialfehler in Werkstoffen zu entdecken.
Die erste medizinische Anwendung der Sonografie publizierte 1942 der österreichische Neurologe Karl Theodor Dussik, der einen Seitenventrikel des Großhirns mithilfe des Amplitudenverlaufs (A-Mode) zur Darstellung brachte.
(Indirekter) piezoelektrischer Effekt
Das Aussenden sowie das Empfangen von Ultraschallwellen beruht auf dem sogenannten, im Jahr 1880 von den Brüdern Pierre und Jacques Curie entdeckten piezoelektrischen Effekt:
- Werden elastische Körper wie etwa Piezokristalle mechanisch verformt, entsteht eine elektrische Polarisation bzw. Spannung. Hervorgerufen wird dieser Effekt durch eine Verschiebung des positiven und negativen Ladungsschwerpunkts bei ausgeübtem Druck, wodurch sich ein elektrischer Dipol und somit eine Spannung ausbildet. Piezokristalle sind Kristalle mit polaren Achsen, jedoch ohne Symmetriezentrum. Hierzu gehören z. B. α-Quarz, Turmalin, Seignette-Salz, Zinksulfid und Rohrzucker.
- Umgekehrt können elastische Körper in einem von außen angelegten elektrischen Feld ebenfalls durch eine Ladungsverschiebung deformiert werden; man spricht dann von einem umgekehrten oder indirekten piezoelektrischen Effekt.
Impuls-Echo-Prinzip
Dementsprechend regt bei der Sonografie das elektrische Signal eines Hochfrequenzgenerators den oder die im Schallkopf linear oder gekrümmt angeordneten Piezokristall(e) zu Schwingungen an. Hierdurch entstehen Druckschwankungen in Form von Ultraschallwellen, die von der Hautoberfläche ausgehend als gerichteter Impuls in die Tiefe gesendet werden (Dauer ca. 0,3 bis 0,6 μs). Dieses Signal wird je nach Inhomogenität der Organ- und Gewebestruktur unterschiedlich reflektiert, was als Echogenität bezeichnet wird. Im jetzt als Empfänger wirkenden Schallkopf erzeugt das zurückkehrende und auf die Kristalle auftreffende Echo wiederum eine elektrische Spannung. Im Ultraschallgerät selbst werden diese elektrischen Signale in Bildpunkte umgewandelt.
Ein nächster Impuls kann erst ausgesendet werden, wenn alle Echos des vorherigen Ultraschallimpulses abgeklungen sind. Daher ist die Wiederholrate abhängig von der Eindringtiefe des Ultraschalls in den zu untersuchenden Körper. Diese ist umso kleiner, je höher die Frequenz ist. Je höher allerdings die Frequenz, desto höher wiederum ist das örtliche Auflösungsvermögen, also die Fähigkeit, unmittelbar nebeneinanderliegende Objekte gerade noch auseinanderhalten zu können. Somit muss, um die bestmögliche Auflösung zu erreichen, stets die höchstmögliche Frequenz gewählt werden, die gerade noch eine Bildgebung in der gewünschten Tiefe ermöglicht. Mit anderen Worten, eine höhere Ortsauflösung geht immer auf Kosten der sonografischen Untersuchungstiefe.
Reflexion an Grenzflächen ausschlaggebend
Grundlage der sonografischen Bildentstehung ist das Phänomen, dass Schallwellen beim Durchtritt durch biologisches Gewebe abgeschwächt werden. Dies geschieht durch Reflexion und Brechung, Absorption, Streuung und Divergenz. Ausschlaggebend hierbei ist die Reflexion von Schallwellen an Grenzflächen zwischen unterschiedlichen Körperstrukturen:
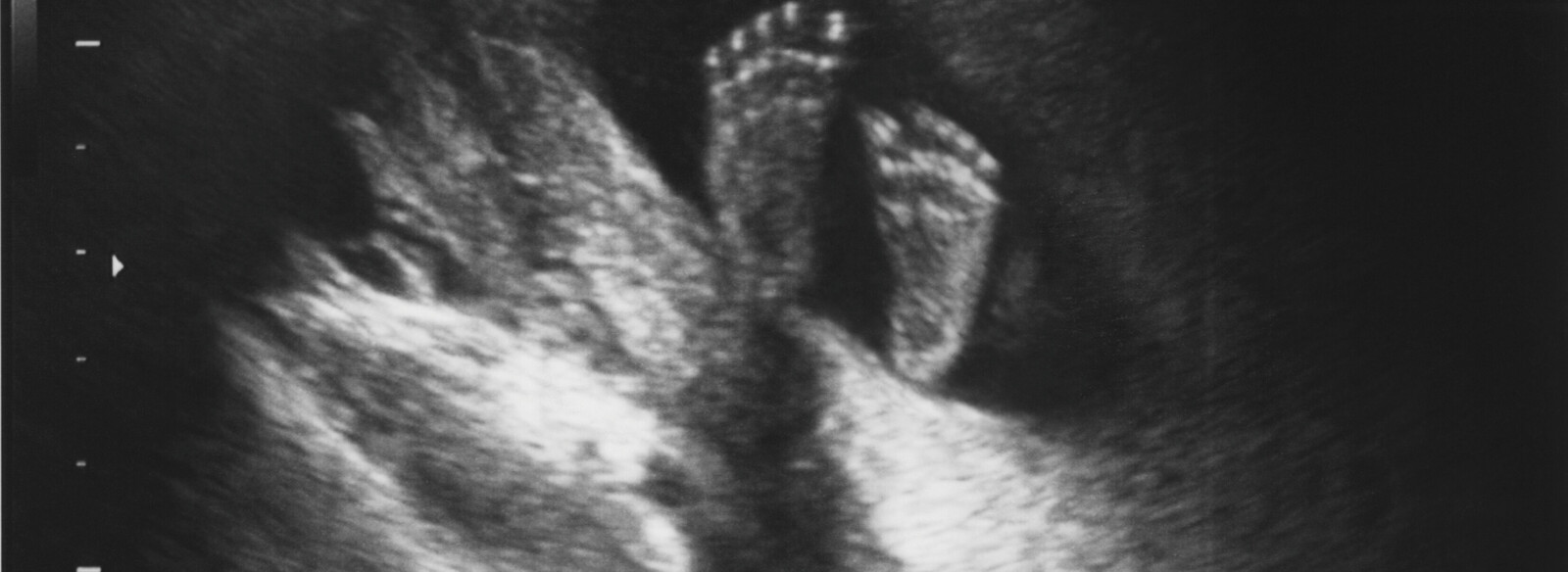
- Diese fällt umso stärker aus, je größer der Impedanzunterschied an einer solchen Grenzfläche ist (Impedanz: Maß für den Widerstand, welcher der Ausbreitung von Schallwellen entgegenwirkt). So zeigt sich etwa an den Grenzflächen von Weichteilgewebe zu Knochen, kalkdichten Konkrementen wie Gallensteinen, Metall oder Luft nahezu eine Totalreflexion. Hier entsteht also ein Echo mit sehr hoher Intensität, wobei dorsal der Grenzfläche eine Schallauslöschung resultiert (dorsaler Schallschatten, s. Abb. 1). Letztere kann zum Beispiel – bedingt durch gasgefüllte Darmschlingen – bei einer Oberbauchsonografie die Beurteilung vor allem des Pankreas erheblich erschweren.
- Der Stärke der Reflexion wird – ab der B-Mode-Darstellung, s. unten) – ein Grau- oder Helligkeitswert zugeordnet. So werden Strukturen geringer Echogenität (Flüssigkeiten wie Blut oder Urin) dunkel bis schwarz dargestellt, während Strukturen hoher Echogenität (Kalk, Knochen, Gase) hell oder weiß erscheinen.
- Von praktischer Bedeutung ist der Impedanzunterschied zwischen Raumluft und Körperoberfläche beim Aufsetzen des Schallkopfs. Damit es nicht schon an dieser Grenzfläche zu einer Totalreflexion kommt, ist die luftfreie Ankopplung mittels eines Kontaktgels unerlässlich.
- Treffen Schallwellen schräg auf Grenzflächen (vor allem auf Grenzflächen mit glatter Oberfläche und hoher Impedanz), ändert sich deren Ausbreitungsrichtung. Somit resultiert hier keine Reflexion, vielmehr kommt es zu einer Brechung des Schalls.
Weitere Faktoren der Schallabschwächung
Da Schallwellen Atome zum Schwingen bringen, entsteht Reibung. Die kinetische Energie der Schallwellen wird dadurch teilweise in Wärme umgewandelt (Absorption). Daher verringert sich die Wellenamplitude längs ihrer Ausbreitungsrichtung, die Intensität der reflektierten Welle wird also abgeschwächt. Das Ausmaß der Dämpfung hängt von der Dichte der Materie und der Wellenfrequenz ab, sie ist in Wasser beispielsweise geringer als in Weichteilgewebe. Weiterhin erfahren auf glatte Oberflächen auftreffende Schallwellen eine gerichtete Reflexion (Einfallswinkel gleich Ausfallswinkel), während „unruhige“ Oberflächen zu einer Streuung von Schallwellen führen. Je kleiner hierbei die Reflektoren im Vergleich zur Wellenlänge des Schalls sind, desto größer fällt die Fraktion der gestreuten Echos aus. Im Sonogramm zeigen sich diese als heller Schleier, wobei Kontrast und Detailschärfe deutlich abnehmen können. Ein Beispiel hierfür ist die Leberverfettung, wo die sehr feinen Fetttröpfchen eine diffus erhöhte Echodichte zur Folge haben. Demgegenüber ist die mit der Entfernung vom Schallkopf zunehmende Divergenz des Strahlenbündels nicht organ- oder gewebebedingt. Verantwortlich hierfür sind sowohl die Schallkopfkonstruktion als auch die Eindringtiefe des Schalls.
Eine grundsätzliche Kenngröße von Ultraschallwellen ist ihre Ausbreitungsgeschwindigkeit in einem beliebigen schwingenden Medium. Sie ist abhängig von der Dichte und Kompressibilität der durchdrungenen Materie und nimmt mit deren Steifigkeit zu, ist beispielsweise in Knochen also deutlich höher als in Luft (s. Tab. 1).
Medium |
Schallgeschwindigkeit [m/s] |
|---|---|
Luft |
340 |
Wasser |
1500 |
Weichteilgewebe |
1540 |
Leber |
1549 |
Niere |
1561 |
Muskel |
1570 |
Knochen |
3600 |
Artefakte können auch hilfreich sein
Neben den bereits genannten Schallschatten können sich bei der Sonografie noch weitere Artefakte bemerkbar machen. In der Regel geben diese Phänomene keine tatsächlichen anatomischen Gegebenheiten wieder, vielmehr handelt es sich um methodenbedingte und systeminhärente Bildfehler, welche die Interpretation der Darstellung erschweren können. So können Teile des Bildes gegenüber der Umgebung zu dunkel oder zu hell sein, oder es kommt zu Bildern, die geometrisch verzerrt sind. Auch können durch Spiegelungen und weitere physikalische Phänomene nicht existierende Strukturen erscheinen (s. Kasten „Typische Artefakte“).
|
dorsale Schallverstärkung
|
|
Zystenrandschatten
|
|
Rauschen
|
|
Spiegelartefakt
|
Allgemein beruht die Entstehung von Artefakten darauf, dass die in Ultraschallgeräten hinterlegten Abbildungsalgorithmen auf „idealisierten“ Annahmen zur Ausbreitung von Schallwellen im menschlichen Körper basieren. Je nach Untersuchungsbedingung ergibt sich hieraus eine gewisse „Störanfälligkeit“. Kennt der Untersucher die jeweiligen Entstehungsmechanismen, kann er diese Probleme durch Optimierung der Geräteeinstellung und Untersuchungstechnik vermeiden. So sind viele Artefakte auch daran erkennbar, dass sie sich durch Schwenken des Schallkopfs verschieben.
Allerdings können Artefakte auch hilfreich bzw. diagnostisch beweisend sein, etwa als
- kometenschweifartige Gebilde durch Auftreffen des Ultraschalls auf Cholesterolanlagerungen an der Wandung von Gallenblase und Gallenwegen.
- Totalreflexion mit Reverberationen (Wiederholungsartefakten) zwischen Leber und Brustwand in Linksseitenlage als Zeichen von freier Luft bei Hohlorganperforation.
Seltene Schadensquellen
Generell stellt die Anwendung von Ultraschall eine sichere Methode für die Bildgebung dar. Als mögliche, wenn auch sehr seltene Schadensquellen muss zum einen an thermische Effekte gedacht werden, zum anderen an die sogenannte Kavitation (lat. cavis = Höhle):
- Wärmeentwicklung: Wie schon erwähnt, erwärmt sich das beschallte Gewebe durch die Absorption von Ultraschallenergie; dies geschieht proportional zur Schallintensität bzw. -frequenz. Man geht davon aus, dass für gesundes Gewebe von Erwachsenen eine kurzfristige Temperaturerhöhung um ca. 1,5 °C unbedenklich ist. Beim Embryo dagegen kann eine Erwärmung zu Fehlbildungen wie einem zu kleinen Gehirn, Herzfehlern oder Lippen-Kiefer-Gaumen-Spalten führen.
- Kavitation: Innerhalb eines beschallten Gewebebereichs wechseln in zeitlicher Folge Druckmaxima und -minima ab. In der Unterdruckphase einer Schallwelle können hier Hohlräume und Gasbläschen entstehen, die in der Druckphase schwingen bzw. kollabieren und dadurch Läsionen verursachen können. Kavitation tritt erst ab einem bestimmten Unterdruck auf. Bei Überschreitung des Schwellenwerts können Scher- und Torsionskräfte auftreten, die biologische Membranen überlasten oder zerstören können. In Organen und Geweben, die bereits viel Luft oder Gas enthalten (Lunge, Darm), liegt die Kavitationsschwelle von vornherein niedriger.
Genaue Schallkopfposition organabhängig
Grundsätzlich lässt sich nahezu jedes Weichteilgewebe sonografisch darstellen, vor allem Organe und Strukturen, die Flüssigkeit enthalten bzw. transportieren oder gut durchblutet sind. Schlecht zu untersuchen sind alle gashaltigen oder von Knochen bedeckten Organe, zum Beispiel der Darm, die Lunge, das Gehirn und das Knochenmark. Auch sind manche Organe im Normalzustand nur schwierig, im krankhaft vergrößerten Zustand dagegen gut erkennbar (Blinddarm, Harnleiter, Nebennieren). Somit eignet sich die Sonografie mit auf der Hautoberfläche platzierter Ultraschallsonde für die Untersuchung folgender Organe:
- Leber, Gallenblase und Gallengänge, Milz, Bauchspeicheldrüse, Nieren, Lymphknoten (Vergrößerung, Tumore, Zysten, Steinleiden),
- arterielle und venöse Blutgefäße außer innerhalb des knöchernen Schädels (Stenosen, Thromben, Verschlüsse),
- Muskeln, Gelenke (Schwellungen, Verletzungen, Ergüsse),
- Schilddrüse (Vergrößerung/Verkleinerung, Zysten, Tumore),
- weibliche Brust (Zysten, Verkalkungen, Tumore),
- Herz (als transthorakale Echokardiografie: Wandbewegungsstörung durch Ischämie/Infarkt, Kardiomyopathie, Herzklappenfehler, Perikarderguss).
Hierbei setzt der Untersucher den Schallkopf in verschiedenen, für die einzelnen Organe klassischen Schnitten auf (z. B. transversal, subkostal, Schulter-Nabel-Schnitt) und beurteilt durch Kippen und Lageveränderung des Schallkopfs das Organ und benachbarte Strukturen. Dabei ist zu berücksichtigen, dass die Sonografie in tiefer gelegenen Schichten eine geringere Auflösung bietet als die Computer- und Magnetresonanztomografie. Problematisch kann auch sein, dass sich Flüssigkeiten (z. B. frisches Blut gegenüber Aszites) sonografisch nicht unterscheiden oder dass eine eingeschmolzene Metastase die Kriterien einer Zyste erfüllt.
Demgegenüber werden bei der sogenannten Endosonografie spezielle Sonden in Körperhohlräume eingeführt, z. B. in die Vagina, in das Rektum, oder auch in den Ösophagus bzw. Magen. Somit lassen sich auch von außen schwer beurteilbare Bereiche darstellen, etwa die Ovarien und/oder der Uterus transvaginal oder die Prostata transanal. Transösophageal durchgeführt ist das Zielorgan zumeist das Herz, z. B. zur Suche nach Blutgerinnseln im linken Vorhof als kardiale Emboliequelle bei Vorhofflimmern oder zur Feststellung von Endokarditiskomplikationen bzw. Herzklappenfehlern.
Somit kann eine Ultraschalluntersuchung je nach Anforderung mit unterschiedlichen Sonden und Techniken durchgeführt werden. Ebenso stehen unterschiedliche Systeme zur Verfügung, was die Auswertung und Bildrekonstruktion der Messergebnisse betrifft (s. Kasten „Unterschiedliche Systeme zur sonografischen Bildrekonstruktion“).
|
A-Mode (Amplitudenmodus)
|
|
B-Mode (Brightness-Mode)
|
|
M-Mode (Motion-Mode)
|
|
3D-Ultraschall
|
Den Blutfluss hörbar machen
Die Aussagekraft der sonografischen Darstellung kann je nach Indikation durch die Anwendung des Doppler-Effekts erhöht werden, der im Jahr 1842 von dem österreichischen Mathematiker und Physiker Christian Johann Doppler entdeckt wurde. Vereinfacht dargestellt kommt es bei einer relativen Bewegung zwischen Sender und Empfänger zu einer Veränderung der Wellenfrequenz. So erscheint einem stehenden Beobachter die Frequenz einer sich nähernden Schallquelle höher als die einer stehenden Schallquelle. Umgekehrt wird die Frequenz bei der Entfernung der Schallquelle tiefer wahrgenommen.
Der Doppler-Effekt entsteht auch bei der Reflexion einer mechanischen Welle an einem bewegten Objekt wie einer Blutsäule. Die Erythrozyten fungieren somit als Grenzfläche, an denen vom Schallkopf als „ruhender“ Sender kommende Ultraschallwellen einer definierten Frequenz reflektiert werden. Verringert sich die Entfernung des Schallkopfes zu dieser Grenzfläche, nimmt die Frequenz zu, während sie bei größer werdender Entfernung abfällt. Der Computer errechnet aus der Verschiebung zwischen ausgesandter und reflektierter bzw. empfangener Frequenz die Blutflussgeschwindigkeit in Abhängigkeit vom Messwinkel (resultierend aus der Position des Schallkopfs). Die auf dem Monitor sichtbaren dynamischen Flussmuster können über Lautsprecher als frequenzabhängiges Rauschen hörbar gemacht werden. Bei der farbcodierten Doppler-Sonografie werden Bewegungen auf den Schallkopf zu typischerweise mit der Farbe Rot und solche vom Schallkopf weg mit der Farbe Blau überlagert.
Die Doppler-Domänen: Gefäßerkrankungen und Schwangerschaft
Die Doppler-Sonografie ist heute eine Routinemethode in der Diagnose von Gefäßerkrankungen. Eine Erweiterung stellt die sogenannte Duplex-Sonografie dar, eine Kombination aus Ultraschallschnittbildgerät und Doppler-Einrichtung. Zusätzlich zum Blutfluss als solchem werden hier die Blutgefäße und/oder das Herz als flächiges Bild mit dargestellt.
Zu den angiologischen bzw. kardiovaskulären Indikationen gehören:
- Screening bei peripherer arterieller Verschlusskrankheit (pAVK),
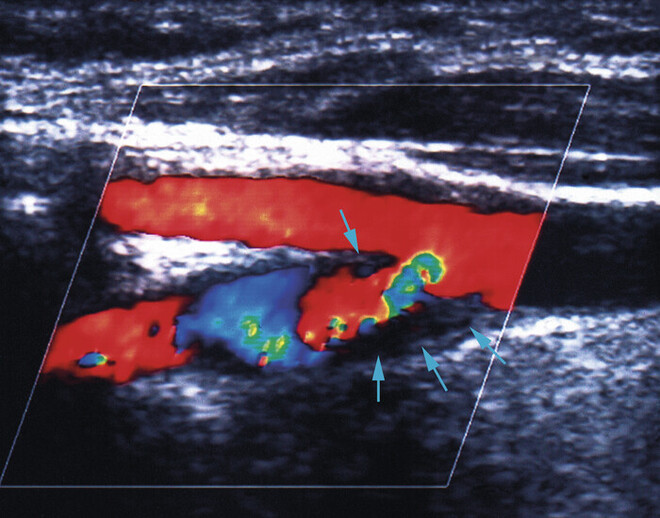
- Nachweis einer Stenose hirnversorgender Gefäße, z. B. der A. carotis (s. Abb. 2),
- Nachweis einer Gefäßaussackung (Aneurysma),
- Erfolgs- und Verlaufskontrolle nach gefäßchirurgischem Eingriff (z. B. Stentimplatation, Thrombusentfernung bei akutem arteriellem Gefäßverschluss, Bypass einer Extremitätenarterie, vaskuläre Versorgung einer transplantierten Niere),
- Nachweis venöser Thrombosen,
- Beurteilung einer chronisch-venösen Insuffizienz.
In der (neurochirurgischen) Notfall- und Intensivmedizin kann durch eine dünne Knochenlamelle im Schläfenbereich der Blutfluss in den zerebralen Arterien (Aa. cerebri media, anterior und posterior) bestimmt werden. Wichtigste Indikationen sind ein gesteigerter Hirndruck (z. B. nach Trauma), der Verdacht auf eine Subarachnoidalblutung oder ein zerebraler Kreislaufstillstand (im Rahmen der Hirntoddiagnostik).
Wichtige fetomaternale Zielgefäße sind die Nabelschnurarterien, die Aa. uterinae sowie im fetalen Kreislauf die Aorta, der Aortenisthmus und die A. cerebri media. Folgende Verdachtsdiagnosen oder Indikationen zur Doppler-Untersuchung sind in den Mutterschaftsrichtlinien festgelegt:
- Verdacht auf intrauterine Wachstumsretardierung,
- Zustand nach Mangelgeburt oder intrauterinem Fruchttod,
- schwangerschaftsinduzierte Hypertonie bzw. Präeklampsie,
- Zustand nach Präeklampsie/Eklampsie in vorheriger Schwangerschaft,
- Auffälligkeiten der fetalen Herzfrequenz,
- begründeter Verdacht auf Fehlbildung oder fetale Erkrankung (vor allem angeborene Herzfehler),
- Mehrlingsschwangerschaften mit diskordantem Wachstum.
Alternative zur Mammografie?
Bei jüngeren Frauen mit dichtem Brustgewebe ist die Sensitivität der Mammografie deutlich vermindert bei gleichzeitig gesteigertem Brustkrebsrisiko. Insbesondere die Inzidenz von Intervallkarzinomen ist hier ca. 18-fach erhöht (im Intervall zwischen zwei Screeninguntersuchungen auftretendes oft rasch wachsendes Karzinom). Mammografiebilder sind hier schwerer zu beurteilen als bei älteren Frauen mit lockerem Brustgewebe. Darüber hinaus tritt etwa ein Viertel der Mammakarzinome bei Frauen zwischen 40 und 49 Jahren auf, also unterhalb des Mindestalters für das Mammografiescreening.
Hier sollte bei unklaren Tastbefunden oder einseitiger Schmerzhaftigkeit schnellstmöglich eine Brustultraschalluntersuchung durchgeführt werden. Gutartige Prozesse wie Zysten oder Tumore wie Fibroadenome lassen sich sonografisch meist zuverlässig von malignen Tumoren differenzieren. Allerdings besteht die Gefahr, dass Mikroverkalkungen als möglicher Hinweis auf ein Mammakarzinom nicht sicher erkannt werden.
Nicht zuletzt deshalb wird in den derzeit gültigen Leitlinien der systematische Einsatz der Sonografie nicht als alleinige Methode zur Brustkrebsfrüherkennung empfohlen.
Grundsätzlich wird die Ultraschalluntersuchung dann eingesetzt, wenn eine Mammografie kein eindeutiges Ergebnis zeigt. Oft kann aus unklaren Herdbefunden der Brust unter Ultraschallkontrolle per Biopsie in lokaler Betäubung eine repräsentative Probe gewonnen und damit eventuell eine Operation vermieden werden. |
Literatur
[1] Hünerbein R. Radiologische Verfahren. In: Reiser M, Kuhn FP, Debus J (Hrsg.). Radiologie. Georg Thieme Verlag 4. Auflage 2017
[2] Jaspers N, Michels G. Technische und physikalische Grundlagen. In: Michels G, Jaspers N (Hrsg.). Sonographie organ- und leitsymptomorientiert. Springer Verlag 1. Auflage 2012
[3] Strahlenschutzkommission. Ultraschallanwendung am Menschen. Verabschiedet in der 256. Sitzung der Strahlenschutzkommission am 19. und 20. April 2012
[4] Tuma J, Jenssen C, Möller K et al. Artefakte in der Sonografie und ihre Bedeutung für die internistische und gastroenterologische Diagnostik – Teil 1: B-Mode-Artefakte. Z Gastroenterol 2016;54:433-450
[5] Stenzel M, Mutze S, Dahse HP et al. Sonographie Standard – Abdomen. Empfehlungen der Sektion Radiologie der DEGUM (Deutsche Gesellschaft für Ultraschall in der Medizin) 2007
[6] Leitlinie der Deutschen Gesellschaft für Gynäkologie und Geburtshilfe e. V. Standards in der Perinatalmedizin – Dopplersonographie in der Schwangerschaft. AWMF-Register Nr. 015/019m, Juni 2012
[7] Leitlinienprogramm Onkologie. Interdisziplinäre S3-Leitlinie für die Früherkennung, Diagnostik, Therapie und Nachsorge des Mammakarzinoms. AWMF-Registernummer: 032-045OL, November 2017
[8] Leinmüller R. Zusätzlicher Ultraschall bei dichter Brust gefordert. Deutsches Ärzteblatt 2010;46:A2287-A2288
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.